- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Множественная миелома и другие парапротеинемии
Содержание
- 2. Моноклональные гаммапатииГруппа заболеваний, характеризующаяся пролиферацией одного клона плазматических клеток, продуцирующих электрофоретически и иммунологически гомогенный (моноклональный)протеин.
- 3. Моноклоновая ү-патия. Моноклоновый белок сыворотки при денситометрии после электрофореза на агарозном геле. Пик в ү-фракции .
- 4. Иммунофиксация выявляет моноклональный белок IgA k .
- 5. Моноклональные гаммапатии I. Моноклональные гаммапатии неопределенного
- 6. II.Злокачественные моноклональные гаммапатии1. Множественная миелома (Симптоматическая миелома)*.2.
- 7. Вариантные (редкие) формы множественной миеломы*А) несекретирующая множественная миеломаБ) остеосклеротическая форма миеломыС) биклональная миеломаД) плазмоклеточный лейкоз
- 8. Незлокачественные заболевания, редко ассоциирующиеся с моноклональными протеинамиЗаболевания
- 9. 3. Заболевания печени- хронические гепатиты, - первичный
- 10. Причины 1068 случаев моноклональной гаммапатии по данным
- 11. Диагностические критерии МГНЗ ( MGUS) (
- 12. Солитарная плазмацитома кости ( требуются все три
- 13. Крупный опухолевый узел в верхней доле правого легкого.Внекостная плазмоцитома
- 14. Рекомендации по ведению солитарной экстрамедуллярной плазмацитомы (Guidelines
- 15. Тлеющая или индолентная (бессимптомная) миелома Моноклональный протеин
- 16. Множественная миелома – плазмоклеточная опухоль, характеризующаяся увеличением
- 17. ЭпидемиологияММ составляет 1% всех онкологических заболеванийММ составляет
- 18. Этиологические факторы Генетическая предрасположенность ( расовые различия,
- 19. При множественной миеломе объектом опухолевой трансформации является
- 20. Патогенез и патофизиология миеломной болезниПервый патогенетический шаг
- 21. Патогенез миеломы14q32 regionBCL1/PRAD-1/cyclin D1 (11q23), cyclin D3 (6p21), FGFR3-MMSET (4p16.3), c-maf (16q23), mafB (20q11)
- 22. Регуляция скорости роста опухолевых клеток при ММ
- 23. Диагностические критерии множественной миеломы ( требуется наличие
- 24. C (calcium) – кальций сыворотки >0,25ммоль/л выше
- 25. Клинические проявления ММПоражение костей Множественные остеолитические очаги
- 26. Периферическая кровьАнемия, ускорение СОЭ, реже- лейкопения, тромбоцитопения,
- 27. Нарушения со стороны почекПротеинурия, цилиндры без эритроцитов
- 28. Лабораторные исследования при миеломе Полный клинический анализ
- 29. Электрофорез –иммунофиксация (сыворотки или концентрированной мочи)Количественная оценка
- 30. Цитогенетические аномалии при миеломеИспользование стандартных методов цитогенетического
- 31. Цитогенетические изменения при ММ- гипердиплоидия – трисомия
- 32. Группы риска при множественной миеломе (Клиника Мейо,США
- 33. Плазматические клетки при миеломной болезни
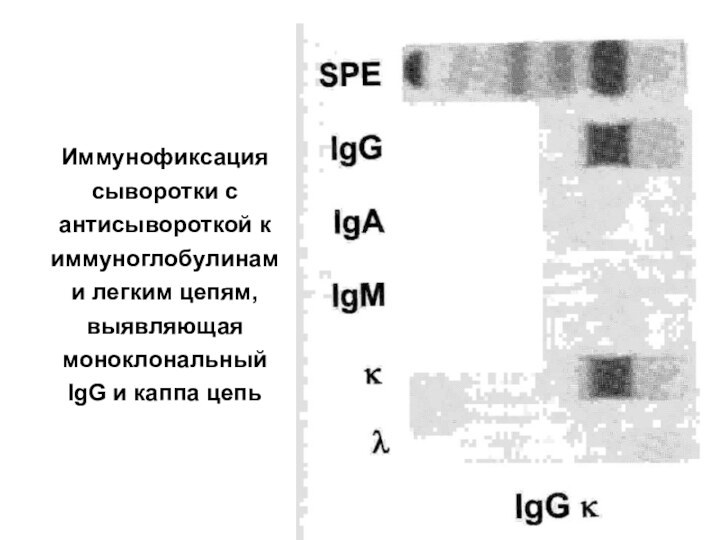
- 34. Иммунофиксация сыворотки с антисывороткой к иммуноглобулинам и легким цепям, выявляющая моноклональный IgG и каппа цепь
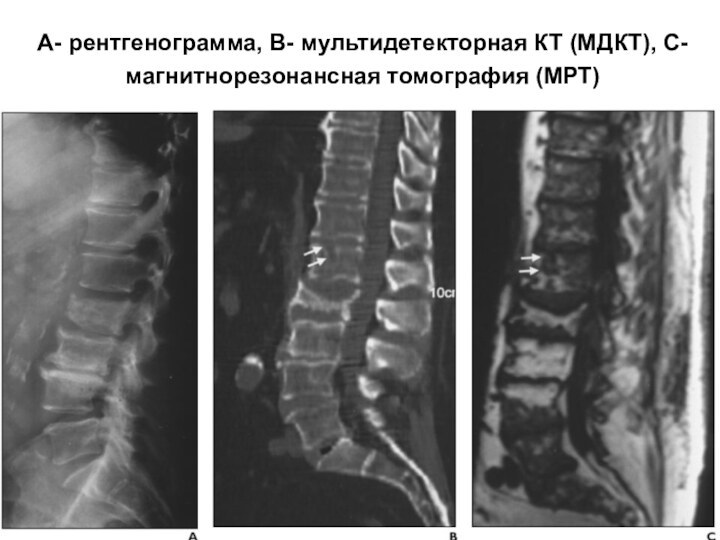
- 38. А- рентгенограмма, В- мультидетекторная КТ (МДКТ), С- магнитнорезонансная томография (МРТ)
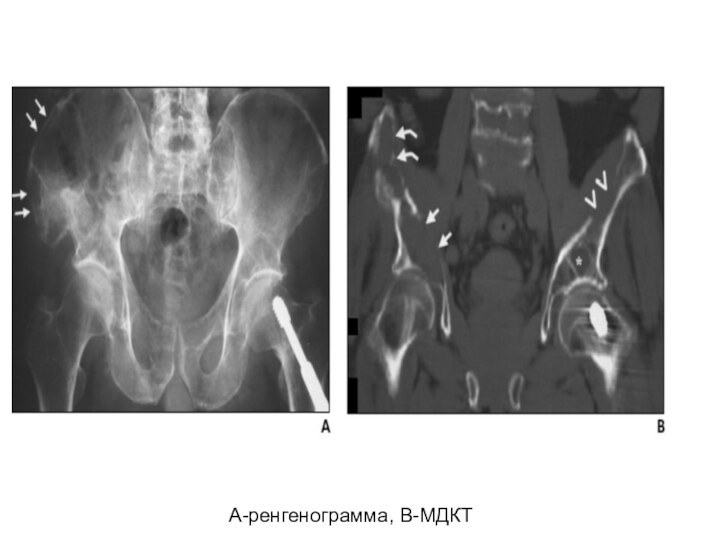
- 39. А-ренгенограмма, В-МДКТ
- 42. Иммунохимические варианты множественной миеломыВариантЧастота,%G-миелома55-65А-миелома20-25D-миелома2-5Е-миеломаТочно не установленаБолезнь легких цепей ( миелома Бенс-Джонса)12-20Диклоновые миеломы1-4М-миелома0,5
- 43. Стадии множественной миеломы по Durie/Salmon.СтадияКритерии1А,ВУровень Hb >100
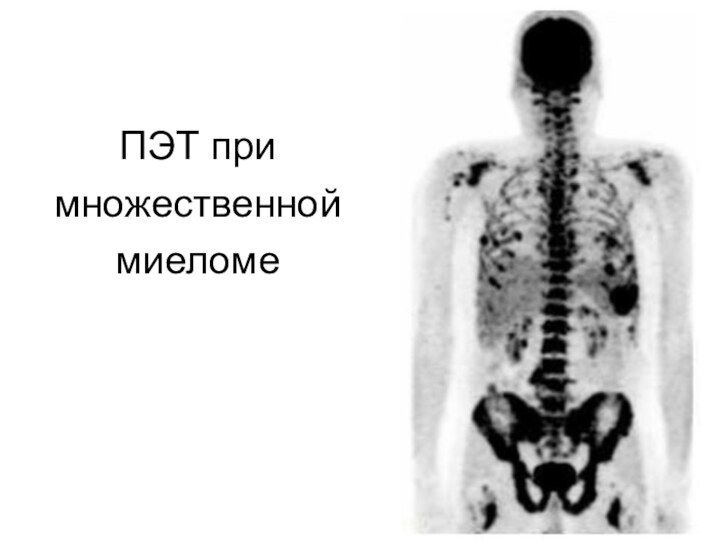
- 44. ПЭТ при множественноймиеломе
- 45. Durie/Salmon PLUS система стадирования множественной миеломы Классификация
- 46. Стадии ММ по SWOG системе (2003 г)
- 47. Прогностические факторы при множественной миеломеВозрастСоматический статусΒ2-микроглобулинАльбумин сывороткиКреатинин
- 48. Международный прогностический индекс при ММIPI группа 1
- 49. Группы риска при множественной миеломе (Клиника Мейо,США
- 50. Индукционная терапия при множественной миеломеВозраст < 65
- 51. Программы ХТ больных ММVADвинкристина 0,4 мг/24 часа
- 52. Лечение осложнений миеломыОсложнениеТерапевтические подходыПоражение костейБифосфонаты (бонефос, аредиа,
- 53. Анемияпри симптомах анемии эритропоэтин во время химиотерапии
- 54. Почечная недостаточ-ностьКоррекция обратимых причин, таких как дегидратация,
- 55. Трансплантация стволовых клетокПо сравнению с со стандартными
- 56. Общая выживаемость больных множественной миеломойАнализ выживаемости 2981
- 57. Факторы влияющие на эффективность лечения больных множественной
- 58. Макроглобулинемия Вальденстрёма –злокачественное лимфопролиферативное заболевание с продукцией
- 59. Макроглобулинемия ВальденстремаВпервые описана в 1944 г. Jan
- 60. Этиология и предрасполагающие факторы-предшествующая IgM-MGUS;-генетическая предрасположенность;-хроническая антигенная стимуляция(инфекции,аутоиммунные процессы и т.д.);-возможная связь с вирусом гепатита С;
- 61. Патогенетические механизмы развития Макроглобулинемии ВальденстремаГеномные нарушения -
- 62. Макроглобулинемия Вальденстрема. Характеризуется наличием моноклонального иммуноглобулина М
- 63. Диагностические критерии-Моноклональный IgM сыворотки крови ;-лимфоплазмоцитарная инфильтрация
- 64. Прогностические факторы возраст > 65 лет;β2-микроглобулин >3
- 65. Клиническая манифестация макроглобулинемии ВальденстремаСимптомыПризнакиСлабость, усталостьСимптомы гипервязкостиНочная потливостьПотеря
- 66. Признаки синдрома гипервязкостиКровотечение из носа и десен,
- 67. Критерии начала терапии-лихорадка, ночная потливость, слабость, снижение
- 68. Лечение макроглобулинемии ВальденстремаПлазмаферез – с возмещением альбумином
- 69. Болезни тяжелых цепейВ-клеточные лимфатические опухоли с крайне
- 70. В соответствии с классом Н-цепей, синтезируемых опухолевыми
- 71. Морфологические методы исследования в отличие от других
- 72. Клиническая картина вариабельна и определяется распространенностью процесса и поражением тех или иных органов.
- 73. ЗаболеваниеБТЦ үБТЦ αБТЦ μВозраст Средний возраст 60
- 74. Скачать презентацию
- 75. Похожие презентации





































































Слайд 2
Моноклональные гаммапатии
Группа заболеваний, характеризующаяся пролиферацией одного клона плазматических
клеток, продуцирующих электрофоретически и иммунологически гомогенный (моноклональный)
Слайд 3 Моноклоновая ү-патия. Моноклоновый белок сыворотки при денситометрии после электрофореза
на агарозном геле. Пик в ү-фракции .
Слайд 5
Моноклональные гаммапатии
I. Моноклональные гаммапатии
неопределенного значения (MGUS)
А)
доброкачественная (IgG, IgA, IgD, IgM)
Б) ассоциированная со злокачественными заболеваниями,
не продуцирующими моноклональные протеины.
Слайд 6
II.Злокачественные моноклональные гаммапатии
1. Множественная миелома (Симптоматическая миелома)*.
2. Вялотекущая
(тлеющая) или индолентная миелома.
3. Плазмацитома.
А) Солитарная плазмацитома костей.
Б) Экстрамедуллярная
плазмацитома.4. Злокачественные лимфопролиферативные заболевания
А) Макроглобулинемия Вальденстрема
Б) Неходжкинские лимфомы
5. Болезнь тяжелых цепей (γ,α,µ)
6. Амилоидоз (первичный AL-амилоидоз и вторичный)
Слайд 7
Вариантные (редкие) формы множественной миеломы*
А) несекретирующая множественная миелома
Б)
остеосклеротическая форма миеломы
С) биклональная миелома
Д) плазмоклеточный лейкоз
Слайд 8
Незлокачественные заболевания, редко ассоциирующиеся с моноклональными протеинами
Заболевания кожи.
-
гангренозная пиодермия,
- лихеноидный микседематоз (IgG лямбда),
- ксантогранулема,
-
псориаз,- дискоидный волчаночный эритематоз (кожная форма СКВ),
- склеродерма ( кожная форма склеродермии),
2. Лимфопролиферативные синдромы, ассоциированные с иммунодефицитом.
- СПИД ,
- трансплантация почки, трансплантация костного мозга.
Слайд 9
3. Заболевания печени
- хронические гепатиты,
- первичный билиарный
цирроз печени.
4. Аутоимунные заболевания
- ревматоидный артрит,
- полимиозит (IgG
каппа), - ревматическая полимиалгия,
- miasthenia gravis
-воспалительные серонегативные полиартриты,
4. Неклассифицируемые
Слайд 10 Причины 1068 случаев моноклональной гаммапатии по данным клиники
Mейo, 2001 г.
MGUS – 62%
Множественная миелома – 16%
AL-амилоидоз –
8%Тлеющая миелома – 4%
Болезнь Вальденстрема – 3%
Лимфопролиферативные заболевания – 3%
Солитарная или экстрамедуллярная
плазмацитома – 1%
Другие – 3%
Слайд 11 Диагностические критерии МГНЗ ( MGUS) ( требуется наличие
всех трех)
Уровень моноклонального белка сыворотки и/или мочи повышен, но
ниже, чем при множественной миеломе ( IgG сыворотки <30 g/l, IgA <20 g/l, моноклональные цепи каппа или лямбда Ig в моче <1 g/ 24 часа)2. Моноклональные плазматические клетки в костном мозге менее 10%
3. - нормальный уровень кальция, гемоглобина и креатинина крови
- отсутствие остеодеструктивного синдрома и остеопороза при рентгенологическом и др. методах исследования
- отсутствие клинических и лабораторно-инструментальных признаков амилоидоза, паранеопластического синдрома
Слайд 12
Солитарная плазмацитома кости ( требуются все три критерия)
1.
Доказанная биопсией моноклональная плазмацитома кости в единственном месте по
данным рентгенологического, МРТ и/или ФДГ ПЭКТ исследований ( если должны быть негативны вне первичного очага). Первичное повреждение может быть ассоциировано с низким М-компонентом в сыворотке и /или моче( IgG <35 g/l, IgA <20 g/l Ig , моноклональные цепи каппа или лямбда <1 g/ 24 часа2. Костный мозг содержит менее 10% моноклональных плазматических клеток
3. Отсутствуют дисфункции органов, ассоциированные с миеломой
Слайд 14 Рекомендации по ведению солитарной экстрамедуллярной плазмацитомы (Guidelines Working
Group of the UK Myeloma Forum,2004)
Выполнение КТ и МРТ
необходимо для получения пространственного изображения и исключения других очагов.Диагноз устанавливается на основании биопсии и проведения дифференциального диагноза с неходжкинскими лимфомами и множественной миеломой.
Лучевая терапия – метод выбора при плазмацитомах шеи и головы.
Солитарная экстрамедуллярная плазмацитома должна быть удалена хирургическим путем, если это выполнимо.
Неоперированные пациенты должны получать химиотерапию как при множественной миеломе.
Оптимальным можно считать комбинированное лечение – химиотерапия+ лучевая терапия
Слайд 15
Тлеющая или индолентная (бессимптомная) миелома
Моноклональный протеин присутствует в
сыворотке ( ≥ 30 г/л) и/или моче
2. Моноклональные плазматические
клетки ≥10% в костном мозге 3. Нет поражения органов-мишеней (отсутствуют CRAB критерии).
Нет критериев, удовлетворяющих критериям MGUS, множественной миеломы или солитарной плазмацитомы кости или мягких тканей
Слайд 16 Множественная миелома – плазмоклеточная опухоль, характеризующаяся увеличением плазматических
клеток в костном мозге, повышенной продукцией моноклонового белка, деструктивным
поражением скелета, развитием почечной недостаточности, анемии и гиперкальциемии. Заболевание относится к группе злокачественных моноклоновых гаммапатий. В последней классификации ВОЗ лимфоидных опухолей (1997) заболевание относится к группе В-клеточных опухолей с фенотипом зрелых (периферических) клеток и охарактеризовано как миелома или плазмоцитома (солитарная и внекостная). Синонимами термина множественная миелома являются миелома, плазмоклеточная миелома, активная миелома, симптоматическая миелома, болезнь Рустицкого-Калера.
Слайд 17
Эпидемиология
ММ составляет 1% всех онкологических заболеваний
ММ составляет около
10% всех гемобластозов
Люди монголоидной расы болеют ММ крайне редко
(за исключением японцев), а негроидной – значительно чаще, чем европеоиднойЧастота ММ составляет 1- 4 случаев на 100 000 населения
Соотношение мужчин и женщин составляет 3:2
ММ встречается в возрасте 18-85 лет. Частота заболеваемости увеличивается с возрастом, средний возраст - 69 лет
Слайд 18
Этиологические факторы
Генетическая предрасположенность ( расовые различия, семейные случаи)
Хроническая
антигенная стимуляция ( инфекции, воспаление, заболевания соединительной ткани, аутоиммунные
процессы, аллергические заболевания, ревматоидный артрит)этиологическая роль вирусов ( ВИЧ, гепитит С, герпесвирус 8) и ионизирующего излучения?
Слайд 19 При множественной миеломе объектом опухолевой трансформации является клетка-предшественница
В-лимфоцитов
(клетка, проделавшая этапы антиген-зависимой дифферецировки, переключения изотипов Н-цепей Ig
и гипермутаций V-региона) . Будучи опухолевой, она способна дифференцироваться до конечного этапа – плазматической клетки, секретирующей моноклональный Ig.
Слайд 20
Патогенез и патофизиология миеломной болезни
Первый патогенетический шаг –в
развитии миеломы – появление ограниченного количества клональных плазматических клеток,
клинически обозначаемого как MGUS ( моноклональная гаммапатия неопределенного значения)Ежегодный риск трансформации MGUS в множественную миелому - 1%
Ежегодный риск трансформации тлеющей миеломы в множественную миелому 10% в год в первые 5 лет, 5% в год следующие 5 лет и 1-2% в год в последующие годы.
65% пациентов имеют цитогенетические изменения в виде транслокаций, которые вовлекают локус тяжелой цепи иммуноглобулинов на хромосоме 14q32 и одну из пяти хромосом-партнеров 11q13 ( ССТВ1) (наиболее часто), 4р16.3 ( FGFR-3 и MMSET), 6q21 (CCND3), 16q23 ( c-maf) и 20q11 (mafB), которые играют важную роль в эволюции MGUS.
Слайд 21
Патогенез миеломы
14q32 region
BCL1/PRAD-1/cyclin D1 (11q23), cyclin D3 (6p21),
FGFR3-MMSET (4p16.3), c-maf (16q23), mafB (20q11)
Слайд 22 Регуляция скорости роста опухолевых клеток при ММ осуществляется
рядом интерлейкинов и факторов роста, секретируемых стромальными клетками костного
мозга, самими миеломными клетками, а также иммунокомпетентными клетками микроокружения.Миеломная клетка способна непосредственно (через аутокринный механизм) и опосредованно (через стромальные клетки) поддерживать свой рост/пролиферацию, неконтролируемую продукцию моноклонового белка, и блокировать процессы апоптоза.
Слайд 23 Диагностические критерии множественной миеломы ( требуется наличие всех
трех)
1. Моноклональные плазматические клетки в костном мозге >10% или
наличие доказанной при биопсии плазмацитомы2. Присутствие моноклонального белка в сыворотке и/или моче ( если моноклональный белок не выявляется ( несекретирующая миелома), требуется более 30% плазматических клеток и/или плазмоцитома)
3. Связанные с миеломой органные дисфункции (CRAB):
Гиперкальциемия >10,5 мг/л или верхняя граница нормы
Почечная недостаточность с креатинином > 2 мг/дл
Анемия с гемоглобином менее 100 г/л или на 20 г ниже нормы
Литические поражения костей или остеопороз
Слайд 24 C (calcium) – кальций сыворотки >0,25ммоль/л выше верхних
нормальных значений(>2,75 ммоль/л)
R (renal) – нарушение функции почек (креатинин
>173 ммоль/л)A (anemia) – анемия (гемоглобин <100 г/л)
B (bone) – костные повреждения (литическое повреждение или остеопороз)
Критерии CRAB
Слайд 25
Клинические проявления ММ
Поражение костей
Множественные остеолитические очаги повреждения
плоских костей и эпифизов трубчатых костей
Диффузный остеопороз (остеопения)
Костные переломы
Уменьшение
роста (вертебральный коллапс)Болевой синдром
Эффекты, ассоциированные с остеодеструкцией
Гиперкальциемия у 20-40%
( утомляемость, жажда, тошнота, запоры, повреждение почек, полиурия, сонливость, судороги, кома)
Гиперкальцийурия
Внекостные плазмацитомы
Вовлечение мягких тканей преимущественно в области головы/шеи, очаги в печени, почках, легких и т.д.
Слайд 26
Периферическая кровь
Анемия, ускорение СОЭ, реже- лейкопения, тромбоцитопения,
Нарушение
свертывания крови
Циркулирующие плазмоциты и плазмобласты
Изменения белков плазмы
Гиперпротеинемия (синдром гипервязкости)
Гиперволемия
Моноклональные
иммуноглобулины (снижение уровня нормальных иммуноглобулинов)Повышенный β2-микроглобулин
Гипоальбуминемия
Повышенный СРБ и ИЛ6 сыворотки
Гипонатриемия, возможна гиперкалиемия
Слайд 27
Нарушения со стороны почек
Протеинурия, цилиндры без эритроцитов и
лейкоцитов
Канальцевая дисфункция с ацидозом
Почечная недостаточность
Иммуно-супрессия
Бактериальные инфекции ( пневмококк)
Вирусные инфекции
( в т.ч. Herpes zoster)Нарушения со стороны нервной системы
периферическая нейропатия
компрессия спинного мозга при поражении позвоночника
( радикулярный синдром, парезы и параличи)
Общие симптомы
Общая слабость, недомогание, похудание,
Слайд 28
Лабораторные исследования при миеломе
Полный клинический анализ крови,
СОЭ
Биохимическое исследование сыворотки крови с оценкой: общего белка и
белковых фракций ( электрофорез) , мочевины, креатинина, мочевой кислоты, кальцияСуточная потеря белка с мочой, электрофорез белков мочи
Общий анализ мочи, определение белка Бенс-Джонса
Протромбиновое время, АПТВ
Слайд 29
Электрофорез –иммунофиксация (сыворотки или концентрированной мочи)
Количественная оценка уровня
иммуноглобулинов сыворотки крови
Рентгенологическое исследование костей, КТ, МРТ, ПЭКТ, сцинтиграфия
костей скелета, денситометрияАспирационная биопсия костного мозга, трепанобиопсия
СРБ, в2-микроглобулин, ЛДГ, ИЛ-6
Определение пролиферативного индекса и количества Ki-67-положительных плазматических клеток
Цитогенетическое исследование
Иммунофенотипирование?
Слайд 30
Цитогенетические аномалии при миеломе
Использование стандартных методов цитогенетического исследования
(метафазы)выявляет аномалии кариотипа у 18-30% больных на ранних этапах
заболевания и у 50-60% - в далеко зашедших стадияхМетод флюоресцентной in situ гибридизации
( FISH ) выявляет аномалии в 90% случаев.
Метод секвенирования генов и метод microarray гибридизации выявляет экспрессию 9732 генов.Составлен каталог экспрессированных генов при множественной миеломе (Myeloma Gene Index). На основании выявления активации 70 основных генов выделяют агрессивные формы множественной миеломы с прогнозируемой длительностью жизни менее 1 года.
Слайд 31
Цитогенетические изменения при ММ
- гипердиплоидия – трисомия 6,
7, 9, 11, 15, 17, 19, 21 хромосом -
10% (прогноз хороший)- t (11;14) - 20%
- t (6;14) - <5%
- t (4;14) - 15%
- t (14;16) – 5%
- del 13q - 10%
- del 17p (p53) – 10%
Слайд 32
Группы риска при множественной миеломе (Клиника Мейо,США 2008)
Стандартный
риск (75%)
Высокий риск (25%)
FISH транслокация 11;14
FISH транслокация 6;14
гипердиплоидия
Все другие
FISH и цитогенетические нарушенияFISH делеция 17p
FISH транслокация 4;14
FISH транслокация 14;16
Делеция 13q
Гиподиплоидия
пролиферативный
индекс плазматических клеток ≥ 3%
Слайд 34 Иммунофиксация сыворотки с антисывороткой к иммуноглобулинам и легким
цепям, выявляющая моноклональный IgG и каппа цепь
Слайд 42
Иммунохимические варианты множественной миеломы
Вариант
Частота,%
G-миелома
55-65
А-миелома
20-25
D-миелома
2-5
Е-миелома
Точно не установлена
Болезнь легких цепей
( миелома Бенс-Джонса)
12-20
Диклоновые миеломы
1-4
М-миелома
0,5
Слайд 43
Стадии множественной миеломы по Durie/Salmon.
Стадия
Критерии
1
А,В
Уровень Hb >100 г/л;
Нормальный
уровень кальция сыворотки;
На РГ нормальная костная структура или одиночный
очаг поражения;Низкий уровень М-протеина:
IgG<50 г/л, IgА<30 г/л;
Белок Бенс-Джонса при электрофорезе мочи <4г/сутки
(< 5 остеолитических очагов, легкий остеопороз)
2 А,В
Показатели выше, чем в 1 стадии, но ни один из них не достигает значений, характерных для 3 стадии
3
А,В
(В - креатинин > 2 мг/дл)
Уровень Hb<85 г/л;
Уровень кальция сыворотки превышает нормальные значения;
Множественные поражения костей (≥3 литических очагов);
Высокий уровень М-протеина:
IgG>70 г/л;
IgА>50 г/л;
Белок Бенс-Джонса при электрофорезе мочи >12 г в сутки
(>20 остеолитических очагов, выраженный остеопороз)
Слайд 45
Durie/Salmon PLUS система стадирования множественной миеломы
Классификация
ЯМР
и/или ПЭТ c 18-фтордеоксиглюкозой
Моноклональные гаммапатии неопределенного значения
Отсутствуют
очаги поражения Стадия IА (тлеющая или индолентная миелома)
Плазмацитома и/или ограниченный очаг
Множественная миелома
Стадии IБ, IIA/Б, IIIA/Б.
Стадия IБ
< 5 локальных очагов, диффузная форма легкой степени тяжести
Стадия II А/Б
5-20 локальных очагов, диффузная форма средней степени тяжести
Стадия IIIA/Б
>20 локальных очагов, диффузная форма тяжелой степени
А – креатинин сыворотки <2 мг/дл, отсутствие внекостномозговых очагов;
Б - креатинин сыворотки > 2 мг/дл, наличие внекостномозговых очагов;
Слайд 46
Стадии ММ по SWOG системе (2003 г)
Стадия
I β2-микроглобулин < 2,5 мг/дл
Стадия II β2-микроглобулин ≥ 2,5
< 5,5 мг/длСтадия III β2-микроглобулин ≥ 5,5 мг/дл
альбумин сыворотки ≥ 3 г/дл
Стадия IV β2-микроглобулин ≥ 5,5 мг/дл
альбумин сыворотки < 3 г/дл
Слайд 47
Прогностические факторы при множественной миеломе
Возраст
Соматический статус
Β2-микроглобулин
Альбумин сыворотки
Креатинин сыворотки
Лактатдегидрогеназа
СРБ
Уровень
гемоглобина в крови
Количество тромбоцитов
Пролиферативный индекс
Наличие плазмобластов и циркулирующих плазмоцитов
делеции
13, 17p, транслокации 4;14, 14;16Наличие экстрамедуллярных очагов (МРТ,РЭТ)
Слайд 48
Международный прогностический индекс при ММ
IPI группа 1 β2-микроглобулин
< 3,5 мг/дл
альбумин сыворотки > 3,5 г/дл
IPI группа 2
β2-микроглобулин < 3,5 мг/длальбумин сыворотки < 3,5 г/дл
или β2-микроглобулин 3,5 - 5,5 мг/дл
IPI группа 3 β2-микроглобулин > 5,5 мг/дл
Слайд 49
Группы риска при множественной миеломе (Клиника Мейо,США 2008)
Стандартный
риск (75%)
Высокий риск (25%)
FISH транслокация 11;14
FISH транслокация 6;14
гипердиплоидия
Все другие
FISH и цитогенетические нарушенияFISH делеция 17p
FISH транслокация 4;14
FISH транслокация 14;16
Делеция 13q
Гиподиплоидия
пролиферативный
индекс плазматических клеток ≥ 3%
Слайд 50
Индукционная терапия при множественной миеломе
Возраст < 65 лет
ВАД
(винкристин, адриамицин, дексаметазон)
ЦВАД( циклофосфамид, винкристин, адриамицин, дексаметазон)
ГиперЦВАД
VD(велкейд, дексаметазон)
PAD (велкейд,
адриамицин, дексаметазон)Возраст > 65 лет
МР (Мелфалан 8-10 мг р.о. 1-7 день, преднизолон 40-60 мг/м2 1-7 день)
МВП (мелфалан 8 мг 1-7 день,
Преднизолон 60 мг/м2 1-7 день,
Велкейд 1,3 мг/м2 день 1,4,8,11)
Слайд 51
Программы ХТ больных ММ
VAD
винкристина 0,4 мг/24 часа в/в,
1-4 дни
доксорубицина 9 мг/м2/24 часа в/в 1-4 дни
дексаметазон
40 мг per os в 1-4, 9-12, 17 – 21 дниHyperCVAD
циклофосфамид 300 мг/м2 внутривенно каждые 12 ч 1-3 дни
адриамицин 25 мг/м2/24 часа в/в 1-2 дни,
винкристин 1 мг/24 часа 1-2 дни и 2 мг в/в 11-й день.
дексаметазон 40 мг per os в 1-4 и 11-14-й дни
каждые 28 дней
Слайд 52
Лечение осложнений миеломы
Осложнение
Терапевтические подходы
Поражение костей
Бифосфонаты (бонефос, аредиа, зомета)
Контроль
за болью вплоть до наркотических аналгетиков, отказ от НПВП
Локальное
облучение для лечения плазмоцитом и очагов деструкции с рефрактерным болевым синдромом и компрессией корешковВертебропластика и кифопластика при определенных повреждениях позвонков для уменьшения боли и улучшения качества жизни
Слайд 53
Анемия
при симптомах анемии эритропоэтин во время химиотерапии или
гемотрансфузии
Инфекции
Назначение антибиотиков широкого спектра действия при терапии кортикостероидами
Внутривенный иммуноглобулин
для рецидивирующих серьезных инфекций , ассоциированных с гипогаммаглобулинемиейРассмотрение профилактики Pneumocystis carinii, когда проводится пролонгированная терапия ГКС, отмена триметоприма-сульфометоксазола при назначении талидомида
Гипер-
кальциемия
Внутривенно жидкость и кортикостероиды
Бифосфонаты
Слайд 54
Почечная недостаточ-ность
Коррекция обратимых причин, таких как дегидратация, гиперкальциемия,
гиперурикемии
Химиотерапия для быстрого контроля за заболеванием, бортезомиб
Щелочной диурез при
ОПН, обусловленной мочекислой нефропатией, избегать ощелачивания при у пациентов с гиперкальциемиейплазмообмен при острой почечной недостаточности
Синдром гипервяз-
кости
Плазмаферез при уровне белка более 110 г/л
Тромбо-филия
Профилактическое применение прямых или непрямых антикоагулянтов и дезагрегантов при использовании больших доз дексаметазона, талидомида и ревлимида
Слайд 55
Трансплантация стволовых клеток
По сравнению с со стандартными методами
лечения общая и безрецидивная выживаемость выше на 10-20 месяцев
Кондиционирование
мелфаланом в дозе100-140- 200 мг/ м2Двойная трансплантация через 3-6 мес
Аллогенная трансплантация
Слайд 56
Общая выживаемость больных множественной миеломой
Анализ выживаемости 2981 больного
ММ в клиниках Mayo (США) за 1971-2006гг
Медиана общей выживаемости
до 2000 года – 29,9 месяцев
после 2000 года 44,8 месяцев
Kumar S.K. et al. Blood 2008; 111: 2516.
Слайд 57 Факторы влияющие на эффективность лечения больных множественной миеломой
Более широкое использование высокодозной химиотерапии (мелфалан 200 ) c
ТПСК. Тандемная ТПСК.Внедрение в схемы лечения новых препаратов (талидамид, бортезомиб, ревлимид)
Учет основных факторов риска при выборе тактики лечения. Формирование групп риска (International Staging System –ISS, mSMART classification- Mayo Stratification of Myeloma and Risk Adapted Therapy)
Attal M. et al. Hematology 2007: 311-316.
Kumar S.K. et al. Blood 2008; 111(5): 2516-2520.
Greipp P.R. et al. J.Clin.Oncol. 2005;23: 3412-3420.
Dispenzieri A. et al Mayo Clin Proc.2007; 82: 323-341.
Слайд 58
Макроглобулинемия Вальденстрёма –
злокачественное лимфопролиферативное заболевание с продукцией моноклонального
IgМ и наличием в костном мозге полиморфных B-лимфоцитов на
разных стадиях созревания.По классификации ВОЗ (1997) – Лимфоплазмацитоидная лимфома
Слайд 59
Макроглобулинемия Вальденстрема
Впервые описана в 1944 г. Jan Waldenstrom
Хроническое
лимфопролиферативное заболевание В-клеточной природы, морфологически представленное лимфоцитами, плазмацитами и
характеризующееся продукцией моноклонового IgМВстречается в 7-10 раз реже ММ
Представляет около 2% всех гемобластозов
Средний возраст 65 лет ( от 32 до 92 лет)
Мужчины составляют 70%
Слайд 60
Этиология и предрасполагающие факторы
-предшествующая IgM-MGUS;
-генетическая предрасположенность;
-хроническая антигенная стимуляция(инфекции,аутоиммунные
процессы и т.д.);
-возможная связь с вирусом гепатита С;
Слайд 61
Патогенетические механизмы развития Макроглобулинемии Вальденстрема
Геномные нарушения - BLIMP
1 и BLyS
BLIMP 1 (B-Lymphocyte Inhibitor of Maturation and
Proliferation) - регулирует переход зрелой В-клетки в стадию Плазматической клетки. Нарушения в этом гене приводят к В-клеточным злокачественным новообразованиям;BLyS (B-Lymphocyte Stimulator). Относится к семейству TNF; Ингибирует апоптоз злокачественных B-клеток, регулирует секрецию IgM нормальными В-клетками ; у больных Макроглобулинемией Вальденстрема наблюдается повышенная экспрессия BLyS в лимфоплазмацитарных клетках
Blood,April 2006, vol 107,
Elsawa,Novak,Kyle)
Слайд 62
Макроглобулинемия Вальденстрема.
Характеризуется наличием моноклонального иммуноглобулина М (PIgM),
высокой вязкостью сыворотки крови и геморрагическим синдромом без тромбоцитопении.
МВ хронический лейкоз В-клеточной природы, морфологически представленный лимфоцитами, плазмоцитами и всеми переходными формами клеток и характеризующийся продукцией PIgM.В отличие от ММ часто встречается фиброз стромы костного мозга, нередко значительно выраженный.
Иммунофенотип – экспрессируют РIgM как на своей поверхности sIgM, так и внутри цитоплазмы сIgM, а также CD19, CD20, CD22, CD79a, CD10 и др.
В отличии от нормальных пентамерных молекул секретируются моно- , ди-, тетрамеры IgM в разных соотношениях
Из кариологических изменений наиболее часто встречаются изменения хромосом 10,11,12,20, более редка – t (8;14), t (14;18) в результате чего происходит активация c-myc или bcl-2-онкогенов
При использовании FISH метода выявляется делеция длинного плеча 6 хромосомы(21-55%) , трисомия 4 хромосомы (18%), трисомия 5 хромосомы (8%) и моносомия 8 (8 %).
Слайд 63
Диагностические критерии
-Моноклональный IgM сыворотки крови ;
-лимфоплазмоцитарная инфильтрация костного
мозга(наличие полиморфных В-клеток на разных стадиях созревания: малые лимфоциты,
лимфоплазмацитоидные клетки, плазматические клетки)-интертрабекулярная инфильтрация костного мозга;
-иммунофенотипирование: существует вариабельность в иммунофенотипе, но в большинстве случаев выявляются: CD 19+, CD 20+ , CD 22+ ; CD 5- , CD 23+/-.
Слайд 64
Прогностические факторы
возраст > 65 лет;
β2-микроглобулин >3 мг/л;
моноклональные IgM>
70 г/л;
гемоглобин < 115 г/л;
тромбоциты < 100*10^9;
низкий риск: 1
фактор, исключая возраст;высокий риск: >2 факторов;
промежуточный риск: 2 фактора, либо старше 65 лет.
Медиана выживаемости – 5-10 лет.
Слайд 65
Клиническая манифестация макроглобулинемии Вальденстрема
Симптомы
Признаки
Слабость, усталость
Симптомы гипервязкости
Ночная потливость
Потеря веса
Периферическая
нейропатия
Гепатомегалия - 20%
Спленомегалия -15%
Лимфаденопатия -15%
Пурпура
Уртикарные поражения кожи, макулопапулезные поражения,
артропатииПротеинурия (легкие цепи)
анемия
Инфекции
Проявления криоглобулинемии (васкулит)
Слайд 66
Признаки синдрома гипервязкости
Кровотечение из носа и десен, реже
– желудочно-кишечные и послеоперационные)
Пурпура
Нарушения зрения (размытые границы или потеря
зрения)Ретинопатия:
ретинальные кровоизлияния или экссудация
Сосудистая дилятация и сегментация
Отек соска зрительного нерва
Тромбоз вены сетчатки
Отек соска зрительного нерва
Головная боль, головокружение
Потеря слуха
Атаксия, парестезии
Сомноленция, потеря сознания, кома
Диплопия, геморрагический инсульт
Сердечная недостаточность
Слайд 67
Критерии начала терапии
-лихорадка, ночная потливость, слабость, снижение массы
тела ( на 10 % и более );
-прогрессирующая спленомегалия
или лимфаденопатия;-Hb <= 100 г/л;
-число тромбоцитов < 100*10 ^9/л;
-выраженные проявления синдрома гипервязкости;
-периферическая нейропатия;
Слайд 68
Лечение макроглобулинемии Вальденстрема
Плазмаферез – с возмещением альбумином и
растворами , особенно для пожилых пациентов
Алкилирующие агенты: хлорбутин (0,3
мг/кг дн 7 дней каждые 6 нед), мелфалан, циклофосфан в сочетании или без ГКС ( 40мг/м2), протокол М2, CHOPИФ-а – 1-3 MU 3 раза в нед.
Аналоги нуклеозидов: флюдарабин ( 25 мг/м2 в/в дни 1-4 каждые 4 нед), кладрибин (2-хлородещксиаденозин) 0,12 мг/кг дн 2х часовой в/в инфузией дни1-5
Высокодозная химиотерапия с поддержанием ПСКК
Сплленэктомия
Ритуксимаб + флударабин, ритуксимаб + кладрибин
R-CHOP
бортезомиб
Слайд 69
Болезни тяжелых цепей
В-клеточные лимфатические опухоли с крайне разнообразными
морфологией и клиническими проявлениями. Их характерной особенностью являются секреция
фрагментов тяжелых цепей (Н) различных изотипов иммуноглобулинов (Ig)Слайд 70 В соответствии с классом Н-цепей, синтезируемых опухолевыми клетками
выделяют 4 варианта болезни тяжелых цепей: ү, α, μ,
δ.История изучения заболевания начата в 1963 году после описания случая БТЦ ү
E. C. Franklin.
Сейчас описано около 400 случаев БТЦ.
Средний возраст – 60 лет (от 15 до 80 лет)
Слайд 71 Морфологические методы исследования в отличие от других лимфопролиферативных
заболеваний не позволяют поставить диагноз из-за чрезвычайной вариабельности картины.
Как
правило имеет место лимфоцито-плазматическая инфильтрация лимфоузлов, костного мозга или внекостных очагов.Диагноз устанавливается на основании иммунохимического анализа белков сыворотки и мочи.
Слайд 72 Клиническая картина вариабельна и определяется распространенностью процесса и
поражением тех или иных органов.
Слайд 73
Заболевание
БТЦ ү
БТЦ α
БТЦ μ
Возраст
Средний возраст 60 лет,
могут болеть дети, чаще мужчины
Чаще до 40 лет.
В
85% случаев в средиземноморье После 50 лет лет
Симптомы
Лихорадка, недомогание, слабость, интеркуррентные инфекции из-за синдрома недостаточности антител, ночные поты, потеря веса,
Увеличение лимфоузлов, селезенки, печени, поражение нелимфатических органов (кожи, щитовидной железы, слюнных желез)
Аутоимунные заболевания (25%)
IgA
2 варианта:
Абдоминальный и легочный
Хроническакя диаррея, мальабсорбция, потеря веса, электролитные нарушения
гепато-спленомегалия, лимфоаденопатия,
Клинические проявления как при хроническом лимфолейкозе, но может быть
остеодеструктив-ный синдром и остеопороз