Слайд 2
Фармакология (от греч. pharmacon – лекарство, яд; и
logos – учение) – это наука о взаимодействии лекарственных
средств биологической и небиологической природы с организмом человека или животного.
Задачи фармакологии:
1. Создание и обоснование рационального применения новых лекарственных средств. 2. Изучение новых свойств уже известных лекарственных препаратов.
Слайд 3
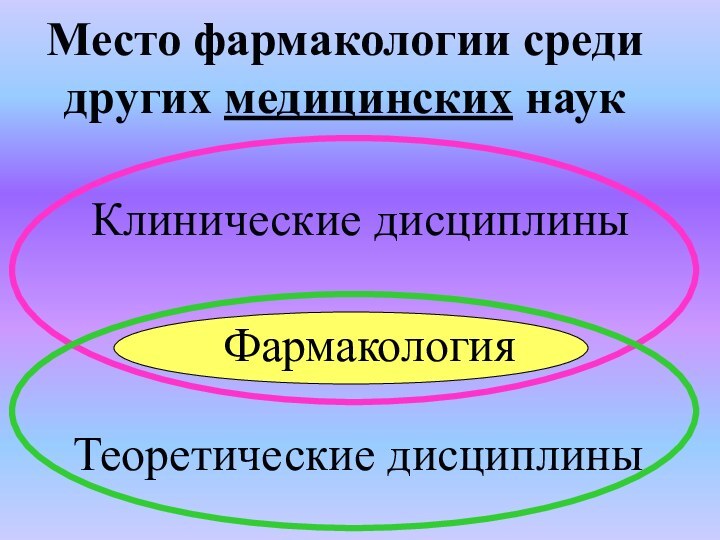
Место фармакологии среди других медицинских наук
Теоретические дисциплины
Клинические дисциплины
Фармакология
Слайд 5
Лекарственные средства по технологии приготовления подразделяются
на 3
группы:
натуральные лекарственные средства (настойки, отвары, вытяжки и экстракты растений,
адаптогены типа женьшеня, элеутерококка, а также пенициллин, ферментативные препараты – панзинорм, фестал, мезим и др);
полусинтетические препараты, при их изготовлении природное вещество слегка видоизменяется (почти все антибиотики, гормональные препараты первого поколения)
синтетические лекарства, изготовленные химическим путем (анальгетики, противовирусные препараты, противозачаточные средства, кардиологические и многие другие группы препаратов).
Слайд 9
1. Теоретическая
2. Экспериментальная
3. Клиническая
4. Фармакоэпидемиология
ФАРМАКОЛОГИЯ
Слайд 10
1. Теоретическая
2. Экспериментальная
ФАРМАКОЛОГИЯ
ФУНДАМЕНТАЛЬНАЯ
(изучают на 3 курсе)
+
Слайд 11
1. Общая
2. Частная
ФУНДАМЕНТАЛЬНАЯ ФАРМАКОЛОГИЯ
+
Слайд 12
Фармакодинамика
Фармакокинетика
3. Фармакогенетика
4. Хронофармакология
ОБЩАЯ ФАРМАКОЛОГИЯ
Слайд 13
раздел общей фармакологии, изучающий совокупность эффектов лекарственных
средств и механизмы их действия.
ФАРМАКОДИНАМИКА
Слайд 14
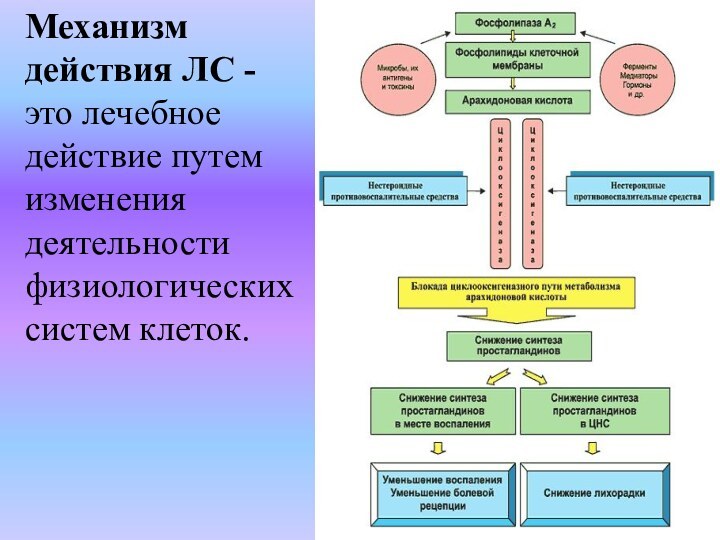
Механизм действия ЛС -
это лечебное действие путем изменения
деятельности физиологических систем клеток.
Слайд 15
«МИШЕНИ»
ЛЕКАРСТВЕННЫХ СРЕДСТВ
1. Биомембраны и ионные каналы
2. Рецепторы
(вне-, и внутри клетки)
3. Ферментные системы
4. Внутриклеточные метаболиты
5. Межклеточные
вещества
6. Возбудители инфекционных и паразитарных заболеваний
7. Токсины и яды
Слайд 16
ПУТИ ДЕЙСТВИЯ ЛВ
*Путем взаимодействия препарата с рецептором (ЛС
+ R).
*Путем действия ЛС на активность ферментов (ЛС +
фермент).
*Путем действия ЛС на биомембраны (ЛС + биомембрана).
*Путем взаимодействия одних ЛС с другими ЛС либо с эндогенными веществами.
Слайд 17
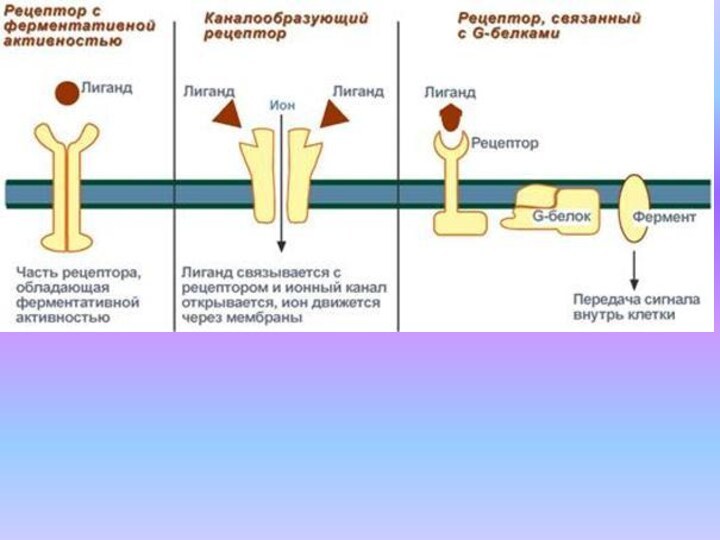
Действие на специфические рецепторы
Рецепторы - макромолекулярные структуры (белок
или гликопротеид), избирательно чувствительные к определенным химическим соединениям.
Слайд 19
Агонист – ЛС, которое при взаимодействии с рецепторами
вызывает фармакологический эффект.
Антагонист – ЛС, которое уменьшает или полностью
устраняет действие другого ЛС.
Антидоты – ЛС, которые устраняют действие других ЛС, вызывающих отравление.
Слайд 20
Антагонизм бывает двух
видов:
- конкурентный (прямой);
- неконкурентный (непрямой).
Конкурентный антагонизм осуществляется путем конкуренции различных ЛС за места связывания на одном и том же рецепторе, что приводит к уменьшению эффектов одного ЛС другим.
Неконкурентный антагонизм связан с различными рецепторами.
Слайд 21
Синергизм – взаимное усиление фармакологического эффекта одного ЛС
другим.
Суммация – общий эффект двух и более одновременно применяемых
ЛС, который равен арифметической сумме эффектов каждого из этих ЛС.
Потенцирование – это когда общий эффект комбинируемых препаратов больше, чем арифметическая сумма их фармакологических эффектов.
Слайд 22
Известно более 70 подтипов 20 известных типов рецепторов
Слайд 23
1.Адренорецепторы – 9 подтипов (альфа-1А,В,С; альфа-2А,В,С; бета-1,2,3)
2.Холинорецепторы –
6 подтипов (М-1,2,3,4; Н-мышечного и нейронального типа)
3.Опиатные рецепторы –
3 подтипа (мю, дельта, каппа)
4.Аденозиновые рецепторы – 4 подтипа (А1, А2а, А2в, А3)
5.Пуриновые рецепторы – 5 подтипов (Р2х, Р2y, Р2z, Р2т, Р2u)
6.Ангиотензиновые рецепторы – 2 подтипа (АТ1, АТ2)
7.Брадикининовые рецепторы – 2 подтипа (В1, В2)
8.ГАМК-рецепторы – 3 подтипа (GABAa, GABAb, GABAc)
9.Гистаминовые рецепторы – 3 подтипа (Н1,2,3)
10.Дофаминовые рецепторы – 5 подтипов (D1,2,3,4,5)
Слайд 24
11.Лейкотриеновые рецепторы – 3 подтипа (LTB4, LTC4, LTD4)
12.Простаноидные
рецепторы – 7 подтипов (DP, FP, IP, TP, EP1,
EP2, EP3)
13.Рецепторы возбуждающих аминокислот – 3 подтипа (NMDA, AMPA, каинатные)
14.Рецепторы нейропептида Y – 2 подтипа (Y1, Y2)
15.Рецепторы предсердного натрийуретического пептида – 2 подтипа (ANPA, ANPB)
16.Серотониновые рецепторы – 7 подтипов (5-HT1(a-f), 5-HT2 (a-c), 5-HT3, 5-HT4, 5-HT5(a-b), 5-HT6, 5-HT7)
17.Холецистокининовые рецепторы – 2 подтипа (CCКа, ССКв)
18.Глициновые рецепторы – 1 подтип (?)
Слайд 26
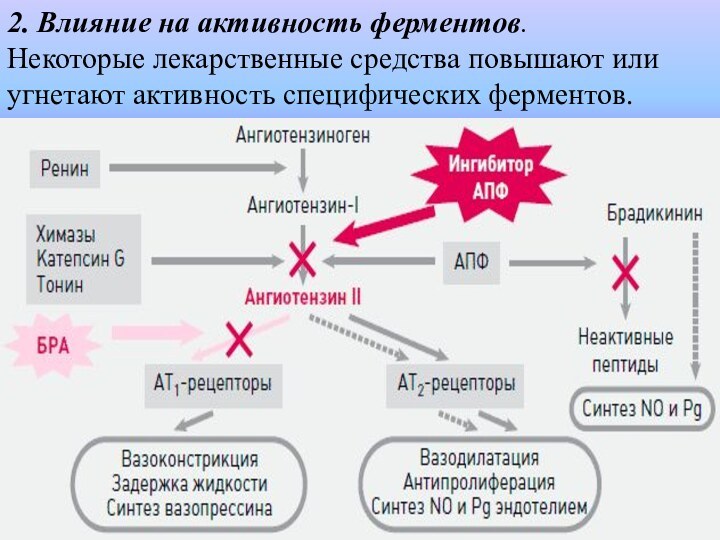
2. Влияние на активность ферментов.
Некоторые лекарственные средства
повышают или угнетают активность специфических ферментов.
Слайд 27
3. Взаимодействие с биомембранами.
Ряд ЛС способны изменять физико-химические
свойства клеточных и субклеточных мембран, изменяя таким образом трансмембранный
ток ионов (Са2+, Na +, К+).
Слайд 28
4. Взаимодействие ЛС с ЛС.
По принципу действия антидотов.
Слайд 29
ВИДЫ ДЕЙСТВИЯ ЛС
Основное – такое действие лекарства, на
которое рассчитывает врач при его применении.
Нежелательное:
-
побочное;
- аллергическое;
- токсическое.
Слайд 30
Побочное действие – это нежелательные реакции организма, обусловленные
фармакологическими свойствами ЛС, и наблюдается при применении его в
дозах, рекомендуемых для лечения.
Cнотворный эффект противоалергического средства димедрол часто используется в качестве основного.
Слайд 31
Аллергическое действие - это способность ЛС вызывать к
ним же повышенную чувствительность за счет активации реакции антиген-антитело.
Токсическое
действие – это реакции, которые возникают при поступлении в организм очень больших доз ЛС, что приводит к т.н. абсолютной передозировке.
Слайд 32
Относительная передозировка – это токсические реакции, которые могут
возникнуть при поступлении в организм даже среднетерапевтических доз, если
у больного нарушены функции метаболизирующих и экскретирующих органов.
Тератогенное действие – это нежелательное действие ЛС на плод, которое приводит к рождению ребенка с аномалиями или уродствами.
Эмбриотоксическое действие – это токсическое действие ЛС на плод до 12 недель беременности.
Слайд 33
Фетотоксическое действие – это токсическое действие на плод
после 12 недель беременности.
Мутагенное действие – способность ЛС нарушать
генетический аппарат зародышевых клеток, изменяя генотип потомства.
Канцерогенное действие – способность веществ вызывать образование злокачественных опухолей.
Слайд 34
Различают два вида действия
лекарств –
1.
Местное (возникает на месте его приложения)
2. Резорбтивное (действие всосав-шегося в кровь и поступившего в ткани лекарства).
Слайд 35
ВИДЫ ДОЗ
Пороговая – это минимальная доза ЛС, которая
вызывает какой-либо биологический эффект.
Среднетерапевтическая – доза препарата, которая вызывает
оптимальный лечебный эффект.
Высшая терапевтическая – доза, которая вызывает наибольший фармакологический эффект.
Широта терапевтического действия – это интервал между пороговой и высшей терапевтической дозами.
Слайд 36
Токсическая - доза, при которой возникают симптомы отравления.
Смертельная
– доза, которая вызывает смерть.
Разовая – pro dosi –
доза на один прием.
Курсовая – доза на курс лечения.
Ударная – доза, назначаемая в начале лечения, которая превышает среднетерапевтическую в 2-3 раза и назначается с целью быстрого достижения необходимой концентрации ЛС в крови или других биосредах.
Поддерживающая – доза, назначаемая после ударной, и она соответствует, как правило, среднетерапевтической.
Слайд 37
ДЕЙСТВИЕ ЛЕКАРСТВ ПРИ ИХ ПОВТОРНОМ ВВЕДЕНИИ В ОРГАНИЗМ
Кумуляция (cumulatio) – это
усиление действия ЛС при их повторном введении в организм.
Кумуляция бывает двух видов: материальная (физическая) и функциональная.
Слайд 38
Материальная кумуляция – реализуется, когда увеличение лечебного эффекта
происходит за счет накопления в организме ЛС.
Функциональная кумуляция –
это когда увеличение лечебного эффекта и появление симптомов передозировки происходит быстрее, чем накопление в организме самого препарата.
Привыкание – это снижение фармакологической активности препарата при его повторном введении в организм.
Перекрестное привыкание – это привыкание к препаратам, сходного (близкого) химического строения.
Слайд 39
ФАРМАКОКИНЕТИКА
это раздел общей фармакологии, который изучает
различные этапы прохождения лекарства в организме:
1.Всасывание (абсорбция),
2.
Биотранспорт (связывание с сывороточными белками),
3. Распределение по органам и тканям,
4. Биотрансформация (метаболизм),
5. Выведение (экскреция) ЛС из организма.
Слайд 40
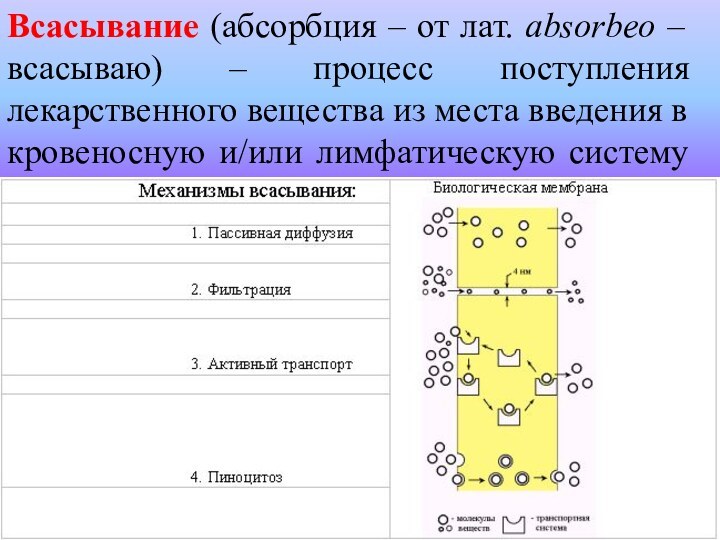
Всасывание (абсорбция – от лат. absorbeo – всасываю)
– процесс поступления лекарственного вещества из места введения в
кровеносную и/или лимфатическую систему через биологические мембраны.
Всасывание осуществляется по нескольким механизмам:
Слайд 41
Процесс всасывания ЛС характеризуется следующими фармакокинетическими параметрами:
Биодоступность (f)
– относительное количество препарата, которое поступает из места введения
в кровь (%).
Константа скорости всасывания (К01) – параметр, который характеризует скорость поступления ЛС из места введения в кровь (ч -1, мин -1).
Период полуабсорбции (t ½α) – время, необходимое для всасывания из места введения в кровь ½ введенной дозы (ч, мин).
Время достижения максимальной концентрации (tmax) – это время, за которое достигается максимальная концентрация ЛС в крови (ч, мин).
Слайд 42
1. Пути введения ЛC в организм
Пути введения разделяют
на:
энтеральные (через пищеварительный тракт)
парентеральные (минуя пищеварительный
тракт).
Путь введения определяет:
скорость наступления эффекта
его величину
продолжительность
характер фармакологического эффекта.
Слайд 43
I. Энтеральные пути введения
1. Через рот (внутрь, пероральный, per
os);
2. На слизистую полости рта (трансбуккальный) - лингвально, сублингвально, буккально,
дентально
3. Через прямую кишку (ректальный, per rectum).
Слайд 44
Приём внутрь зависим от многих факторов:
- приём
пищи;
- одновременный приём других препаратов, усиливающих перистальтику;
-
разрушение препарата в кишечнике;
- задержка препарата в пищеводе.
Лучше всего принимать препараты внутрь - в положении сидя и запивая 3-4 глотками воды.
Слайд 46
Пероральный путь введения недоступен:
- при нарушении акта глотания,
- при упорной рвоте,
- в бессознательном состоянии,
-
в раннем детском возрасте,
- при отказе больного принимать лекарства и т.д.
В этих случаях введение лекарственных средств и/или питательных растворов осуществляется по тонкому желудочному зонду через носовые ходы или через рот в желудок и/или в 12-перстную кишку.
Слайд 47
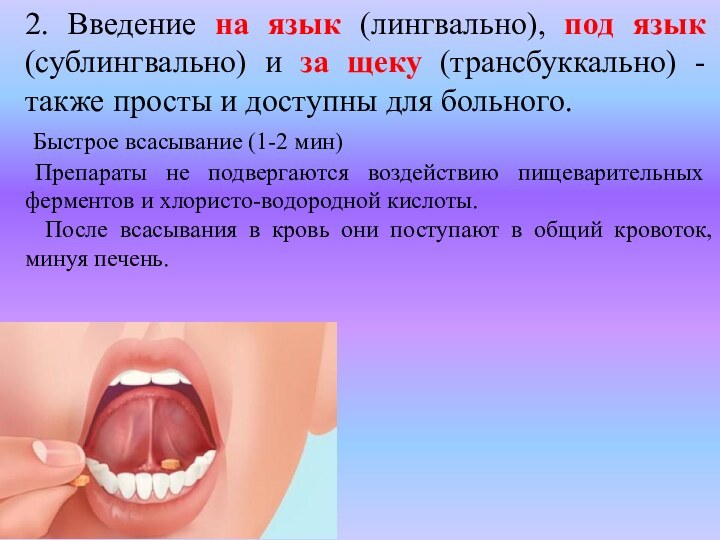
2. Введение на язык (лингвально), под язык (сублингвально)
и за щеку (трансбуккально) - также просты и доступны
для больного.
Быстрое всасывание (1-2 мин)
Препараты не подвергаются воздействию пищеварительных ферментов и хлористо-водородной кислоты.
После всасывания в кровь они поступают в общий кровоток, минуя печень.
Слайд 48
Ректально лекарственные вещества назначаются в форме суппозиториев или
в лекарственных клизмах, объемом до 50 мл.
Слайд 49
II. Парэнтеральные пути введения
К парентеральным путям введения относится:
Местно
- на кожу, слизистые и зубы (кроме ЖКТ)
Ингаляционно -
в дыхательные пути
Инъекционно -
В мягкие и твердые ткани.
В сосудистые системы (вены, артерии, ЛУ).
Внутрикожно и подкожно.
Около/над/под твердую и мягкую. оболочки мозга и оболочку нервов.
В естественные и патологические полости.
Электро-, и фонофорез
Слайд 50
Внутриартериальный путь (вводят рентгеноконтрастные и противоопухолевые препараты,
а также антибиотики).
Внутримышечный путь. Мышечная ткань имеет
хорошее кровоснабжение и поэтому всасывание лекарственных веществ в кровь происходит довольно быстро, что позволяет через 5-10 мин создать достаточно высокую концентрацию лекарственного вещества в крови. Внутримышечно вводят водные растворы (до 10 мл), а для обеспечения длительного эффекта – эмульсии и суспензии.
Слайд 51
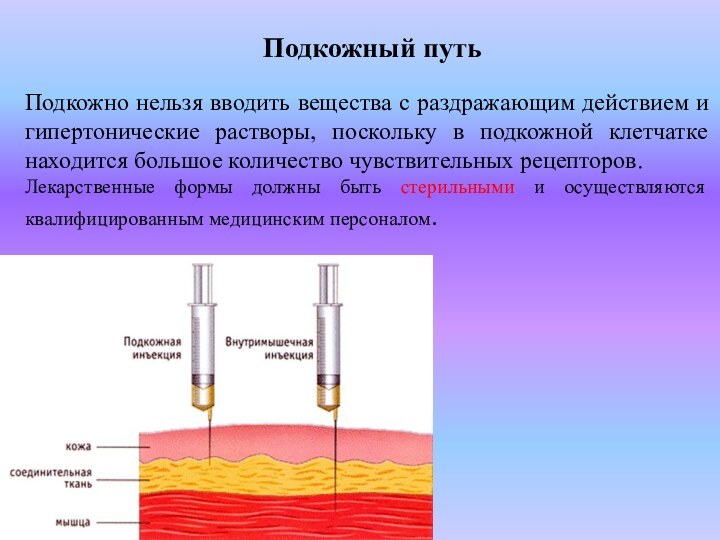
Подкожный путь
Подкожно нельзя вводить вещества с
раздражающим действием и гипертонические растворы, поскольку в подкожной клетчатке
находится большое количество чувствительных рецепторов.
Лекарственные формы должны быть стерильными и осуществляются квалифицированным медицинским персоналом.
Слайд 52
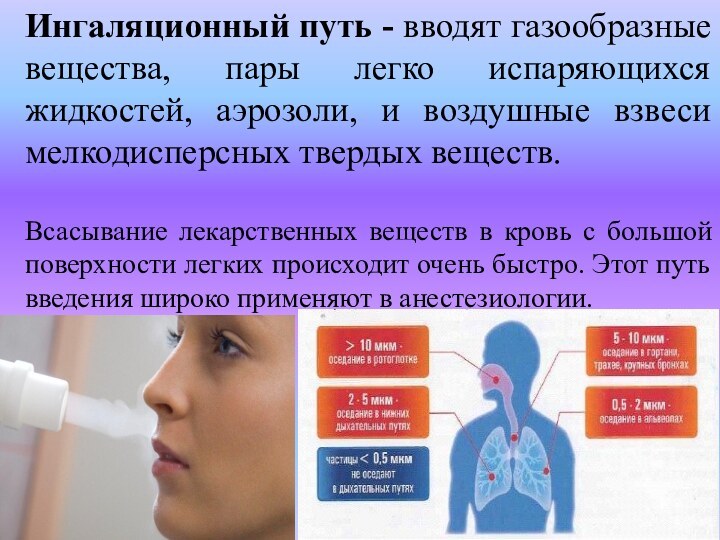
Ингаляционный путь - вводят газообразные вещества, пары легко
испаряющихся жидкостей, аэрозоли, и воздушные взвеси мелкодисперсных твердых веществ.
Всасывание лекарственных веществ в кровь с большой поверхности легких происходит очень быстро. Этот путь введения широко применяют в анестезиологии.
Слайд 53
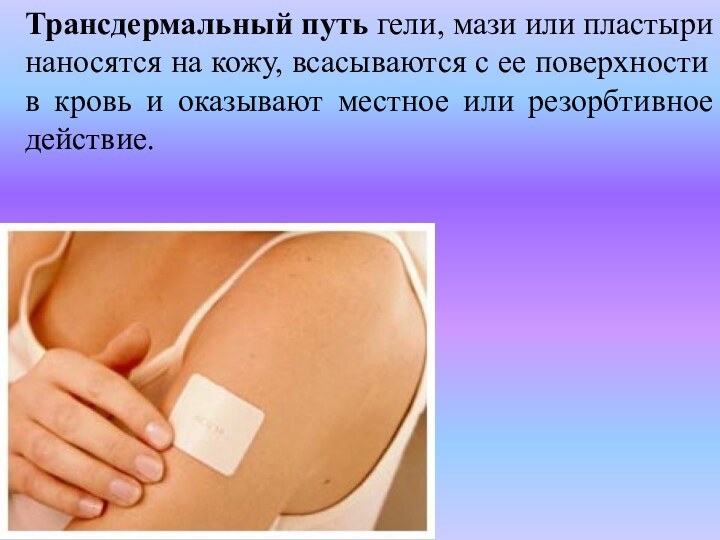
Трансдермальный путь гели, мази или пластыри наносятся на
кожу, всасываются с ее поверхности в кровь и оказывают
местное или резорбтивное действие.
Слайд 54
Введение лекарственных веществ под оболочки мозга используется
для специальных видов обезболивания (перидуральная спинномозговая анестезия) и введения
антибиотиков при инфекционных поражениях тканей и оболочек мозга.
Здесь особенно важно соблюдать стерильность и применять препараты, полностью лишенные раздражающих свойств.
Слайд 55
Лекарственные вещества можно вводить так же:
8. Внутрибрюшинно,
9.
Внутриплеврально,
10. В тело и в просвет органа (введение
стимуляторов мускулатуры матки в тело матки, кардиотонических средств в сердце),
11. На слизистую оболочку носа.
12. На слизистую оболочку глаза.
13. В полость суставной сумки (например, введение гидрокортизона при ревматоидном артрите).
Слайд 56
2. Биотранспорт – обратимые взаимодействия ЛВ с транспортными
белками плазмы крови и мембранами эритроцитов.
Подавляющее число лекарства (90%)
обратимо взаимодействуют с человеческим сывороточным альбумином. Кроме того, ЛС образуют обратимые комплексы с глобулинами, липопротеидами, гликопротеидами. Концентрация связанной с белком фракции соответствует свободной, т.е. не связанной с белком фракции: [Ссвяз] = [Ссвоб].
Слайд 57
Фармакологической активностью обладает лишь свободная (несвязанная с белком)
фракция, а связанная – является своего рода резервом препарата
в крови.
Связанная часть ЛС с транспортным белком определяет:
силу фармакологического действия лекарства;
продолжительность фармакотерапевтического действия.
Места связывания белка являются общими для многих веществ.
Слайд 58
Процесс обратимого взаимодействия лекарств с транспортными белками характеризуется
следующими фармакокинетическими параметрами:
Константа ассоциации (Касс) – характеризует степень сродства
препарата к белку сыворотки крови (моль-1).
Число мест связывание (N) – показатель активных центров белка, на которых фиксируется одна молекула препарата.
Слайд 59
После попадания в системный кровоток лекарственные вещества распределяются
в различных тканях организма.
3. Распределение лекарств в организме.
Как
правило, лекарства в организме распределяются по органам и тканям неравномерно с учетом их тропности (сродства).
На характер распределения лекарств в организме влияют следующие факторы:
* степень растворимости в липидах;
*интенсивность регионарного (местного) кровоснабжения;
*степень сродства к транспортным белкам;
*состояние биологических барьеров (гематоэнцефалического, плацентарного).
Слайд 60
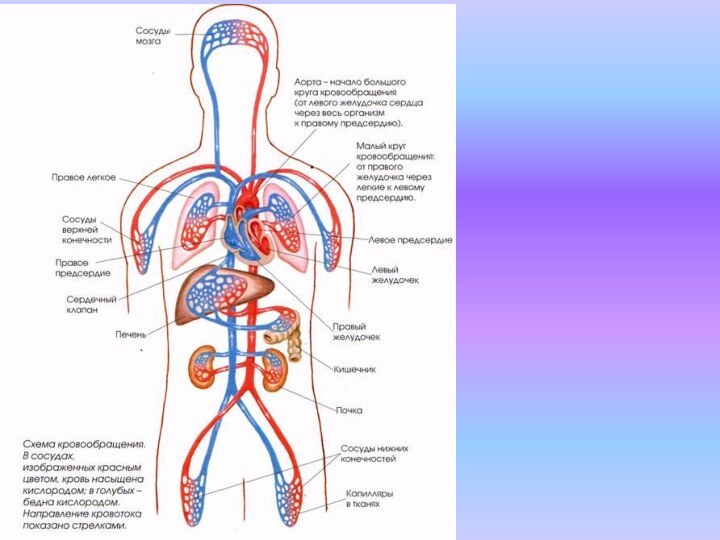
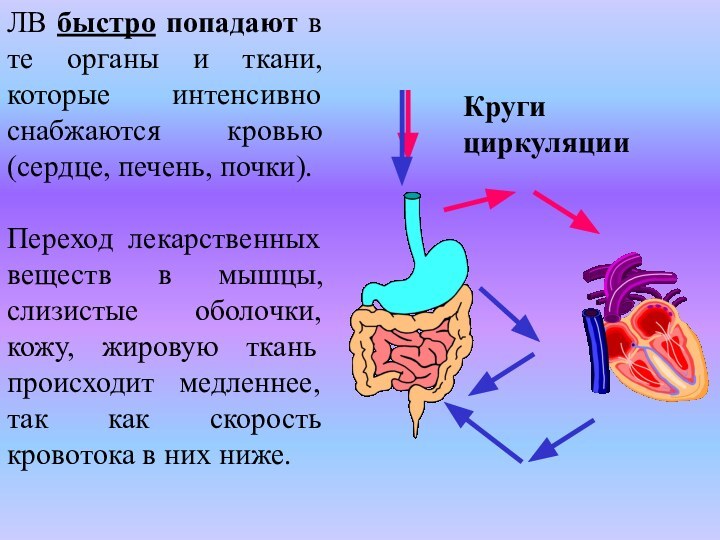
ЛВ быстро попадают в те органы и ткани,
которые интенсивно снабжаются кровью (сердце, печень, почки).
Переход лекарственных
веществ в мышцы, слизистые оболочки, кожу, жировую ткань происходит медленнее, так как скорость кровотока в них ниже.
Круги циркуляции
Слайд 61
Основными местами распределения ЛС в организме являются:
внеклеточная
жидкость;
внутриклеточная жидкость;
жировая ткань.
Фармакокинетический параметр, характеризующий этап распределения:
Объем распределения
(Vd) - степень захвата ЛС тканями из крови (л, мл).
Слайд 62
РАСПРЕДЕЛЕНИЕ ЛВ
В одних органах концентрация ЛВ может
быть высокой, в других - ничтожно малой.
Накопление ЛВ
в органах и тканях зависит от состава этих тканей. Основную роль в депонировании ЛВ принадлежит липидам, белкам, мукополисахаридам.
Липофильные ЛВ накапливаются НЕРАВНОМЕРНО - в мозге, жировой ткани и меньше в мышечной ткани. Так, при наркозе в головном мозге содержание наркозных средств значительно больше, чем в скелетных мышцах.
Водорастворимые ЛВ накапливаются РАВНОМЕРНО - в межклеточной жидкости, в органах выделения (почках).
Многие ЛВ имеют свойство избирательно накапливаться в местах специфического действия. Йод накапливается в щитовидной железе, сердечные гликозиды в сердечной мышце, женские половые гормоны в матке и влагалище.
Слайд 63
Биологические (гисто-гематические) барьеры - это стенки капилляров.
Они играют
существенную роль в распределении лекарственных веществ.
«забарьерные» ткани:
мозг, плацента, половые
железы, глаза, щитовидная железа и др.
Слайд 64
4. Биотрансформация (метаболизм).
Один из центральных этапов фармакокинетики и
основной путь детоксикации (обезвреживания) ЛС в организме.
В биотрансформации принимают
участие: печень, почки, легкие, кожа, плацента.
Биотрансформация осуществляется в 2 фазы.
Слайд 65
Реакции I фазы (биотрансформации) – это гидроксилирование,
окисление, восстановление, дезаминарование, дезалкилирование и т.д.
(ЛС становится более
гидрофильным). Это обеспечивает более легкую экскрецию метаболитов из организма с мочой.
Реакции I фазы осуществляются с помощью ферментов эндоплазматического ретикулума (микросомальные ферменты или ферменты монооксигеназной системы), основным из которых является цитохром Р - 450.
Слайд 66
В процессе реакций II фазы образуются коньюгаты или
парные соединения препарата с одним из эндогенных веществ (например,
с глюкуроновой кислотой, глутатионом, глицином серной кислоты). Образовавшиеся коньюгаты являются фармакологически неактивными веществами и легко выводятся из организма с одним из экскретов. Однако не вся введенная доза ЛС подвергается биотрансформации, часть ее выводится в неизмененном виде.
Слайд 67
5. Выведение (экскреция).
Является завершающим этапом фармакокинетики, в процессе
которого лекарство в виде метаболитов или в неизмененном виде
выводятся из организма с одним из экскретов. Чаще всего ЛС выводятся из организма с мочой, желчью, выдыхаемым воздухом, слюной, потом, грудным молоком. Наибольший удельный вес экскреции приходится на почки.
При этом реализуются следующие механизмы:
клубочковая фильтрация;
канальцевая секреция;
канальцевая реабсорбция.
Слайд 68
Основные фармакокинетические параметры:
Константа экскреции (Кех) – характеризует скорость
выделения лекарства из организма с каким-либо экскретом (ч-1, мин-1).
Константа
элиминации (Кel) – характеризует скорость исчезновения препарата из организма путем экскреции и биотрансформации (ч-1,мин-1).
Период полуэлиминации (t1/2) – это время исчезновения из организма лекарства путем биотрансформации и экскреции ½ введенной или поступившей и всосавшейся дозы (ч, мин.).