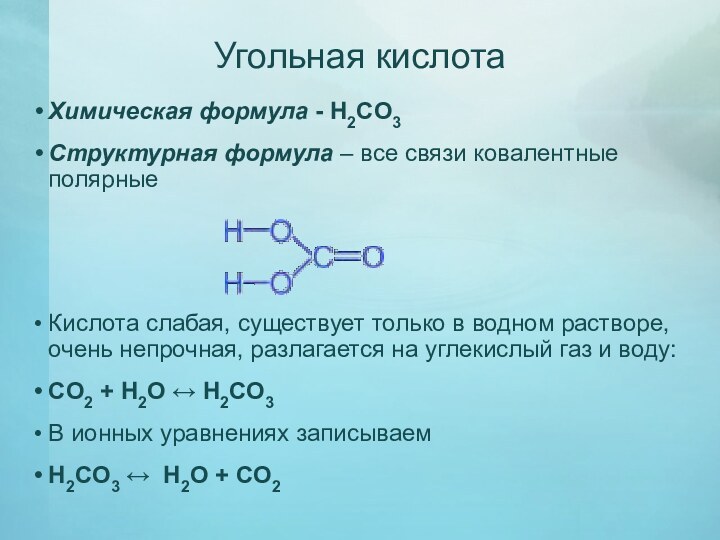
а CО2 - обязательный компонент атмосферы. Какой это оксид
по классификации? Что он образует с Н2О.Составить уравнения реакций взаимодействия углекислого газа с водой и дать физико-химическую характеристику этой реакции.
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть