Слайд 2
СИНДРОМ АЛЬПОРТА
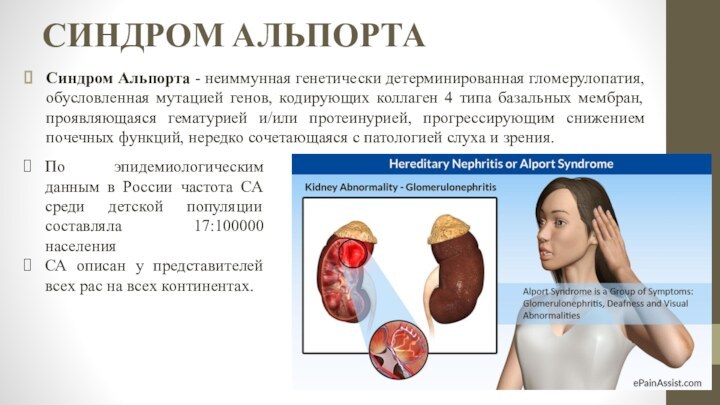
Синдром Альпорта - неиммунная генетически детерминированная гломерулопатия,
обусловленная мутацией генов, кодирующих коллаген 4 типа базальных мембран,
проявляющаяся гематурией и/или протеинурией, прогрессирующим снижением почечных функций, нередко сочетающаяся с патологией слуха и зрения.
По эпидемиологическим данным в России частота СА среди детской популяции составляла 17:100000 населения
СА описан у представителей всех рас на всех континентах.
Слайд 3
ЭТИОЛОГИЯ И ПАТОГЕНЕЗ
Синдром Альпорта наследуется по аутосомно-доминантному типу,

частично сцеплен с полом. Больные мужчины-гетерозиготы способны передавать дефектный
ген только дочерям, больные женщины - большей части дочерей и сыновей.
Генетическая основа болезни - мутация в гене а-5 цепи коллагена IV типа. Этот тип универсален для базальных мембран почки, кохлеарного аппарата, капсулы хрусталика, сетчатки и роговицы глаза, что доказано в исследованиях с использованием моноклональных антител против этой фракции коллагена.
При исследовании биоптата почек у больных с синдромом Альпорта по данным электронной микроскопии наблюдаются ультраструктурные изменения базальной мембраны клубочка: истончение, нарушение структуры и расщепление гломерулярных базальных мембран с изменением ее толщины и неравномерностью контуров.
На ранних стадиях наследственного нефрита дефект определяет истончение и ломкость гломерулярных базальных мембран.
При прогрессировании заболевания выявляется утолщение и выраженная деструкция базальных мембран клубочков.
Слайд 5
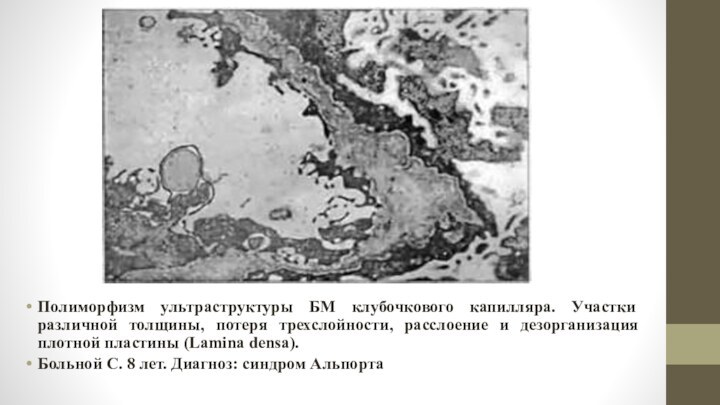
Полиморфизм ультраструктуры БМ клубочкового капилляра. Участки различной толщины,
потеря трехслойности, расслоение и дезорганизация плотной пластины (Lamina densa).
Больной С. 8 лет. Диагноз: синдром Альпорта
Слайд 6
I вариант - клинически проявляется нефритом с гематурией,
тугоухостью и поражением глаз.
Течение нефрита прогрессирующее с развитием
ХПН.
Тип наследования - доминантный, сцепленный с Х-хромосомой.
Морфологически выявляется нарушение структуры базальной мембраны, ее истончение и расщепление.
Выделяют три варианта наследственного нефрита:
II вариант- клинически проявляется нефритом с гематурией без тугоухости.
Течение нефрита прогрессирующее с развитием ХПН.
Тип наследования - доминантный, сцепленный с Х-хромосомой.
Морфологически выявляется истончение базальной мембраны капилляров клубочков (особенно laminadensa).
III вариант - доброкачественная семейная гематурия.
Течение благоприятное, хроническая почечная недостаточность не развивается.
Тип наследования - аутосомно-доминантный или аутосомно-рецессивный.
При аутосомно-рецессивном типе наследования у женщин отмечено более тяжелое течение заболевания.
Слайд 7
КЛИНИЧЕСКАЯ КАРТИНА
Клиника обнаруживается на первом или (чаще) 3-5-м
годах жизни ребенка.
Течение наследственного нефрита может характеризоваться признаками:
гломерулонефрита
гематурической формы,
реже он протекает с нефротическим синдромом
либо по пиелонефритическому типу
В начальной стадии болезни самочувствие ребенка страдает мало, характерной особенностью является упорство и стойкость мочевого синдрома:
гематурия различной степени выраженности, наблюдаемая в 100% случаев.
протеинурия в большинстве случаев не превышает 1 г/сут, в начале заболевания может быть непостоянной, по мере прогрессирования процесса протеинурия нарастает.
Слайд 8
В дальнейшем происходит нарушение парциальных функций почек, ухудшение
общего состояния больного появляются:
интоксикация,
мышечная слабость,
артериальная гипотония,
нарушение
слуха и нарушение зрения (в 20% случаев ).
Наиболее часто выявляются аномалии со стороны хрусталика:
сферофакия,
лентиконус передний, задний или смешанный,
разнообразные катаракты.
Снижение слуха при синдроме Альпорта может возникнуть в различные периоды детства, однако чаще всего тугоухость диагностируется в возрасте 6-10 лет.
Начинается снижение слуха у детей с высоких частот, достигая значительной степени при воздушном и костном проведении, переходя из звукопроводящей в звуковоспринимающую тугоухость.
Слайд 9
Диагностика
Для диагностики СА необходимо присутствие трех из
пяти признаков:
гематурия или летальный исход от ХПН в
семье;
гематурия и/или протеинурия в семье;
специфические изменения БМ клубочков у больного при электронной микроскопии (ЭМ) биоптата;
снижение слуха по данным аудиометрического исследования;
врожденная патология зрения.
Слайд 10
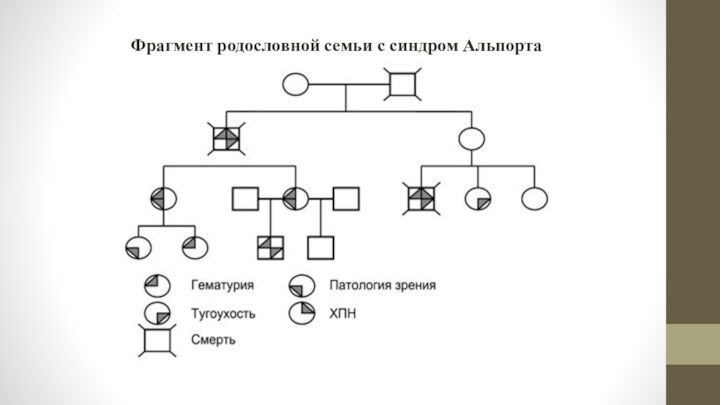
Фрагмент родословной семьи с синдром Альпорта
Слайд 11
Дифференциальная диагностика
С гематурической формой приобретенного гломерулонефрита.
Приобретенный гломерулонефрит имеет
чаще острое начало, период 2-3 нед после перенесенной инфекции,
экстраренальные признаки, в том числе гипертензию с первых дней (при наследственном нефрите, напротив, гипотония), снижение клубочковой фильтрации в начале заболевания, отсутствие нарушения парциальных канальцевых функций, тогда как при наследственном они присутствуют.
Приобретенный гломерулонефрит протекает с более выраженной гематурией и протеинурией, с увеличенной СОЭ.
Диагностическое значение имеют типичные изменения гломерулярной базальной мембраны, свойственные наследственному нефриту.
Слайд 12
Лечение
Антипротеинурическая терапия
Первая линия (иАПФ):
рамиприл в дозе 1-2
мг/м2 /сут,
эналаприл в дозировке вдвое выше (2-4 мг/м2/сут),
лизиноприл, фозиноприл, квинаприл в дозировке вчетверо выше (4-8 мг/м2/сут)
Второй линией являются блокаторы рецепторов ангиотензина (БРА):
лозартан в дозе 12,5 мг/м2/сут, удваивая дозу каждые 3 месяца до достижения максимальной дозы (при отсутствии побочных эффектов) 50 мг/м2/сут,
ирбисартан – тройная доза лозартана (37,5 мг/м 2 /24ч),
вальсартан – 1,5 доза лозартана (18,75 мг/м 2 /24ч) (НГ).
Показана госпитализация в стационар с целью контрольного обследования 1 раз в 6 месяцев, амбулаторное наблюдение.
Слайд 13
С наступлением хронической почечной недостаточности проводится комплекс мероприятий
по лечению артериальной гипертензии, анемии, электролитных и костно-минеральных нарушений,
диализ и трансплантация почки.
Лечение проводится под регулярным контролем уровня калия. Повышение его уровня может быть связано с действием иАПФ или БРА и требует снижение дозы препарата на 50%, а при персистенции гиперкалиемии – полная отмена терапии.
В терминальной стадии ХПН выполняют гемодиализ или трансплантацию почки.
Вторичная профилактика. В семьях с Х-сцепленной формой СА при известных мутациях возможна пренатальная диагностика, что крайне важно, если плод мужского пола.
Перспективы в терапии СА. Реальных перспектив разработки этиотропной терапии СА в настоящее время нет.
Слайд 14
Течение и исход заболевания
Течение и исход заболевания зависят
от пола больных.
У мальчиков рано (с 10-15 лет)
развиваются гипертензия и хроническая почечная недостаточность. Смерть наступает в возрасте 15-30 лет.
У девочек заболевание протекает чаще скрыто в виде гематурического синдрома. Иногда это сочетается с нарушением слуха.
Сопутствующие заболевания и переутомление могут быть причиной декомпенсации и прогрессирования болезни.
Слайд 15
Болезнь тонких базальных мембран
Доброкачественная семейная гематурия (болезнь тонких
базальных мембран) - наследственное заболевание, его основной признак - истончение базальной
мембраны клубочка.
В отличие от синдрома Альпорта, доброкачественная семейная гематурия протекает благоприятно и не приводит к развитию почечной недостаточности.
Этиология и патогенез заболевания изучены плохо.
Клиническая картина. Заболевание проявляется во взрослом возрасте. Основной симптом - рецидивирующие протеинурия и гематурия.
Патоморфология. Макроскопически почки не имеют характерных изменений. Изменений в клубочках обычно не определяют, в эпителии канальцев - вакуоли, содержащие белок и липиды. Иммуногистохимически иммуноглобулины и комплемент не обнаруживают. Гломерулярная базальная мембрана истончена, её трёхслойность сохранена.
Исходы и осложнения. Прогноз благоприятный, продолжительность жизни не уменьшена, почечная недостаточность не развивается.