- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Белки. Органические вещества клетки
Содержание
- 2. Белки – главный компонент клетки Содержатся во всех структурах клетки Составляют 10-20% от всей её массы
- 3. Химический состав белков Белки имеют очень большую
- 4. Аминокислота – органическое вещество, в состав
- 5. Все АК различаются радикалами. В белке
- 6. .
- 7. Функции белков Ферментативная Строительная
- 8. Белки-ферменты Ускорители биохимических реакций в клетке.(липаза, амилаза, пепсин)
- 9. Строительные белки Входят в состав биологических мембран
- 10. . Строительные белкиНапример, коллаген сухожилий, кератин волос.Составляют цитоскелет клетки.
- 11. Транспортные белки.Переносят питательные вещества из клетки, внутри
- 12. Сократительные белки.Используются организмом для движения.Например, актомиозин.
- 13. Регуляторные белки.Выполняют функцию управления деятельностью ферментов.Например, гормон инсулин, тирозин; гормон роста – гипофиз.
- 14. Пищевые белки.Используются
- 15. Защитные белкиЭто
- 16. .При расщеплении 1 грамма белков
- 17. Белки-рецепторы.Определяют способность клетки узнавать чужеродные антигены.Например, белок гликопротеин.
- 18. Растворимость белков в воде Нерастворимые белки -
- 19. Вторичная Структура белка..ПервичнаяТретичнаяЧетвертичная
- 20. Первичная структураПредставляет собой вытянутую
- 21. Вторичная структураПолипептидная цепь,
- 22. Третичная структураПредставляет собой свёрнутую
- 23. .
- 24. Денатурация белка.Пример: вареное яйцо
- 25. Обратимая денатурация.При устранении факторов, вызвавших денатурацию,
- 26. Обратимая денатурация пример Если к
- 27. Спасибо за внимание
- 28. Скачать презентацию
- 29. Похожие презентации
Белки – главный компонент клетки Содержатся во всех структурах клетки Составляют 10-20% от всей её массы

















Слайд 3
Химический состав белков
Белки имеют очень большую молекулярную
массу
Молекула белка построена по принципу полимера – сложное
вещество, молекула которого состоит из мономеров.Мономеры белков – аминокислоты.
Слайд 4
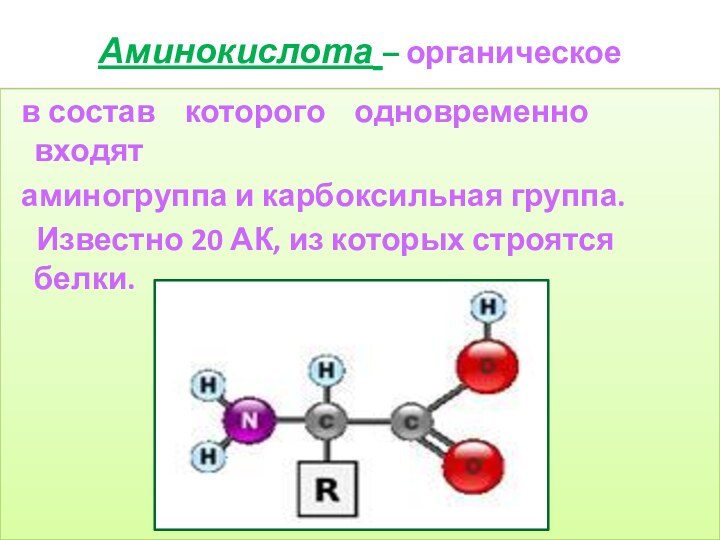
Аминокислота – органическое вещество,
в состав которого
одновременно входят
аминогруппа и карбоксильная группа.
Известно 20 АК, из которых строятся белки.Общая формула АК:
Слайд 5
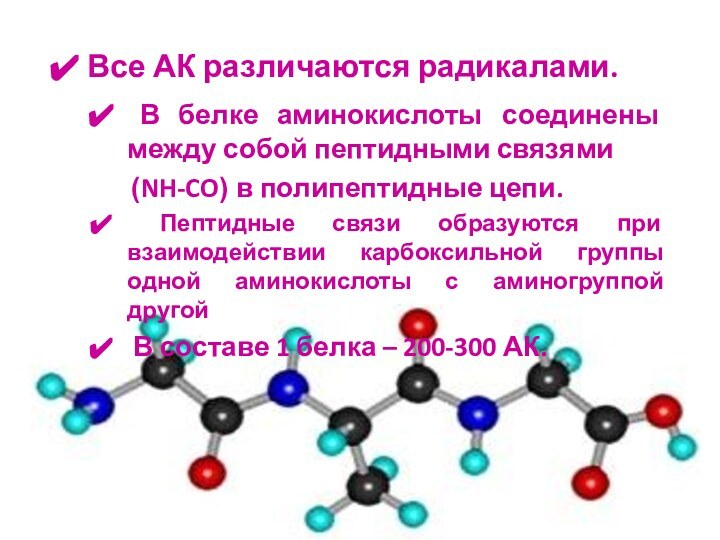
Все АК различаются радикалами.
В белке аминокислоты
соединены между собой пептидными связями
(NH-CO) в
полипептидные цепи.Пептидные связи образуются при взаимодействии карбоксильной группы одной аминокислоты с аминогруппой другой
В составе 1 белка – 200-300 АК.
Слайд 7
Функции белков
Ферментативная
Строительная
Транспортная
СократительнаяРегуляторная
Пищевая
Защитная
Энергетическая
Рецепторная
Слайд 10
.
Строительные белки
Например, коллаген сухожилий, кератин волос.
Составляют цитоскелет
клетки.
Слайд 11
Транспортные белки
.
Переносят питательные вещества из клетки, внутри клетки,
в клетку. Например, гемоглобин доставляет кислород к тканям, карбоксигемоглобин
-выносит углекислый газ.
Слайд 13
Регуляторные белки
.
Выполняют функцию управления деятельностью
ферментов.
Например, гормон инсулин, тирозин; гормон роста – гипофиз.
Слайд 14
Пищевые белки
.
Используются на
ранних этапах развития организма для роста.
Например, казеин молока, яичный
альбумин.
Слайд 15
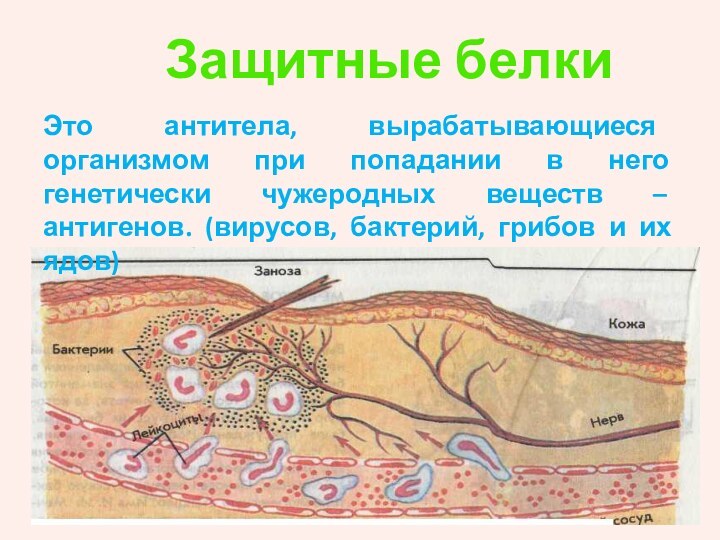
Защитные белки
Это антитела,
вырабатывающиеся организмом при попадании в него генетически чужеродных веществ
– антигенов. (вирусов, бактерий, грибов и их ядов)
Слайд 16
.
При расщеплении 1 грамма белков до
углекислого газа и воды выделяется 17,6 кДж энергии.
Энергетические белки
Слайд 17
Белки-рецепторы
.
Определяют способность клетки узнавать чужеродные
антигены.
Например, белок гликопротеин.
Слайд 18
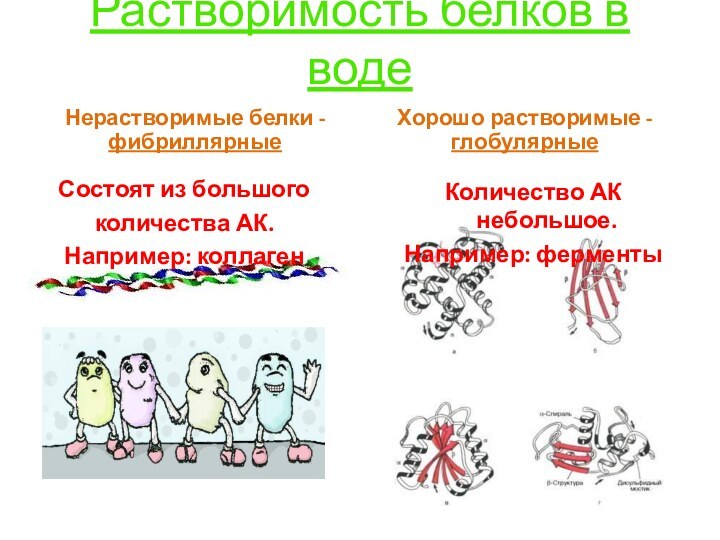
Растворимость белков в воде
Нерастворимые белки - фибриллярные
Состоят из
большого
количества АК.
Например: коллаген
Хорошо растворимые - глобулярные
Количество АК небольшое.
Например: ферменты
Слайд 20
Первичная структура
Представляет собой вытянутую нить;
определяется
3 факторами:
природой АК, входящих в состав белков
количеством
АКпоследовательностью АК.
Слайд 21
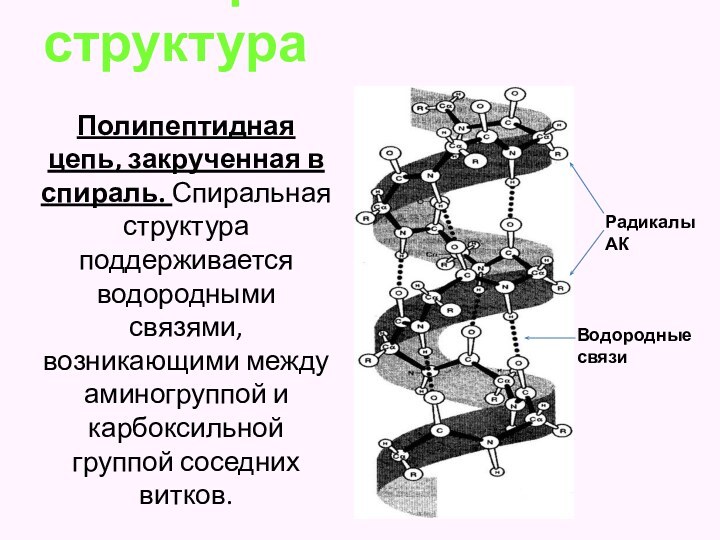
Вторичная структура
Полипептидная цепь, закрученная
в спираль. Спиральная структура поддерживается водородными связями, возникающими между
аминогруппой и карбоксильной группой соседних витков.Радикалы АК
Водородные связи
Слайд 22
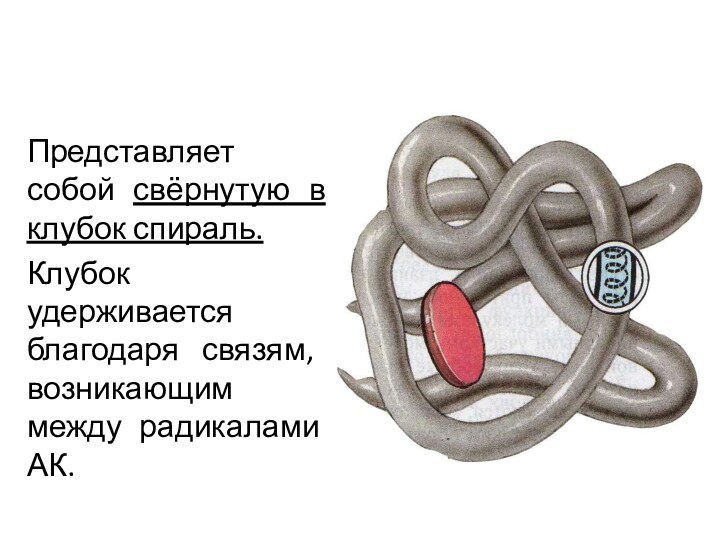
Третичная структура
Представляет собой свёрнутую в
клубок спираль.
Клубок удерживается благодаря связям, возникающим между радикалами
АК.
Слайд 23
.
Четвертичная структура
Несколько полипептидных цепей,
образующих
сложный белок, напоминающих клубок.Имеют лишь
некоторые белки.
Например, гемоглобин.
Слайд 24
Денатурация белка
.
Пример: вареное яйцо
.
Разрушение вторичной и третичной структур до первичной под влиянием высокой или низкой температур, сильных кислот и щелочей, этилового спирта и др. факторов.
Необратимая
Обратимая
Слайд 25
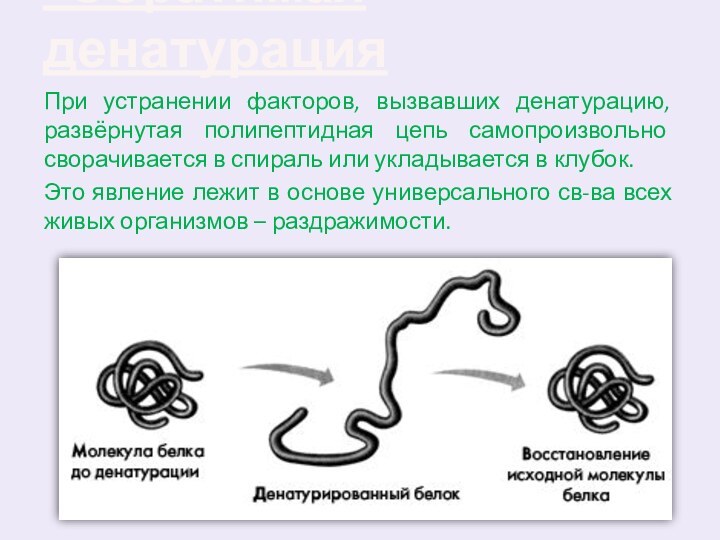
Обратимая денатурация
.
При устранении факторов, вызвавших денатурацию, развёрнутая
полипептидная цепь самопроизвольно сворачивается в спираль или укладывается в
клубок.Это явление лежит в основе универсального св-ва всех живых организмов – раздражимости.