- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Ферменты
Содержание
- 2. ФЕРМЕНТЫ – высокоэффективные биологические катализаторы, синтезируемые живыми
- 3. ЧРЕЗВЫЧАЙНО ВАЖНАЯ РОЛЬУчаствуют во всех химических процессахКлеткаОрганизмПроявляют свою каталитическую активность в водной среде
- 4. ФЕРМЕНТЫ – ПРОСТЫЕ БЕЛКИСОСТОЯТ ТОЛЬКО ИЗПОЛИПЕПТИДНЫХ ЦЕПЕЙГИДРОЛИЗУЮТСЯ ДО АМИНОКИСЛОТПЕПСИН, ТРИПСИН, УРЕАЗА
- 5. ФЕРМЕНТЫ – СЛОЖНЫЕ Б Е Л К
- 6. Ф Е Р М Е Н Т
- 7. Изоферменты фермент, существующий в виде нескольких изоформ
- 8. ОРГАНЫ И ТКАНИ ИМЕЮТ ХАРАКТЕРНЫЙДЛЯ НИХ НАБОР
- 9. С У Б С Т Р А
- 10. Каталитическая активностьСпособность фермента превращать в продуктопределенное количество
- 11. АКТИВАТОРЫ ФЕРМЕНТОВСоединения, которые приводятфермент в каталитическиактивное состояниеИоны двухвалентных металлов:Zn2+, Cа2+, Mg2+, Cu2+
- 12. ИНГИБИТОРЫ ФЕРМЕНТОВСоединения, которые снижают каталитическуюактивность ферментовИ н
- 13. ИНГИБИТОРЫ ФЕРМЕНТОВКОНКУРЕНТНЫЕНЕКОНКУРЕНТНЫЕСВЯЗЫВАЕТСЯ С АКТИВНЫМЦЕНТРОМ ФЕРМЕНТА↓ СКОРОСТЬ КАТАЛИЗА,
- 14. СПЕЦИФИЧНОСТЬ ФЕРМЕНТАДЕЙСТВИЕ КАЖДОГО ФЕРМЕНТАСТРОГО ОГРАНИЧЕНО ОДНИМ ТИПОМРЕАКЦИИ И ОДНИМ СУБСТРАТОМ(НЕБОЛЬШИМ ЧИСЛОМ СХОДНЫХХИМИЧЕСКИХ ВЕЩЕСТВ)
- 15. Международная единица активностиМЕ - КОЛИЧЕСТВО ФЕРМЕНТА, КОТОРОЕ
- 16. Классы ферментов
- 17. Ферменты участвуют во всех биологических процессахНарушение метаболизма,
- 18. Применение ферментов в медицинедиагностическое (энзимодиагностика) терапевтическое (энзимотерапия)
- 19. ЭнзимотерапияЗаместительная терапия - использование ферментов в случае
- 20. ЭнзимотерапияКак элемент комплексной терапии - применение ферментов
- 21. Применение ферментов в качестве специфических реактивовспецифические эндонуклеазы,
- 22. Значение энзимодиагностикиИзвестно около 20 тестов, основанных на
- 23. Энзимодиагностикапостановка диагноза заболевания (или синдрома) на основе
- 24. Ферменты сывороткиКлеточныепоступают в кровь из органов и
- 25. Причины повышения активности клеточных ферментов в кровинарушение
- 26. Факторы, определяющие концентрацию фермента в крови при
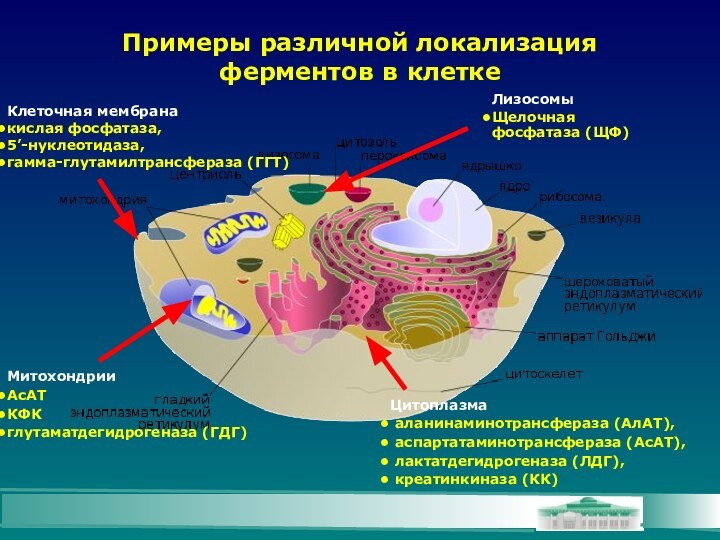
- 27. Примеры различной локализация ферментов в клеткеКлеточная мембранакислая
- 28. Причины понижения активности клеточных ферментов в крови
- 29. Механизмы удаления ферментов из кровиБольшинство ферментов катаболизируется
- 30. Основные правила дифференциальной диагностики– Определение более чем
- 31. Не всегда активность фермента в
- 32. Перед тем как указывать на
- 33. АлкогольдегидрогеназаАлкогольдегидрогеназа (АДГ; КФ 1.1.1.1.) печеночный цитоплазматический фермент,
- 34. АлкогольдегидрогеназаИзоферментный спектр алкогольдегидрогеназы печени отражает патологические изменения
- 35. АльдолазаАльдолаза (фруктозобисфосфат-(фруктозодифосфат)-альдолаза; КФ 4.1.2.13) – фермент, относящийся
- 36. Альфа-амилаза (1,4-a-D-глюкан глюканогидролаза; КФ 3.2.1.1) относится к
- 37. Альфа-амилаза Плазма крови человека содержит альфа-амилазы
- 38. Альфа-амилаза Оба изофермента амилазы имеют молекулярную массу около
- 39. Альфа-амилаза Выявление гиперамилаземи и гиперамилазурии является важным, но
- 40. Альфа-амилаза АМ · КРС · 100
- 41. Альфа-амилаза В норме амилазо-креатининовый индекс не выше 3 Превышение
- 42. Альфа-амилаза При заболеваниях, протекающих под маской панкреатита, содержание
- 43. АминотрансферазыАспартатаминотрансфераза (КФ 2.6.1.1. L-аспартат: 2-оксоглутарата-минотрансфераза, АСТ или
- 44. АминотрансферазыАланинаминотрансфераза (КФ 2.6.1.2. L-аланин: 2-оксоглутарата-минотрансфераза, АЛТ или
- 45. АминотрансферазыАминотрансферазы катализируют процессы трансаминирования. Они распределены по
- 46. АминотрансферазыАсАТ имеет изоферменты, локализованные в цитозоле, в
- 47. АминотрансферазыАсАТ в высоких концентрациях присутствует в клетках
- 48. Аминотрансферазы Поражение любого из этих органов и тканей
- 49. Аминотрансферазы Наиболее резкие изменения АсАТ наблюдаются при поражении
- 50. Аминотрансферазы Снижение активности АсАТ:при недостаточности пиридоксина (витамина В6)при почечной недостаточности при беременности
- 51. Аминотрансферазы Повышение активности АлАТ наиболее часто отмечается при острых заболеваниях печени и желчных путей.
- 52. Аминотрансферазы Коэффициент де Ритис - АсАТ/АлАТ = 1,3
- 53. Гамма-глутамилтрансфераза Гамма-глутамилтрансфераза (ГГТ; КФ 2.3.2.2) Катализирует перенос гамма-глутамилового
- 54. Гамма-глутамилтрансфераза Тест по определению активности ГГТ в последнее
- 55. Гамма-глутамилтрансфераза Активность ГГТ в сыворотке крови повышается при
- 56. Гамма-глутамилтрансфераза Существенное увеличение активности ГГТ наблюдается при холестазе,
- 57. Глутаматдегидрогеназа Глутаматдегидрогеназа (ГДГ; КФ 1.4.1.3) – фермент, катализирующий превращение глутамата в 2-оксоглутарат и аммиак.
- 58. Глутаматдегидрогеназа ГДГ в наибольшем количестве содержится в клетках
- 59. Глутаматдегидрогеназа Повышение активности ГДГ и ГГТ во многом
- 60. Глутатионредуктаза Глутатионредуктаза (ГР; КФ 1.6.4.2) – НАДФ-зависимый фермент, катализирующий превращение окисленной формы глутатиона в восстановленную.
- 61. Глутатионредуктаза ГР присутствует практически во всех тканях, но
- 62. Глутатионредуктаза Повышение активности фермента наблюдается при гепатите, механической
- 63. Глутатионредуктаза Недостаток ГР отмечается при дефиците рибофлавина.
- 64. Глутатионпероксидаза Глутатионпероксидаза (ГП, КФ 1.11.1.9) – один из
- 65. Глутатионпероксидаза Содержится практически во всех тканях. ГП клеток
- 66. Глутатионпероксидаза Пероксид водорода и активные радикалы образуются в
- 67. Глутатионпероксидаза Определение ГП помогает оценить антиоксидантную способность организма
- 68. Глутатионпероксидаза Увеличение активности наблюдается при: дефиците глюкозо-6-фосфатдегидрогеназыостром лимфоцитарном лейкозе талассемии
- 69. Глутатионпероксидаза Уменьшение активности ГП сопровождает: сердечно-сосудистые заболеванияатеросклероз сахарный
- 70. Глутатионпероксидаза Уменьшение активности ГП значительно повышает риск возникновения раковых заболеваний
- 71. Глюкозо-6-фосфатдегидрогеназа Одним из основных поставщиков НАДФН для глутатионовой
- 72. Глюкозо-6-фосфатдегидрогеназа В большом количестве находится в эритроцитах и
- 73. Изоцитратдегидрогеназа Изоцитратдегидрогеназа (ИДГ; КФ 1.1.1.42) – фермент, имеющий
- 74. Изоцитратдегидрогеназа НАДФ-зависимая форма присутствует во всех тканях, но
- 75. Каталаза Каталаза (КФ 1.11.1.6; Н2О2:Н2О2 – оксидоредуктаза) –
- 76. Каталаза- В клетках каталаза локализуется в пероксисомах.
- 77. Каталаза Каталазный индекс (отношение величины каталазной активности определенного
- 78. Каталаза Уменьшение активности каталазы отмечается при злокачественных новообразованиях
- 79. Креатинкиназа Креатинкиназа или креатинфосфокиназа (КК; КФ 2.7.3.2.) катализирует
- 80. Креатинкиназа Фермент существует в виде трех изоферментов: КК-ВВ
- 81. Креатинкиназа Увеличение общей КК: травмы, операции, инфаркт миокарда,
- 82. Креатинкиназа КК-ММ увеличивается в сыворотке при тех же состояниях, как и общая КК.
- 83. Креатинкиназа КК-МВ увеличивается более чем в 1,5 раза при: инфаркте миокарданезначительно увеличивается при:миокардитахстенокардиизатяжной аритмиишокетяжелых отравлениях
- 84. КреатинкиназаКК-ВВ незначительно повышается при:некоторых формах ракатравме сердечной
- 85. Лактатдегидрогеназа Лактатдегидрогеназа (ЛДГ; КФ 1.1.1.27) катализирует обратимое восстановление пирувата до лактата, в качестве кофермента используется НАДН
- 86. Лактатдегидрогеназа ЛДГ имеет молекулярную массу около 134 кДа. ЛДГ
- 87. Лактатдегидрогеназа ЛДГ - это цитозольный фермент, присутствует во
- 88. Изоферменты Лактатдегидрогеназы
- 89. ЛактатдегидрогеназаПовышается при остром повреждении:сердцаэритроцитовпочекскелетных мышцпеченилегких кожи
- 90. Лактатдегидрогеназа Общая активность ЛДГ в сыворотке крови не
- 91. Лактатдегидрогеназа Однократное исследование ЛДГ-1 обладает клинической специфичностью в
- 92. Лактатдегидрогеназа Однократное исследование ЛДГ1 обладает клинической специфичностью в
- 93. Лактатдегидрогеназа Повышение ЛДГ1 отмечается также при опухолях репродуктивных органов: тератома, семинома яичка, дисгерминома яичника
- 94. Лактатдегидрогеназа ЛДГ2, ЛДГ3 и ЛДГ4 обладают промежуточными свойствами.
- 95. Лактатдегидрогеназа При нелимфоцитарных лейкозах увеличивается активность ЛДГ3 и ЛДГ4 Увеличение ЛДГ3 иногда наблюдается при острых панкреатитах
- 96. ЛактатдегидрогеназаАктивность ЛДГ4 возрастает при:поражении печенив активную фазу
- 97. ЛактатдегидрогеназаЛДГ 5 Наибольшее содержание этого изофермента характерно
- 98. ЛипазаЛипаза (КФ 3.1.1.3) – фермент, катализирующий расщепление глицеридов на глицерин и высшие жирные кислоты
- 99. Липаза Различают липазу : желудочного происхождения, поджелудочной железы, легких, кишечного сока, лейкоцитов и др.
- 100. Липаза Определение активности липазы в крови является наиболее
- 101. Липаза Одновременное определение уровня альфа-амилазы (кровь и моча)
- 102. 5-Нуклеотидаза 5-Нуклеотидаза (5'-рибонуклеотид – фосфогидролаза; КФ 3.1.3.5) катализирует
- 103. 5-Нуклеотидаза Возрастание активности 5-нуклеотидазы происходит параллельно активности щелочной
- 104. 5-Нуклеотидаза Главное отличие 5-нуклеотидазы от щелочной фосфатазы: отсутствие
- 105. Сорбитолдегидрогеназа Сорбитолдегидрогеназа (полиолдегидрогеназа, L-идитол, НАД+5-оксидоредуктаза, СДГ, КФ 1.1.1.14)
- 106. Сорбитолдегидрогеназа СДГ содержится преимущественно в цитоплазме гепатоцитов, поэтому повышение активности фермента специфично отражает поражение печени.
- 107. Супероксиддисмутаза Супероксиддисмутаза (супероксид оксидоредуктаза, СОД, КФ 1.15.1.1.) фермент
- 108. Супероксиддисмутаза При инфаркте миокарда СОД защищает сердечную мышцу
- 109. Супероксиддисмутаза Степень повышения СОД обратно пропорциональна деятельности левого
- 110. Супероксиддисмутаза Значительное увеличение активности СОД возможно при:ишемии органов нефропатиизаболеваниях, сопровождающихся воспалением (ревматоидный артрит)сепсисе
- 111. Фосфатазы Ферменты, катализирующие разрыв сложноэфирной связи в моноэфирах
- 112. Щелочная фосфатаза Оптимум рН щелочной фосфатазы лежит
- 113. Щелочная фосфатаза В сыворотке несколько изоферментов ЩФ,
- 114. Щелочная фосфатаза 1. Костная ЩФ В кости ЩФ
- 115. Щелочная фосфатаза 1. Костная ЩФЗначительное увеличение ее
- 116. Щелочная фосфатаза 2. Печеночная ЩФПредставлена двумя изоферментами.1
- 117. Щелочная фосфатаза 3. ЩФ желчи - фермент
- 118. Щелочная фосфатаза 4. Кишечная ЩФ Синтезируется энтероцитами,
- 119. Щелочная фосфатаза 5. Почечная ЩФ Частично всасывается
- 120. Щелочная фосфатаза 6. Плацентарная ЩФ Появляется в
- 121. Щелочная фосфатаза 7. Неидентифицированные изоферменты ЩФ изоферменты
- 122. Кислая фосфатаза Фосфатаза кислая (КФ, КФ 3.1.3.2)
- 123. Кислая фосфатаза Под наименованием «кислая фосфатаза» подразумевают
- 124. Кислая фосфатаза Активность кислой фосфатазы сыворотки крови
- 125. Кислая фосфатаза Определение кислой фосфатазы в сыворотке
- 126. Тартрат-резистентная кислая фосфатаза (TRACP 5B) TRACP5B –
- 127. Холинэстераза В тканях человека обнаружены два различных
- 128. Холинэстераза Определение активности холинэстеразы в сыворотке представляет
- 129. Холинэстераза Снижение активности холинэстеразы наблюдается при тяжелых хронических заболеваниях печени.
- 130. Холинэстераза Повышение активности холинэстеразы наблюдается при нефротическом
- 131. Эластаза Эластаза-1 (панкреатическая) является протеолитическим ферментом, синтезируется
- 132. Эластаза Подобно другим панкреатическим ферментам (амилаза, липаза)
- 133. Общие правила работы с ферментамиНельзя сильно встряхивать
- 134. Общие правила работы с ферментами2. Растворенные, лиофильно
- 135. 3. Время начала и окончания ферментативной реакции
- 136. 5. Не изменять соотношение рабочий реагент/сыворотка.6. Нельзя
- 137. 8. Длина оптического пути кюветы должна соответствовать
- 138. 11. Следить за качеством воды12. Использовать поверенные
- 139. 14. Строго соблюдать условия хранения15. Регулярно проверять
- 140. Спектр ферментов, определяемых в ИДЦАльфа амилаза (сыворотка
- 141. Скачать презентацию
- 142. Похожие презентации









































































































































Слайд 2
ФЕРМЕНТЫ – высокоэффективные биологические катализаторы, синтезируемые живыми клетками
Впервые
обнаружены в дрожжах
Слайд 3
ЧРЕЗВЫЧАЙНО ВАЖНАЯ РОЛЬ
Участвуют во всех химических процессах
Клетка
Организм
Проявляют свою
каталитическую активность в водной среде
Слайд 4
ФЕРМЕНТЫ – ПРОСТЫЕ БЕЛКИ
СОСТОЯТ ТОЛЬКО ИЗ
ПОЛИПЕПТИДНЫХ ЦЕПЕЙ
ГИДРОЛИЗУЮТСЯ ДО
АМИНОКИСЛОТ
ПЕПСИН, ТРИПСИН, УРЕАЗА
Слайд 5
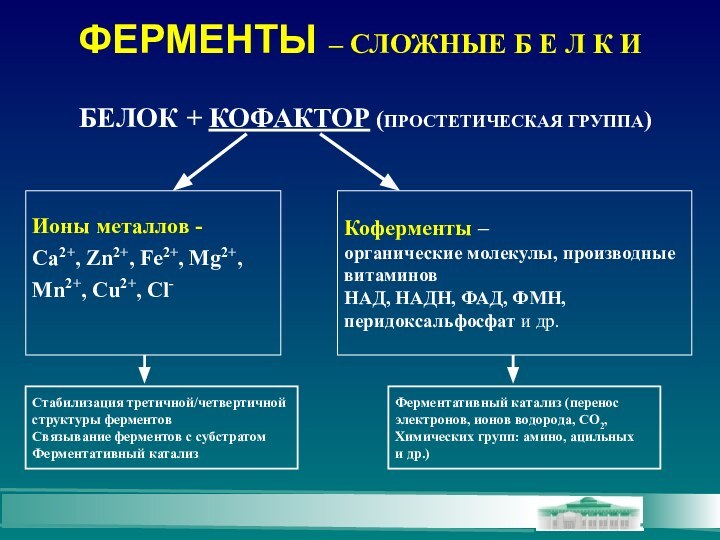
ФЕРМЕНТЫ – СЛОЖНЫЕ Б Е Л К И
Ионы
металлов -
Ca2+, Zn2+, Fe2+, Mg2+,
Mn2+, Cu2+, Cl-
Коферменты –
органические молекулы,
производныевитаминов
НАД, НАДН, ФАД, ФМН,
перидоксальфосфат и др.
Стабилизация третичной/четвертичной
структуры ферментов
Связывание ферментов с субстратом
Ферментативный катализ
Ферментативный катализ (перенос
электронов, ионов водорода, СО2,
Химических групп: амино, ацильных
и др.)
БЕЛОК + КОФАКТОР (ПРОСТЕТИЧЕСКАЯ ГРУППА)
Слайд 6 Ф Е Р М Е Н Т Ы
–
ВЫСОКОЭФФЕКТИВНЫЕ КАТАЛИЗАТОРЫ
Увеличивают скорость химической реакции
в миллионы/миллиарды раз
БЕЗ УЧАСТИЯ ФЕРМЕНТОВ
ХИМИЧЕСКИЕРЕАКЦИИ ПРОТЕКАЮТ ТАК МЕДЛЕННО, ЧТО
ПОЧТИ НЕ ОКАЗЫВАЮТ ВЛИЯНИЯ НА МЕТАБОЛИЗМ
! ! !
Слайд 7
Изоферменты
фермент, существующий в виде нескольких изоформ
ферменты из
одного источника
катализируют одну и ту же реакцию
отличаются
по а/к составумогут иметь различный молекуллярный вес
разную электрофоретическую подвижность
разные иммунологические/биохимические характеристики
различный рН-оптимум
разная стабильность
разные способы регуляции
ЛДГ – 5 изоформ – тетрамеры – комбинация 2 типов субъединиц
КК – 2 субъединицы – 3 изоформы
Слайд 8
ОРГАНЫ И ТКАНИ ИМЕЮТ ХАРАКТЕРНЫЙ
ДЛЯ НИХ НАБОР ИЗОФЕРМЕНТОВ
ОКОЛО
100 ФЕРМЕНТОВ ИМЕЮТ ИЗОФОРМЫ
РАСПРЕДЕЛЕНИЕ ИЗОФЕРМЕНТОВ ЛДГ, КК,
α-АМИЛАЗЫ В
СЫВОРОТКЕ ВАЖНО ДЛЯДИАГНОСТИКИ РЯДА ЗАБОЛЕВАНИЙ
Слайд 9 С У Б С Т Р А Т
Ы – вещества, с которыми происходит химическое превращение под действием
ферментовСУБСТРАТЫ –
ПРИРОДНЫЕ ВЕЩЕСТВА
ХИМИЧЕСКИ СИНТЕЗИРОВАННЫЕ
Фермент может иметь
один или несколько субстратов
Слайд 10
Каталитическая активность
Способность фермента превращать в продукт
определенное количество молекул
субстрата
в единицу времени, оставаясь неизменным
Ферменты могут осуществлять
от 1 до
106 циклов превращенийсубстрата в секунду
1 моль трипсина 100 цикл/сек, глюкозоксидаза –
17 000 цикл/сек, карбоангидраза – 600 000 цикл/сек
Слайд 11
АКТИВАТОРЫ ФЕРМЕНТОВ
Соединения, которые приводят
фермент в каталитически
активное состояние
Ионы двухвалентных
металлов:
Zn2+, Cа2+, Mg2+, Cu2+
Слайд 12
ИНГИБИТОРЫ ФЕРМЕНТОВ
Соединения, которые снижают каталитическую
активность ферментов
И н г
и б и р о в а н и
еобратимое
необратимое
активность фермента
восстанавливается
активность фермента
не восстанавливается
Слайд 13
ИНГИБИТОРЫ ФЕРМЕНТОВ
КОНКУРЕНТНЫЕ
НЕКОНКУРЕНТНЫЕ
СВЯЗЫВАЕТСЯ С АКТИВНЫМ
ЦЕНТРОМ ФЕРМЕНТА
↓ СКОРОСТЬ КАТАЛИЗА, СНИЖАЯ
ДОЛЮ
МОЛЕКУЛ ФЕРМЕНТА,
СВЯЗЫВАЮЩИХ СУБСТРАТ
СВОЙ УЧАСТОК СВЯЗЫВАНИЯ
НА МОЛЕКУЛЕ ФЕРМЕНТА
↓ СКОРОСТЬ
КАТАЛИЗА, ИЗМЕНЯЯСТРУКТУРУ АКТИВНОГО
ЦЕНТРА ФЕРМЕНТА
Слайд 14
СПЕЦИФИЧНОСТЬ ФЕРМЕНТА
ДЕЙСТВИЕ КАЖДОГО ФЕРМЕНТА
СТРОГО ОГРАНИЧЕНО ОДНИМ ТИПОМ
РЕАКЦИИ И
ОДНИМ СУБСТРАТОМ
(НЕБОЛЬШИМ ЧИСЛОМ СХОДНЫХ
ХИМИЧЕСКИХ ВЕЩЕСТВ)
Слайд 15
Международная единица активности
МЕ - КОЛИЧЕСТВО ФЕРМЕНТА, КОТОРОЕ КАТАЛИЗИРУЕТ
ПРЕВРАЩЕНИЕ
1 МКМОЛЯ СУБСТРАТА ИЛИ ПОЛУЧЕНИЕ 1 МКМОЛЯ
ПРОДУКТА В МИНУТУ
В СТАНДАРТНЫХ ОПТИМАЛЬНЫХ УСОВИЯХЕдиница активности в системе СИ – катал (кат.) –
количество фермента, которое катализирует
превращение 1 моля субстрата или получение
1 моля продукта в секунду
1 кат. = 6 · 107 МЕ 1 МЕ = 16.67 · 10-9 кат.
Слайд 17
Ферменты участвуют во всех биологических процессах
Нарушение метаболизма, вызванное
заболеванием, приводит к изменению концентрации соответствующих ферментов в биологических
жидкостяхОпределение активности ферментов в сыворотке
крови и моче является незаменимым орудием
в диагностике и мониторинге целого
ряда заболеваний
Слайд 18
Применение ферментов в медицине
диагностическое (энзимодиагностика)
терапевтическое (энзимотерапия)
в
качестве специфических реактивов для определения ряда веществ (ферментативные методы
определения субстратов)
Слайд 19
Энзимотерапия
Заместительная терапия - использование ферментов в случае их
недостаточности:
Заместительная энзимотерапия эффективна при желудочно-кишечных
заболеваниях, связанных с недостаточностью секреции пищеварительных соков. Например, пепсин используют при ахилии, гипо- и анацидных гастритах. Дефицит панкреатических ферментов также в значительной степени может быть компенсирован приёмом внутрь препаратов, содержащих основные ферменты поджелудочной железы (фестал, энзистал, мезим-форте и др.))
Слайд 20
Энзимотерапия
Как элемент комплексной терапии - применение ферментов в
сочетании с другой терапией.
В качестве
дополнительных терапевтических средств ферменты используют при ряде заболеваний. Протеолитические ферменты (трипсин, химотрипсин) применяют при местном воздействии для обработки гнойных ран с целью расщепления белков погибших клеток, для удаления сгустков крови или вязких секретов при воспалительных заболеваниях дыхательных путей.
Ферментные препараты рибонуклеазу и дезоксирибонуклеазу используют в качестве противовирусных препаратов при лечении аденовирусных конъюнктивитов, герпетических кератитов.
Ферментные препараты стали широко применять при тромбозах и тромбоэмболиях. С этой целью используют препараты фибринолизина, стрептолиазы, стрептодеказы, урокиназы.
Фермент гиалуронидазу (лидазу), катализирующий расщепление гиалуроновой кислоты, используют подкожно и внутримышечно для рассасывания контрактур рубцов после ожогов и операций (гиалуроновая кислота образует сшивки в соединительной ткани)
Слайд 21
Применение ферментов в качестве специфических реактивов
специфические эндонуклеазы, катализирующие
разрывы межнуклеотидных связей ДНК, для диагностики фенилкетонурии, α- и
β-талассемии и других наследственных болезней)глюкозооксидазу применяют для количественного определения глюкозы в моче и крови.
Фермент уреазу используют для определения содержания количества мочевины в крови и моче.
С помощью различных дегидрогеназ обнаруживают соответствующие субстраты, например пируват, лактат, этиловый спирт и др.
Слайд 22
Значение энзимодиагностики
Известно около 20 тестов, основанных на количественном
определении активности ферментов (и изоферментов), главным образом в крови
(реже в моче), а также в биоптатах. В практическом плане энзимологические тесты должны помогать в ранней постановке и дифференциации диагноза, информировать о возможном исходе болезни.
Слайд 23
Энзимодиагностика
постановка диагноза заболевания (или синдрома) на основе определения
активности ферментов в биологических жидкостях человека
В особую группу
выделяются иммуноферментные диагностические методы, состоящие в применении антител, химически связанных с каким-либо ферментом, для определения в жидкостях веществ, образующих с данными антителами комплексы антиген — антитело.
Слайд 24
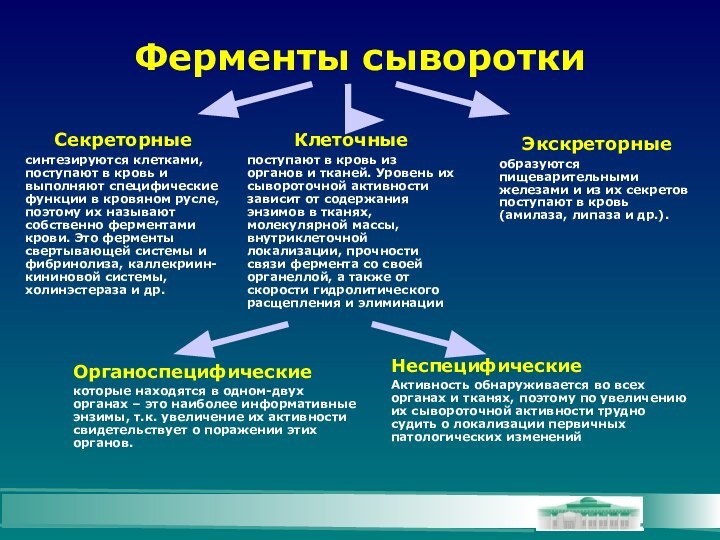
Ферменты сыворотки
Клеточные
поступают в кровь из органов и тканей.
Уровень их сывороточной активности зависит от содержания энзимов в
тканях, молекулярной массы, внутриклеточной локализации, прочности связи фермента со своей органеллой, а также от скорости гидролитического расщепления и элиминацииСекреторные
синтезируются клетками, поступают в кровь и выполняют специфические функции в кровяном русле, поэтому их называют собственно ферментами крови. Это ферменты свертывающей системы и фибринолиза, каллекриин-кининовой системы, холинэстераза и др.
Экскреторные
образуются пищеварительными железами и из их секретов поступают в кровь (амилаза, липаза и др.).
Органоспецифические
которые находятся в одном-двух органах – это наиболее информативные энзимы, т.к. увеличение их активности свидетельствует о поражении этих органов.
Неспецифические
Активность обнаруживается во всех органах и тканях, поэтому по увеличению их сывороточной активности трудно судить о локализации первичных патологических изменений
Слайд 25
Причины повышения активности клеточных ферментов в крови
нарушение проницаемости
мембраны клеток (при воспалительных процессах)
нарушение целостности клеток (при некрозе)
повышенная
пролиферация клеток с ускорением клеточного цикла (например, при онкопролиферативных процессах)повышенный синтез ферментов
обструкция путей секреции ферментов в полости
снижение клиренса (например, активность амилазы в сыворотке повышается при острой почечной недостаточности)
Слайд 26 Факторы, определяющие концентрацию фермента в крови при повреждении
клеток
природа повреждающего воздействия,
время действия и степень повреждения биомембран
клеток и субклеточных структур органов,период полужизни (полураспада) в плазме крови каждого из диагностических ферментов,
особенности распределения (топографии) ферментов в индивидуальных органах и тканях, а также их внутриклеточная локализация.
Слайд 27
Примеры различной локализация ферментов в клетке
Клеточная мембрана
кислая фосфатаза,
5’-нуклеотидаза,
гамма-глутамилтрансфераза (ГГТ)
Цитоплазма
аланинаминотрансфераза (АлАТ),
аспартатаминотрансфераза (АсАТ),
лактатдегидрогеназа (ЛДГ), креатинкиназа (КК)
Митохондрии
АсАТ
КФК
глутаматдегидрогеназа (ГДГ)
Лизосомы
Щелочная фосфатаза (ЩФ)
Слайд 28
Причины понижения активности клеточных ферментов в крови (гипоферментемия)
Гипоферментемия
встречается относительно редко и касается в основном секреторных ферментов.
В подавляющем большинстве случаев она связана с генетически детерминированными нарушениями синтеза определенных энзимов,
реже – с ингибированием, усиленной деградацией или экскрецией
Слайд 29
Механизмы удаления ферментов из крови
Большинство ферментов катаболизируется плазменными
протеазами и удаляется ретикулоэндотелиальной системой.
Часть ферментов выделяется со
слюной, желчью и другими секреторными жидкостями. Через почечный фильтр небольшие молекулы с молекулярной массой не более 60–70 кДа, (поэтому в норме количество экскретируемых ферментов невелико)
Слайд 30
Основные правила дифференциальной диагностики
– Определение более чем одного
фермента. Разные ткани содержат ферменты в разных количествах. Так,
АлАТ и АсАТ содержатся в гепатоцитах и кардиомиоцитах, но АлАТ существенно больше в печени, а АсАТ в сердце. Поэтому при повреждении печени относительно больше повышается АлАТ, а при повреждении сердца – АсАТ.– Определение спектра изоферментов. Данный подход основан на том, что отдельные изоформы характерны для разных тканей.
– Определение активности ферментов в динамике. Скорость изменения активности фермента в сыворотке определяется разницей между скоростью его появления в сыворотке и скоростью удаления из системы циркуляции. При инфаркте органа и некрозе поврежденных клеток в сыворотке крови происходит повышение активности внутриклеточных ферментов, специфичных для данной ткани, затем после выхода всего фермента активность его снижается. Важным является определение динамики изменения фермента и определение его активности в период повышения в сыворотке, т. к. слишком раннее взятие пробы для анализа может предшествовать подъему активности, слишком позднее – также не позволит получить необходимую информацию.
Слайд 31 Не всегда активность фермента в сыворотке
отражает тяжесть заболевания. Так, острое повреждение клеток при вирусном
гепатите может сопровождаться очень высоким подъемом активности ферментов, которая будет падать по мере выздоровления. В то же время при циррозе печень может быть значительно сильнее вовлечена в патологический процесс, но скорость повреждения клеток ниже и активность ферментов в сыворотке будет повышена незначительно или будет находиться в пределах референтных значений. Этот пример еще раз подчеркивает, что любые результаты по исследованию активности ферментов в сыворотке должны быть обязательно сопоставлены с другими лабораторными анализами и с клинической картиной заболевания.Слайд 32 Перед тем как указывать на возможность
патологического процесса, необходимо исключить возможность неспецифического повышения активности ферментов
в сыворотке. Так, относительно невысокое повышение в плазме активности трансаминаз характерно для многих неспецифических патологических процессов. Тяжелая физическая работа, массивные внутримышечные инъекции могут привести к повышению активности КК в сыворотке. Некоторые лекарственные средства, в частности фенитоин, фенобарбитал могут индуцировать синтез микросомального фермента ГГТ и вызвать его повышение в сыворотке без всякого заболевания. Активность ферментов в сыворотке может меняться в результате агрегации с образованием макромолекул, например, при образовании комплексов с иммуноглобулинами, в которые вступают ЛДГ, ЩФ и КК.
Слайд 33
Алкогольдегидрогеназа
Алкогольдегидрогеназа (АДГ; КФ 1.1.1.1.) печеночный цитоплазматический фермент, класса
оксидоредуктаз. АДГ является цинксодержащем ферментом и преимущественно располагается в
центролобулярном регионе печени. Алкогольдегидрогеназа способна нейтрализировать небольшие дозы алкоголя. Содержится в организме южных народов, в том числе у украинцев, русских, но почти отсут ствует у северных. Фермент катализируюет в присутствии НАД окисление спиртов и ацеталей до альдегидов и кетонов.Идентифицированы изоферменты АДГ, специфичные для печени, слизистой желудка и почек. В больших количествах фермент находится лишь в печени, но небольшие его количества содержат почки. Следы фермента также обнаруживаются в сердечной и скелетной мускулатуре человека. В сыворотке крови здорового человека отсутствует. Активность АДГ ответственна за метаболическое превращение метанола и этиленгликоля в токсические соединения. Этот эффект тормозится введением этанола.
Слайд 34
Алкогольдегидрогеназа
Изоферментный спектр алкогольдегидрогеназы печени отражает патологические изменения в
организме, что используется для диагностических целей. АДГ – семейство
тесно связанных ферментов с выраженным полиморфизмом, что может влиять на скорость выведения этанола. Резкое повышение содержания фермента наблюдается при острых гепатитах (при этом его показатели приходят к норме раньше, чем показатели трансаминаз). При обтурационной желтухе, циррозах печени, инфаркте миокарда, мышечной дистрофии Эрба обычно не наблюдается повышения активности фермента в крови. Цианиды, йодоацетат тормозят действие энзима. Является специфическим для клеток печени. Появление его в сыворотке крови свидетельствует о повреждении клеток печени. Служит критерием выраженности гепатоцеллюлярного некроза и внутрипеченочного холестаза. АДГ рассматривается как высокочувствительный маркер аноксии печени с поражением центров долек.Изоформы алкогольдегидрогеназы имеют большое значение в дифференциальной диагностике заболеваний печени. Так, АДГ1 повышается при вирусных гепатитах, АДГ2 – при алкогольных гепатитах, активности АДГ3 так же, как и АДГ2, чаще увеличиваються при циррозе печени. Референтные пределы: <2,8 МЕ/л · 0,017 [<0,05 мккат/л].
Слайд 35
Альдолаза
Альдолаза (фруктозобисфосфат-(фруктозодифосфат)-альдолаза; КФ 4.1.2.13) – фермент, относящийся к
лиазам, катализирующий превращение фруктозо-1,6-дифосфата (бисфосфата) в дигидроксиацетонфосфат и глицеральдегид-3-фосфат
в процессе гликолиза. Фермент играет важнейшую роль в энергетическом обмене. Молекулярная масса фермента 147–180 кДа, состоит из двух полипептидных цепей. Альдолаза присутствует во всех тканях организма. Генетически обусловленная неполноценность альдолазы является причиной наследственной непереносимости фруктозы.В норме в сыворотке крови активность альдолазы составляет от 0,0038 до 0,02 (в среднем 0,012) мкмоль фруктозо-1,6-дифосфата, превращенного ферментом, содержащимся в 1 мл сыворотки крови, за 1 мин при 37 °С.
Активность альдолазы в крови служит дополнительным диагностическим признаком ряда заболеваний. В ткани злокачественных опухолей фермент в несколько раз активнее, чем в неизмененных тканях, в эритроцитах активность фермента в 100 раз выше, чем в сыворотке крови, гемолиз существенно искажает результаты анализа. При ряде заболеваний (прогрессирующая мышечная дистрофия, инфаркт миокарда, активный ревматизм, рак, поражения печени и др.) активность альдолазы в крови повышается, причем тем значительнее, чем тяжелее протекает болезнь.
В качестве унифицированного метода определения альдолазы принят метод Товарницкого–Валуйской, основанный на том, что продукты расщепления фруктозо-1,6-фосфата альдолазой при реакции с 2,4-динитрофенилгидразином образуют гидразоны, окрашенные в щелочной среде. Интенсивность окраски пропорциональна активности фермента.
Слайд 36 Альфа-амилаза (1,4-a-D-глюкан глюканогидролаза; КФ 3.2.1.1) относится к группе
гидролаз, катализирующих гидролиз полисахаридов до моно- и дисахаридов (мальтоза,
глюкоза), разрушая связи между 1 и 4 атомами углеродаАльфа-амилаза
Слайд 37
Альфа-амилаза
Плазма крови человека содержит альфа-амилазы двух
изозимных типов:
панкреатическую (Р-тип), вырабатываемую поджелудочной железой (40%)
слюнную (S-тип),
продуцируемую слюнными железами (60%)Уровень активности альфа-амилазы в норме:
в сыворотке 25–220 МЕ/л;
в моче 10–490 МЕ/л
Слайд 38
Альфа-амилаза
Оба изофермента амилазы имеют молекулярную массу около 45
кДа, поэтому фильтруются в почках и экскретируются с мочой.
65 % амилазной активности мочи обусловлено панкреатической амилазой.Активность α-амилазы в течение дня и от одного дня к другому подвергается значительным изменениям. Поэтому для наблюдения за динамикой изменения активности фермента необходим забор крови для анализа в одно и то же время суток. Существуют индивидуальные различия этих показателей у обследуемых без патологии органов пищеварения.
Слайд 39
Альфа-амилаза
Выявление гиперамилаземи и гиперамилазурии является важным, но не
специфическим тестом для острого панкреатита; кроме того, повышение ее
активности может быть кратковременным. Для повышения информативности полученных результатов исследования полезно определение активности амилазы крови и мочи сочетать с параллельным определением концентрации креатинина в моче и сыворотке крови. На основании этих данных рассчитывают индекс амилазо-креатининового клиренса по формуле
Слайд 40
Альфа-амилаза
АМ · КРС · 100
КРМ · АС
где:
AM – амилаза мочи
АС – амилаза
сыворотки КРМ – креатинин в моче
КРС – креатинин в сыворотке
Слайд 41
Альфа-амилаза
В норме амилазо-креатининовый индекс не выше 3
Превышение считается
признаком панкреатита, так как при панкреатите возрастает уровень истинно
панкреатической амилазы, и ее клиренс осуществляется на 80 % быстрее клиренса амилазы слюны
Слайд 42
Альфа-амилаза
При заболеваниях, протекающих под маской панкреатита, содержание амилазы
сыворотки может увеличиваться, но показатель амилазо-креатининового клиренса остается нормальным
Слайд 43
Аминотрансферазы
Аспартатаминотрансфераза
(КФ 2.6.1.1. L-аспартат: 2-оксоглутарата-минотрансфераза, АСТ или АсАТ
или более редкое название глутамат-оксалоацетаттрансаминаза (ГОТ).
Нормальные величины активности ферментов
в сыворотке/плазме –АсАТ: 10–30 МЕ/л
Слайд 44
Аминотрансферазы
Аланинаминотрансфераза
(КФ 2.6.1.2. L-аланин: 2-оксоглутарата-минотрансфераза, АЛТ или АлАТ
или более редкое название глутаматпи-руваттрансаминаза (ГТП).
Нормальные величины активности ферментов
в сыворотке / плазме –АлАТ: 7–40 МЕ/л
Слайд 45
Аминотрансферазы
Аминотрансферазы катализируют процессы трансаминирования.
Они распределены по всем
органам и тканям.
Роль кофермента в трансаминазных реакциях играет
пиридоксальфосфат (витамин В6).
Слайд 46
Аминотрансферазы
АсАТ имеет изоферменты, локализованные
в цитозоле,
в митохондриях,
АлАТ – имеет изоферменты, локализованные
в цитозоле (преимущественно)
в митохондриях
(незначительно)
Слайд 47
Аминотрансферазы
АсАТ в высоких концентрациях присутствует в клетках сердечной
и скелетных мышц, печени, почках, поджелудочной железе и эритроцитах.
АлАТ в высоких концентрациях присутствует в клетках печени и в меньшей степени в скелетных мышцах, почках и сердце.
Слайд 48
Аминотрансферазы
Поражение любого из этих органов и тканей может
привести к существенному повышению трансаминаз в сыворотке крови
Слайд 49
Аминотрансферазы
Наиболее резкие изменения АсАТ наблюдаются при поражении сердечной
мышцы.
Например, при инфаркте миокарда активность АсАТ в сыворотке
крови может повышаться в 4–5 раз. Между размерами очага инфаркта и активностью АсАТ в сыворотке имеется тесная корреляция: если в течение нескольких дней не происходит нормализация активности фермента, это свидетельствует о расширении зоны инфаркта.
Слайд 50
Аминотрансферазы
Снижение активности АсАТ:
при недостаточности пиридоксина (витамина В6)
при почечной
недостаточности
при беременности
Слайд 51
Аминотрансферазы
Повышение активности АлАТ наиболее часто отмечается при острых
заболеваниях печени и желчных путей.
Слайд 52
Аминотрансферазы
Коэффициент де Ритис -
АсАТ/АлАТ = 1,3 ±
0,4
при заболеваниях печени – понижается
при заболеваниях
сердца – повышается
Слайд 53
Гамма-глутамилтрансфераза
Гамма-глутамилтрансфераза (ГГТ; КФ 2.3.2.2)
Катализирует перенос гамма-глутамилового остатка
с гамма-глутамилового пептида на аминокислоту, другой пептид или иной
субстрат. В организме человека фермент участвует в метаболизме глутатиона
Слайд 54
Гамма-глутамилтрансфераза
Тест по определению активности ГГТ в последнее время
приобретает все большее значение в диагностике заболеваний печени и
гепато-билиарного тракта, т. к. отличается большей чувствительностью, чем применяемые с этой целью тесты на АлАТ, АсАТ и ЩФ.
Слайд 55
Гамма-глутамилтрансфераза
Активность ГГТ в сыворотке крови повышается при любых
патологиях печени и желчных путей.
В зависимости от механизма
повреждения печени степень увеличения активности ГГТ в сыворотке крови, заметно отличается, что позволяет успешно использовать этот маркер для дифференциальной диагностики заболеваний печени.
Слайд 56
Гамма-глутамилтрансфераза
Существенное увеличение активности ГГТ наблюдается при холестазе, и
лишь незначительное – при повреждении паренхимы печени (некрозе гепатоцитов).
Слайд 57
Глутаматдегидрогеназа
Глутаматдегидрогеназа (ГДГ; КФ 1.4.1.3) – фермент, катализирующий превращение
глутамата в 2-оксоглутарат и аммиак.
Слайд 58
Глутаматдегидрогеназа
ГДГ в наибольшем количестве содержится в клетках печени.
Фермент
находится внутри митохондрий гепатоцитов, поэтому увеличение его активности отражает
глубину цитолиза клеток - по степени ее повышения можно судить о тяжести патологического процесса.
Слайд 59
Глутаматдегидрогеназа
Повышение активности ГДГ и ГГТ во многом сходно,
но есть различия: высокая активность ГДГ наблюдается при острых
повреждениях печени, а высокая ГГТ – при длительных патологических процессах в печени.
Слайд 60
Глутатионредуктаза
Глутатионредуктаза (ГР; КФ 1.6.4.2) – НАДФ-зависимый фермент, катализирующий
превращение окисленной формы глутатиона в восстановленную.
Слайд 61
Глутатионредуктаза
ГР присутствует практически во всех тканях, но наибольшее
его содержание в почках, печени, сердце и эритроцитах.
Слайд 62
Глутатионредуктаза
Повышение активности фермента наблюдается при гепатите, механической желтухе,
сахарном диабете, при дефиците глюкозо-6-фосфатдегидрогеназы, серповидной и мегалобластной анемиях,
после введения никотиновой кислоты, после физической нагрузки.
Слайд 64
Глутатионпероксидаза
Глутатионпероксидаза (ГП, КФ 1.11.1.9) – один из ключевых
ферментов антиоксидантной системы организма, функцией которого является разрушение и
инактивация пероксидов водорода и гидропероксидов (пероксидных радикалов) – токсичных соединений кислорода.
Слайд 65
Глутатионпероксидаза
Содержится практически во всех тканях. ГП клеток печени
состоит из четырех субъединиц, каждая из которых содержит в
активном центре атом селена.
Слайд 66
Глутатионпероксидаза
Пероксид водорода и активные радикалы образуются в результате
пероксидного окисления липидов (ПОЛ), которые приводят к дестабилизации клеточных
мембран и, в тяжелых случаях, к их разрушению. Активация ПОЛ наблюдается при различных заболеваниях: ишемия органов и тканей, сахарный диабет, атеросклероз и мн.др.
Слайд 67
Глутатионпероксидаза
Определение ГП помогает оценить антиоксидантную способность организма при
различных заболеваниях, а также у людей с повышенным риском
селенового дефицита (в старческом возрасте, при плохом питании, курении, алкоголизме, стрессе, почечной недостаточности, химиотерапии и др.), рекомендовать назначение препаратов для антиоксидантной терапии и оценивать эффективность терапии.
Слайд 68
Глутатионпероксидаза
Увеличение активности наблюдается при:
дефиците глюкозо-6-фосфатдегидрогеназы
остром лимфоцитарном лейкозе
талассемии
Слайд 69
Глутатионпероксидаза
Уменьшение активности ГП сопровождает:
сердечно-сосудистые заболевания
атеросклероз
сахарный диабет
аутоиммунные
заболевания (ревматоидный артрит)
процессы старения организма
муковисцидоз
шизофрению и маниакально-депрессивный
психоз
Слайд 70
Глутатионпероксидаза
Уменьшение активности ГП значительно повышает риск возникновения раковых
заболеваний
Слайд 71
Глюкозо-6-фосфатдегидрогеназа
Одним из основных поставщиков НАДФН для глутатионовой антиоксидантной
системы является пентозофосфатный путь, ключевым ферментом которого является Г6ФДГ.
Слайд 72
Глюкозо-6-фосфатдегидрогеназа
В большом количестве находится в эритроцитах и используется,
в основном, для выявления на следственных заболеваний, связанных с
дефицитом фермента – наиболее распространенной наследственной гемолитической анемии, обусловленной дефицитом активности Г6ФДГ эритроцитов.
Слайд 73
Изоцитратдегидрогеназа
Изоцитратдегидрогеназа (ИДГ; КФ 1.1.1.42) – фермент, имеющий 2
формы коферментной специфичности (НАД и НАДФ-зависимые) и катализирующий обратимое
окисление изоцитрата до 2-оксоглутарата.
Слайд 74
Изоцитратдегидрогеназа
НАДФ-зависимая форма присутствует во всех тканях, но наибольшая
ее активность обнаружена в печени, скелетной мускулатуре, сердце.
Повышение
активности ИДГ является чувствительным показателем поражения паренхимы печени, тяжелом инфаркте легкого, миелолейкоза, мегалобластной анемии.
Слайд 75
Каталаза
Каталаза (КФ 1.11.1.6; Н2О2:Н2О2 – оксидоредуктаза) – фермент,
катализирующий реакцию разложения пероксида водорода на воду и молекулярный
кислород:2 Н2О2 = О2 + 2Н2О
Слайд 76
Каталаза
- В клетках каталаза локализуется в пероксисомах.
-
Биологическая роль каталазы заключается в деградации пероксида
водорода, образующегося в клетках в результате действия ряда флавопротеиновых оксидаз и обеспечении эффективной защиты клеточных структур от разрушения под действием пероксида водорода.
Слайд 77
Каталаза
Каталазный индекс (отношение величины каталазной активности определенного объема
крови к количеству эритроцитов в этом объеме), увеличивается при
злокачественной и других макроцитарных анемиях
Слайд 78
Каталаза
Уменьшение активности каталазы отмечается при злокачественных новообразованиях в
печени и почках, причем существует зависимость между величиной опухоли,
скоростью ее роста и степенью уменьшения активности каталазы.
Слайд 79
Креатинкиназа
Креатинкиназа или креатинфосфокиназа (КК; КФ 2.7.3.2.) катализирует обратимую
реакцию фосфорилирования креатинина с участием АТФ в результате чего
образуются креатинфосфат и AДФ.
Слайд 80
Креатинкиназа
Фермент существует в виде трех изоферментов:
КК-ВВ (КК-1)
– мозговой,
КК-МВ (КК-2) – сердечный
КК-ММ (КК-3) –
мышечный
Слайд 81
Креатинкиназа
Увеличение общей КК:
травмы,
операции,
инфаркт миокарда,
уменьшение
кровоснабжения мышц,
миопатии,
дерматомиозит,
мышечные дистрофии,
миокардиты,
отравления, сопровождающиеся комой,
инфекционные болезни (например, брюшной тиф).
Слайд 83
Креатинкиназа
КК-МВ
увеличивается более чем в 1,5 раза при:
инфаркте миокарда
незначительно увеличивается при:
миокардитах
стенокардии
затяжной аритмии
шоке
тяжелых отравлениях
Слайд 84
Креатинкиназа
КК-ВВ
незначительно повышается при:
некоторых формах рака
травме сердечной мышцы
заболеваниях соединительной ткани
у новорожденных при родовой травме мозга
увеличиваться
в 6 раз при:родах (источником являются матка и плацента)
Слайд 85
Лактатдегидрогеназа
Лактатдегидрогеназа (ЛДГ; КФ 1.1.1.27) катализирует обратимое восстановление пирувата
до лактата, в качестве кофермента используется НАДН
Слайд 86
Лактатдегидрогеназа
ЛДГ имеет молекулярную массу около 134 кДа.
ЛДГ тетрамер,
состоящий из двух субъединиц – М (muscle – мышечная)
и Н (heart – сердечная).В сыворотке присутствуют 5 изоферментов, различающиеся составом субъединиц.
Слайд 87
Лактатдегидрогеназа
ЛДГ - это цитозольный фермент, присутствует во всех
клетках организма.
В печени, сердце, почках, скелетной мышце и
эритроцитах активность ЛДГ более чем в 500 раз выше, чем в сыворотке .
Слайд 89
Лактатдегидрогеназа
Повышается при остром повреждении:
сердца
эритроцитов
почек
скелетных мышц
печени
легких
кожи
Слайд 90
Лактатдегидрогеназа
Общая активность ЛДГ в сыворотке крови не является
специфическим тестом для определенной патологии. Поэтому необходимо разделять изоферменты
ЛДГ и, затем, оценивать вклад каждого в общую активность, т.к. они органоспецифичны
Слайд 91
Лактатдегидрогеназа
Однократное исследование ЛДГ-1 обладает клинической специфичностью в отношении
инфаркта миокарда в 66 % случаев, а определение ее
в динамике (через каждые 4–6 часов в течение суток) – в 86 %
Слайд 92
Лактатдегидрогеназа
Однократное исследование ЛДГ1 обладает клинической специфичностью в отношении
инфаркта миокарда в 66 % случаев, а определение ее
в динамике (через каждые 4–6 часов в течение суток) – в 86 %
Слайд 93
Лактатдегидрогеназа
Повышение ЛДГ1 отмечается также при опухолях репродуктивных органов:
тератома, семинома яичка, дисгерминома яичника
Слайд 94
Лактатдегидрогеназа
ЛДГ2, ЛДГ3 и ЛДГ4 обладают промежуточными свойствами. Активность
этих изоферментов повышается при массивном разрушении тромбоцитов (эмболия легочной
артерии, массивные гемотрансфузии) и вовлечении в патологический процесс лимфатической системы.
Слайд 95
Лактатдегидрогеназа
При нелимфоцитарных лейкозах увеличивается активность ЛДГ3 и ЛДГ4
Увеличение ЛДГ3 иногда наблюдается при острых панкреатитах
Слайд 96
Лактатдегидрогеназа
Активность ЛДГ4 возрастает при:
поражении печени
в активную фазу ревматизма
кардиосклерозе с нарушением гемодинамики
остром нефрите
поражениях почек
опухолях печени, предстательной
железы, шейки матки, молочной железы, кишечника тяжелых формах диабета
Слайд 97
Лактатдегидрогеназа
ЛДГ 5
Наибольшее содержание этого изофермента характерно для
скелетных мышц, печени, кожи, слизистых оболочек, а также клеток
некоторых злокачественных опухолей.Значительное увеличение отмечается при:
травмах, воспалительных и дегенеративных заболеваниях мышц
многих болезнях печени (гепатиты, циррозы и др.).
онкологических заболеваниях (например лимфолейкозы)
активная фаза ревматизма
глубоких поражениях почек, сопровождающихся их гипоксией, опухолях почек и отторжении пересаженной почки
при тяжелых формах диабета
Слайд 98
Липаза
Липаза (КФ 3.1.1.3) – фермент, катализирующий расщепление глицеридов
на глицерин и высшие жирные кислоты
Слайд 99
Липаза
Различают липазу :
желудочного происхождения,
поджелудочной железы,
легких,
кишечного сока,
лейкоцитов и др.
Слайд 100
Липаза
Определение активности липазы в крови является наиболее информативным
критерием диагностики острого панкреатита.
Содержание липазы увеличивается и снижается параллельно
повышению и снижению активности амилазы, но нормализация ее уровня происходит позже нормализации амилазы
Слайд 101
Липаза
Одновременное определение уровня альфа-амилазы (кровь и моча) и
липазы – основа диагностики острого панкреатита. Повышение обоих или
одного из ферментов выявляется у 98 % больных с острым панкреатитом.
Слайд 102
5-Нуклеотидаза
5-Нуклеотидаза (5'-рибонуклеотид – фосфогидролаза; КФ 3.1.3.5) катализирует гидролиз
только нуклеотид-5-фосфатов.
Фермент распространен во многих тканях организма (печень,
мозг, мышцы, почки, легкие, щитовидная железа, аорта).
Слайд 103
5-Нуклеотидаза
Возрастание активности 5-нуклеотидазы происходит параллельно активности щелочной фосфатазы
при холестазах любой локализации, но данный фермент более чувствителен
по отношению к первичному и вторичному билиарному циррозу, а также к хроническому активному гепатиту.
Слайд 104
5-Нуклеотидаза
Главное отличие 5-нуклеотидазы от щелочной фосфатазы: отсутствие реакции
на костные заболевания. Считается, что 5-нуклеотидаза является специфической «желчной»
фосфатазой.
Слайд 105
Сорбитолдегидрогеназа
Сорбитолдегидрогеназа (полиолдегидрогеназа, L-идитол, НАД+5-оксидоредуктаза, СДГ, КФ 1.1.1.14) катализирует
реакцию окисления сорбитола до фруктозы, при этом происходит восстановление
НАД
Слайд 106
Сорбитолдегидрогеназа
СДГ содержится преимущественно в цитоплазме гепатоцитов, поэтому повышение
активности фермента специфично отражает поражение печени.
Слайд 107
Супероксиддисмутаза
Супероксиддисмутаза (супероксид оксидоредуктаза, СОД, КФ 1.15.1.1.) фермент (металлопротеин),
катализирующий реакцию превращения двух супероксидных радикалов друг с другом,
превращая их в менее токсичный пероксид водорода и кислород .
Слайд 108
Супероксиддисмутаза
При инфаркте миокарда СОД защищает сердечную мышцу от
действия свободных радикалов, образующихся при ишемии, при этом в
сыворотке крови при инфаркте миокарда регистрируется высокая активность фермента.
Слайд 109
Супероксиддисмутаза
Степень повышения СОД обратно пропорциональна деятельности левого желудочка,
что используется как маркер для оценки повреждения миокарда и
при мышечной дистрофии.
Слайд 110
Супероксиддисмутаза
Значительное увеличение активности СОД возможно при:
ишемии органов
нефропатии
заболеваниях,
сопровождающихся воспалением (ревматоидный артрит)
сепсисе
Слайд 111
Фосфатазы
Ферменты, катализирующие разрыв сложноэфирной связи в моноэфирах фосфорной
кислоты с образованием свободного ортофосфата (аниона ортофосфорной кислоты); относятся
к классу гидролаз.
Слайд 112
Щелочная фосфатаза
Оптимум рН щелочной фосфатазы лежит в
щелочной среде (рН 8,6–10,1).
Фермент расположен на клеточной мембране
и принимает участие в транспорте фосфора.
Слайд 113
Щелочная фосфатаза
В сыворотке несколько изоферментов ЩФ, семь
из которых имеют наибольшее клинико-диагностическое значение.
Для диагностических целей
чаще всего проводят определение активности костной и печеночной форм фосфатазы
Слайд 114
Щелочная фосфатаза
1. Костная ЩФ
В кости ЩФ секретируется
остеобластами, ее роль в формировании кости до конца не
установлена. Предполагают, что она участвует в созревании матрикса и его минерализации.
Слайд 115
Щелочная фосфатаза
1. Костная ЩФ
Значительное увеличение ее активности
в сыворотке крови наблюдается при повышенной деятельности остеобластов:
рост
костей (у детей активность выше, чем у взрослых; увеличивается эта активность в последний триместр беременности), возобновлении движений после длительного постельного режима,
переломах, деформирующем остите,
рахите.
Слайд 116
Щелочная фосфатаза
2. Печеночная ЩФ
Представлена двумя изоферментами.
1 -
основной фермент при патологии гепатобилиарного тракта
2 - основной фермент
при гепатоцеллюлярной патологии
Слайд 117
Щелочная фосфатаза
3. ЩФ желчи - фермент холестаза
Фермент высвобождается из поврежденных желчных протоков при:
недостаточности выделения желчи,
обусловленным нарушением ее выработки печеночными клетками (внутрипеченочный холестаз); прекращении тока желчи по желчным протокам (внепеченочный холестаз)
Слайд 118
Щелочная фосфатаза
4. Кишечная ЩФ
Синтезируется энтероцитами, поступает
в просвет тонкого кишечника и частично всасывается в кровь.
Вклад ее в общую активность ЩФ невелик. Ее активность может быть увеличена у лиц с I или III группой крови, особенно после приема пищи, при заболеваниях кишечника, сопровождающихся диареей.
Слайд 119
Щелочная фосфатаза
5. Почечная ЩФ
Частично всасывается
в кровь, но в основном, экскретируется с мочой. Тест
используется в диагностике заболеваний почек (гломерулонефрит, пиелонефрит, нефропатии).
Слайд 120
Щелочная фосфатаза
6. Плацентарная ЩФ
Появляется в
сыворотке крови при беременности. Самое большое ее содержание отмечается
в третьем триместре. Очень высокие цифры активности ЩФ наблюдаются у женщин с преэклампсией, что является следствием повреждения плаценты. Низкая активность ЩФ у беременных говорит о недостаточности развития плаценты
Слайд 121
Щелочная фосфатаза
7. Неидентифицированные изоферменты ЩФ
изоферменты
Regan или Nagao опухолевого происхождения
наиболее часто определяются при раке
легкого
Слайд 122
Кислая фосфатаза
Фосфатаза кислая (КФ, КФ 3.1.3.2) –
фермент с широкой субстратной специфичностью, катализирующий расщепление сложноэфирных связей
с образованием свободного ортофосфата, по спектру активности близкий к щелочной фосфатазе, от которой отличается иным действием на серосодержащие эфиры, оптимумом рН (4,7–6,0; у ЩФ – 8,4–9,4)
Слайд 123
Кислая фосфатаза
Под наименованием «кислая фосфатаза» подразумевают все
фосфатазы, проявляющие оптимальную активность при рН < 7,0.
Это
ферменты, которые находятся в клетках различных тканей в лизосомах и вне их. Самая высокая концентрация кислой фосфатазы отмечается в предстательной железе (простатический изофермент)
Слайд 124
Кислая фосфатаза
Активность кислой фосфатазы сыворотки крови низкая
в нормальных условиях.
У мужчин примерно наполовину состоит из активности
простатической фосфатазы, остальная активность связана с ферментом, происходящим из печени и разрушенных тромбоцитов и эритроцитов. У женщин кислая фосфатаза сыворотки происходит преимущественно из печени, эритроцитов и тромбоцитов.
Слайд 125
Кислая фосфатаза
Определение кислой фосфатазы в сыворотке обычно
используют для выявления или мониторинга рака простаты у мужчин
Слайд 126
Тартрат-резистентная кислая фосфатаза (TRACP 5B)
TRACP5B – фермент,
секретируемый исключительно остеокластами и попадающий в повышенном количестве в
кровоток при увеличении количества и возрастании активности остеокластов.Определение уровня тартрат-резистентной кислой фосфатазы 5в может быть использовано в качестве маркера метастатического поражения скелета.
Слайд 127
Холинэстераза
В тканях человека обнаружены два различных фермента
этого типа:
ацетилхолинэстераза («истинная» холинэстераза; КФ 3.1.1.7), которая преимущественно
находится в нервной ткани, скелетных мышцах и в низкой концентрации в эритроцитах; сывороточная или псевдохолинэстераза, которая широко распространена, присутствует в печени, поджелудочной железе, секретируется печенью в кровь. Сывороточная холинэстераза является ферментом, катализирующим реакцию гидролиза ацетилхолина
Слайд 128
Холинэстераза
Определение активности холинэстеразы в сыворотке представляет наибольший
клинический интерес как показатель состояния белково-синтезирующей функции печени
Слайд 129
Холинэстераза
Снижение активности холинэстеразы наблюдается при тяжелых хронических
заболеваниях печени.
Слайд 130
Холинэстераза
Повышение активности холинэстеразы наблюдается при нефротическом синдроме
(усиление синтеза альбуминов печенью из-за быстрой потери мелкодисперсной фракции
белков с мочой)Повышение холинэстеразы может наблюдаться при:
ожирении
экссудативной энтеропатии.
артериальной гипертонии,
сахарном диабете,
столбняке,
маниакально-депрессивном психозе, депрессивных неврозах, тревоге
Слайд 131
Эластаза
Эластаза-1 (панкреатическая) является протеолитическим ферментом, синтезируется в
ацинарных клетках поджелудочной железы и экскретируется в просвет двенадцатиперстной
кишки вместе с другими ферментами, в виде предшественника – проэластазы, которая активируется трипсином. Эластаза абсолютно специфична для поджелудочной железы и не определяется ни в каких других органах или тканях
Слайд 132
Эластаза
Подобно другим панкреатическим ферментам (амилаза, липаза) показатель
эластазы панкреатической начинает увеличиваться в крови в острый период
панкреатита, что позволяет поставить диагноз этого заболевания.
Слайд 133
Общие правила работы с ферментами
Нельзя сильно встряхивать растворы
ферментов и допускать образование пены при их перемешивании, т.
к. ферменты при этом могут инактивироваться в результате воздействия на них кислорода воздуха.
Слайд 134
Общие правила работы с ферментами
2. Растворенные, лиофильно высушенные
реагенты, контрольные материалы и контрольные сыворотки, содержащие ферменты, перед
использованием необходимо выдержать при комнатной температуре в течение времени, указанного в инструкции, чтобы фермент пришел в конформационно- активное состояние.Слайд 135 3. Время начала и окончания ферментативной реакции следует
фиксировать по секундомеру.
4. Температура рабочего реагента должна быть такой,
как указано в инструкции.Общие правила работы с ферментами
Слайд 136
5. Не изменять соотношение рабочий реагент/сыворотка.
6. Нельзя разбавлять
рабочий реагент.
7. Фотометрирование следует проводить в указанном в инструкции
диапазоне.Общие правила работы с ферментами
Слайд 137
8. Длина оптического пути кюветы должна соответствовать инструкции.
9.
Калибровка для каждой серии обязательна.
10. Тщательно мыть посуду, наконечники,
пипетки…Общие правила работы с ферментами
Слайд 138
11. Следить за качеством воды
12. Использовать поверенные пипетки,
особенно для микропроб.
13. Учитывать, что гемолиз завышает содержание ферментов,
а, хранение занижает.Общие правила работы с ферментами