- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему по физике на тему Электрический ток в различных средах
Содержание
- 2. Для создания электрического тока в среде необходимо
- 3. Электрический ток в жидкостях Растворы солей, кислот и
- 4. +−+−+−+−+−++−− Проводимость электролитов
- 5. Закон электролиза Закон Фарадея:
- 6. В качестве примера рассмотрим явление электролиза при
- 7.
- 8. Так как этот химический процесс протекает длительное
- 9. Применение электролиза Явление электролиза применяется на практике -
- 11. Электрический ток в металлах Опыт Р.Толмена – Т.Стю-арта
- 12. Определение скорости движения электронов в металлах.
- 13. Сопротивление проводника прямо пропорционально температуре.График зависимости удельного
- 14. Ток в металлическом проводнике увеличивает
- 15. Применение зависимости сопротивления от температурыТермометр сопротивления
- 16. Сверхпроводимость это свойство некоторых материалов обладать строго
- 17. Электрический ток в газахГазы в нормальном состоянии
- 19. Газовые разряды различают: Несамостоятельным газовым разрядом называется
- 20. Самостоятельный разряд - такой газовый разряд, в
- 21. Искровой разрядИскровой разрядвозникает между двумя электро-дами, заряжен-ными
- 22. Дуговой разряд Если после получения искрового разряда от
- 23. Применение дугового разряда:Освещение Сварка Ртутная дуга.
- 24. Коронный разряд В сильно неоднородных электрических полях, образующихся,
- 25. Применение коронного разряда Громоотвод (Подсчитано, что в
- 26. Тлеющий разряд Это разряд, возникающий при
- 27. 2. Как измениться сопротивление алюминиевого проводника при
- 28. Список использованных источников1. Применение электролиза:https://fs00.infourok.ru/images/doc/161/185478/img7.jpg2. Опыт Т.Стюарта – Р.Толмена:https://fs00.infourok.ru/images/doc/86/103927/hello_html_m5ab75448.gif3. График зависимости сопротивления:- https://ds04.infourok.ru/uploads/ex/0eea/000097a1-40f35dcb/310/img9.jpg4. Электрометр:http://edufuture.biz/images/e/e5/A16.28.jpg5. .Молния: http://thoughts-about-life.ru/wp-content/uploads/2012/02/molniya-1024x768.jpg
- 29. Скачать презентацию
- 30. Похожие презентации
Для создания электрического тока в среде необходимо : - наличие заряженных частиц в этой среде; - внешнее электрическое поле . В различных средах эти условия выполняются по


























Слайд 3
Электрический ток в жидкостях
Растворы солей, кислот и оснований,
способные проводить электрический ток, называются электролитами.
Распад молекул электролитов под
действием электрического поля называется электролитической диссоциацией.Выделение вещества на электродах показывает, что в электролитах электрические заряды переносят заряженные атомы вещества – ионы.
Этот процесс называется
электролизом.
Слайд 4
+
−
+
−
+
−
+
−
+
−
+
+
−
−
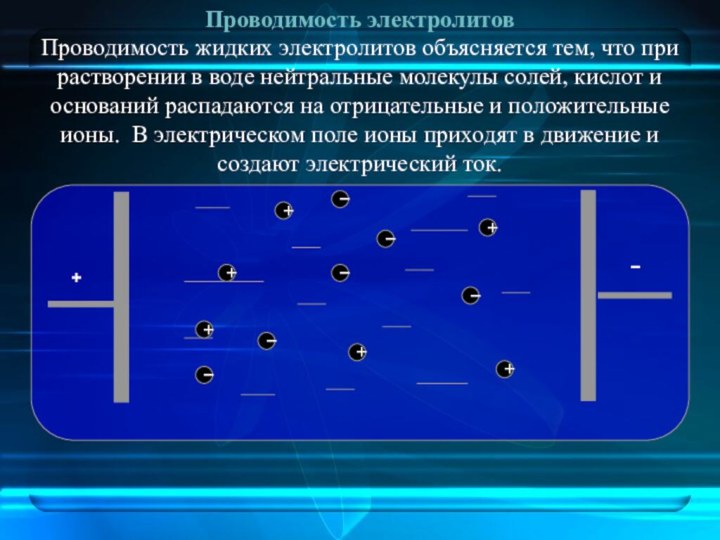
Проводимость электролитов
Проводимость жидких электролитов объясняется тем, что при
растворении в воде нейтральные молекулы солей, кислот и оснований
распадаются на отрицательные и положительные ионы. В электрическом поле ионы приходят в движение и создают электрический ток.
Слайд 5
Закон электролиза
Закон Фарадея:
масса вещества, выделившегося на
электроде за время ∆t при прохождении электрического тока, пропорциональна
силе тока и времени:m= kI∆t.
Это уравнение называется законом электролиза. Коэффициент k, зависящий от выделившегося вещества, называется электрохимическим эквивалентом вещества.
Слайд 6 В качестве примера рассмотрим явление электролиза при пропускании
электрического тока через раствор медного купороса CuSO4 с опущенными
в него медными электродами.
Слайд 8
Так как этот химический процесс протекает длительное время
( в нашем опыте – 30 минут), то на
катоде отлагается медь ( красный налёт), выделяющаяся из электролита. При этом электролит вместо ушедших на катод молекул меди получает новые молекулы меди за счет растворения второго электрода — анода.
Слайд 9
Применение электролиза
Явление электролиза применяется на практике
-
для получения многих металлов из раствора солей;
- для
защиты от окисления или для украшения - производится покрытие различных предметов и деталей машин тонкими слоями таких металлов, как хром, никель, серебро, золото;- в гальванопластике – получение отслаиваемых покрытий;
- для получения электронных плат (основ всех электронных изделий);
- для создания копий с рельефных поверхностей;
- для получения стереотипов для книг высококачественной печати.
Слайд 13
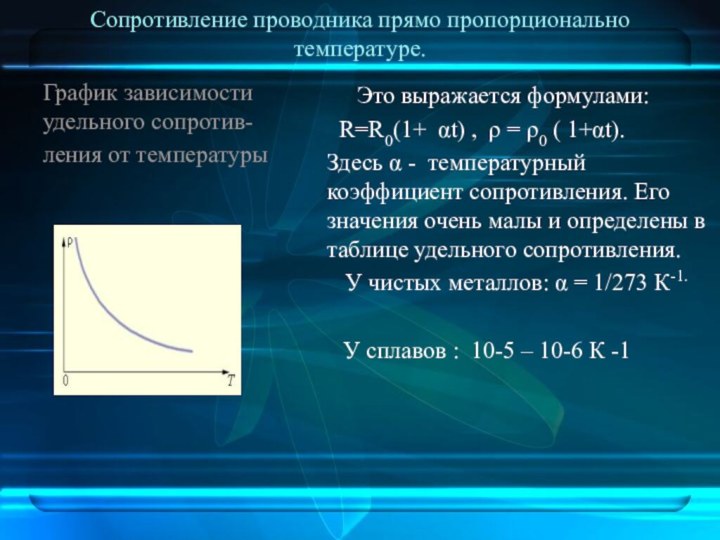
Сопротивление проводника прямо пропорционально температуре.
График зависимости удельного сопротив-
ления
от температуры
Это выражается формулами:
R=R0(1+
αt) , ρ = ρ0 ( 1+αt).Здесь α - температурный коэффициент сопротивления. Его значения очень малы и определены в таблице удельного сопротивления.
У чистых металлов: α = 1/273 К-1.
У сплавов : 10-5 – 10-6 К -1
Слайд 14 Ток в металлическом проводнике увеличивает температуру самого проводника,
в результате его длина увеличивается и проводник провисает.
Слайд 16
Сверхпроводимость
это свойство некоторых материалов обладать строго нулевым
электрическим сопротивлением при
достижении ими темпера
туры ниже определённого значения. Существует
26 чистых элементов, сплавов, переходящих в сверхпрово
дящее состояние.
Слайд 17
Электрический ток в газах
Газы в нормальном состоянии являются
диэлектриками, так как состоят из электрически нейтральных атомов и
молекул и поэтому не проводят электричества.Проводниками могут быть только ионизированные газы,
в которых содержатся электроны, положительные и отрицательные ионы.
В этом случае среде необходим внешний ионизатор.
Роль такого ионизатора играют нагревание и излучение.
Прохождение электрического тока через газы называют газовым разрядом.
Слайд 19
Газовые разряды различают:
Несамостоятельным газовым разрядом называется такой
разряд, который, возникнув при наличии электрического поля, может существовать
только под действием внешнего ионизатора.
Слайд 20
Самостоятельный разряд - такой газовый разряд, в котором
носители тока возникают в результате тех процессов в газе,
которые обусловлены приложенным к газу напряжением.Т. е. данный разряд продолжается и после прекращения действия ионизатора.
Разновидности такого разряда:
- искровой;
- дуговой;
- коронный;
- тлеющий.
Слайд 21
Искровой разряд
Искровой разряд
возникает между двумя электро-дами, заряжен-ными разными
зарядами и име-ющие большую разность потен-циалов. Он кра-тковременный, его
механизм - электронный удар.Молния - вид искрового разряда.
Слайд 22
Дуговой разряд
Если после получения искрового разряда от мощного
источ-ника постепенно уменьшать расстояние между электродами, то разряд из
прерывистого становится непрерывным возни-кает новая форма газового разряда, называемая дуговым разрядом.
Слайд 24
Коронный разряд
В сильно неоднородных электрических полях, образующихся, например,
между острием и плоскостью или между проводом линии электропередачи
и поверхностью Земли, возникает особая форма самостоятельного разряда в газах,называемая коронным разрядом.
Слайд 25
Применение коронного разряда
Громоотвод (Подсчитано, что в атмосфере
всего земного шара происходит одновременно около 1800 гроз, которые
дают в среднем около 100 молний в секунду. Поэтому, защита от молнии представляет собой важную задачу).
Слайд 26
Тлеющий разряд
Это разряд, возникающий при пониженном давлении.
При понижении давления увеличивается длина свободного пробега электрона,
и за время между столкновениями он успевает приобрести достаточную для ионизации энергию в электрическом поле с меньшей напряженностью. Разряд осуществляется электронно-ионной лавиной.Гелий Неон Ксенон
Слайд 27 2. Как измениться сопротивление алюминиевого проводника при охлаждении
от 0°С до -125°С?
3. Электроды, опущенные в раствор медного
купороса, соединены с источником тока, ЭДС которого 12 В ивнутреннее сопротивление 0,2 Ом. Сопротивление раствора между электродами 0,4 Ом. Сколько меди
выделиться за 5 мин?
4. При никелировании изделия на катоде за 30 мин отложился никель массой 18г. Определите силу тока при
электролизе, если молярная масса никеля 0,0587 кг/моль, а валентность n=2.
5. При покрытии изделий золотом используют ток плотность которого 40 А/м². Какой толщины слой золота можно
получить, пропуская ток в течение 2ч.
6. Какой наименьшей скоростью должен обладать электрон для того, чтобы ионизировать атом водорода?
Потенциал ионизации водорода равен 13,5 В