- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Биотехнология игенетическая инженерия
Содержание
- 2. Биотехнология – совокупность методов естественных и
- 3. Генетической инженерией называют прикладную молекулярную и
- 4. Разделы биотехнологии:Генетическая инженерия – технологии основаны на
- 5. К генетической инженерии принято относить следующие
- 7. Ферменты, используемые в генной инженерии. Рестриктазы (рестрикционные
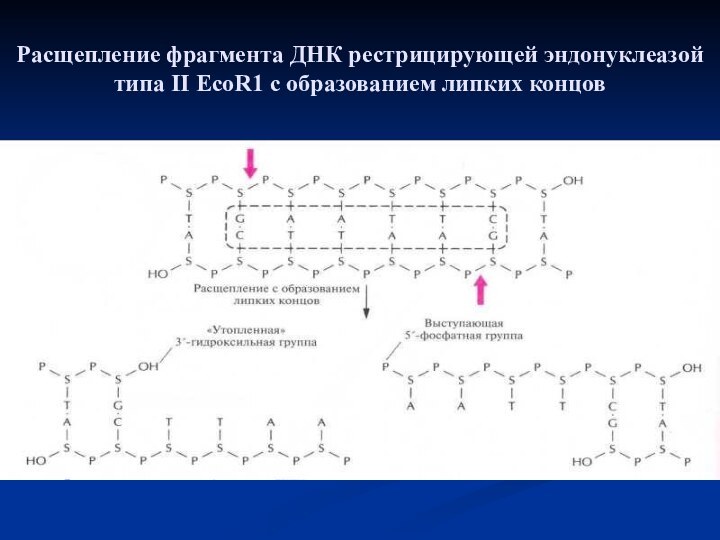
- 8. Расщепление фрагмента ДНК рестрицирующей эндонуклеазой типа II EcoR1 с образованием липких концов
- 9. Схема действия рестриктазы EcoR 1
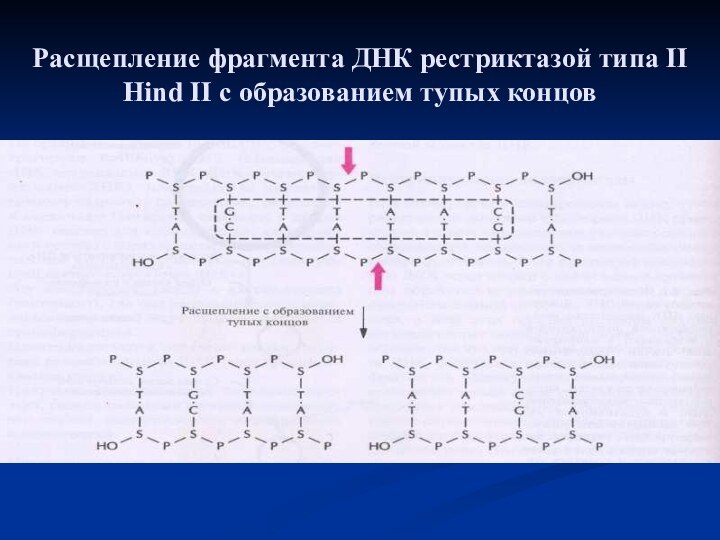
- 10. Расщепление фрагмента ДНК рестриктазой типа II Hind II с образованием тупых концов
- 11. Нуклеотидные последовательности, распознаваемые некоторыми ферментами рестрикции
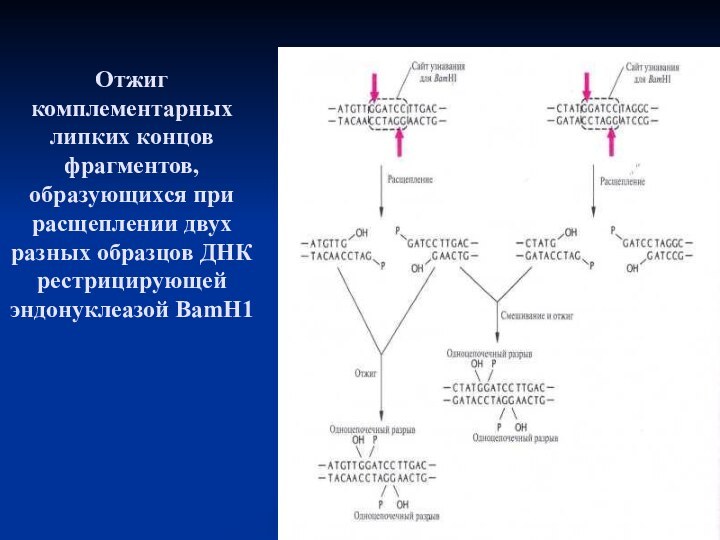
- 12. Отжиг комплементарных липких концов фрагментов, образующихся при расщеплении двух разных образцов ДНК рестрицирующей эндонуклеазой BamH1
- 13. Синтез и выделение фрагментов ДНК
- 14. Схема ферментативного синтеза гена с помощью обратной транскрипции
- 15. Структура химически синтезированного Хораной функционально активного отрезка
- 16. Синтез кДНКСинтез кДНК. К препарату очищенной мРНК
- 17. Синтез кДНК
- 18. Выделение фрагментов ДНК, содержащих нужный ген
- 19. Векторы в генной инженерии. Для осуществления трансгеноза
- 20. Генетическая карта плазмидного вектора pBR322
- 21. Генетическая карта плазмидного вектора pUC19Плазмида состоит из
- 22. Встраивание чужеродной ДНК в плазмидный вектор
- 23. Ферментативный синтез гена и встраивание его в векторную плазмиду
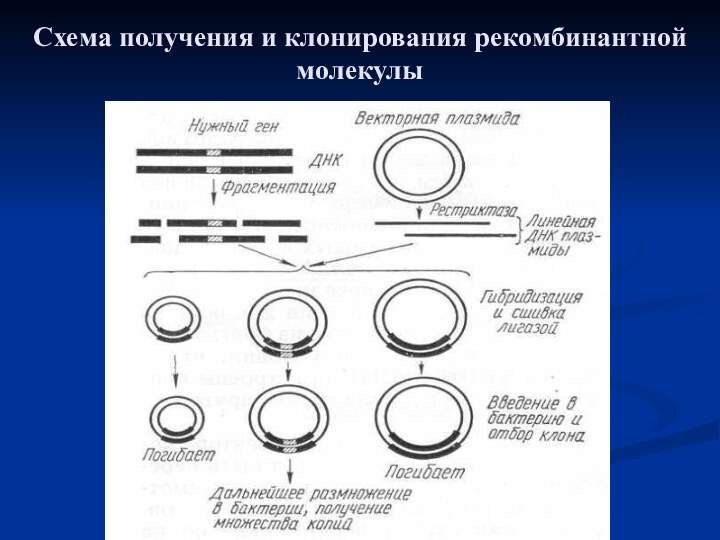
- 24. Схема получения и клонирования рекомбинантной молекулы
- 25. Интеграция чужеродной ДНК в хромосому хозяинаПроцесс интеграции
- 26. Два способа интеграции клонированного в плазмиде гена
- 27. Встраивание чужеродного гена в заранее выбранный сайт
- 28. «Нокаут» гена с помощью направленной гомологичной рекомбинации.
- 29. Векторы для клонирования крупных фрагментов ДНКЛитический путь
- 30. Клонирующая система на основе бактериофага λ.
- 31. Клонирующая система на основе бактериофага λ
- 32. Лигирование липких и тупых концов в молекуле
- 33. Клонирование с помощью космидного вектора Космида имеет
- 34. Клонирование с помощью космидного вектора
- 35. Перенос генов с помощью искусственных дрожжевых хромосом
- 36. Идентификация клеток, несущих трансген
- 39. Методы получения трансгенных животных:1. Метод микроиньекции2. Вирусный метод 3. Эмбриональный метод
- 40. Метод микроиньекцииУ самок вызывают гиперовуляцию после чего
- 41. Получение линий трансгенных мышей методом микроинъекций. Яйцеклетки
- 42. Метод микроинъекций ДНКУвеличение числа яйцеклеток, в которых
- 43. Вирусный методЭмбрион, находящийся на стадии 8 клеток,
- 44. Получение трансгенных мышей с использованием ретровирусных векторовПолучение
- 45. Эмбриональный методЭмбриональные стволовые клетки получают из внутренней
- 46. ES-клетки получают из внутренней клеточной массы
- 47. Использование модифицированных эмбриональных стволовых клетокКлетки, выделенные из
- 48. Трансгенные животные
- 49. Стратегия по введению чужеродных генов в клетки
- 50. Клонирование овцы методом переноса ядраКлонирование овцы методом
- 51. Клонирование овечки Долли
- 52. Трансгенный крупный рогатый скотЕсли предполагается использовать молочную
- 53. Для создания трансгенных коров использовали модифицированную схему
- 54. Получение трансгенных коров
- 55. Трансгенные овцы, козы и свиньи
- 56. Трансгенные птицыМикроинъекция ДНК в оплодотворенные яйцеклетки птиц
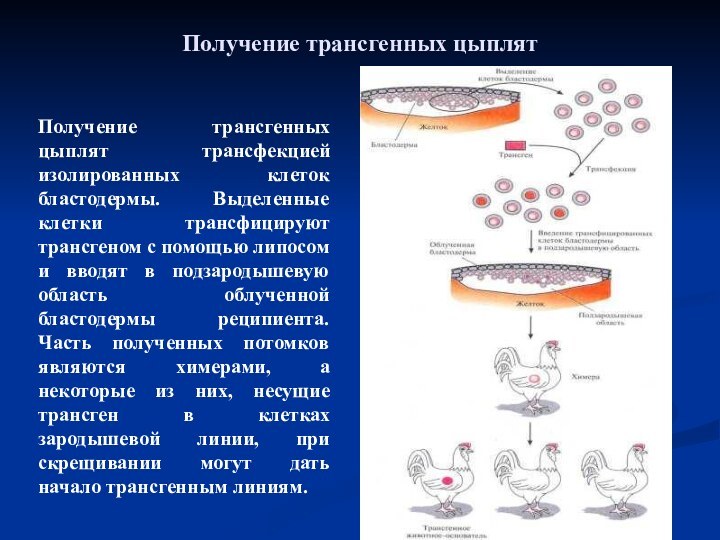
- 57. Получение трансгенных цыплят трансфекцией изолированных клеток бластодермы.
- 58. Трансгенные рыбыПо мере истощения природных рыбных запасов
- 59. Трансгенные мыши: методологияВведение чужеродной ДНК мышам можно
- 60. Трансгенные мыши: применение как модельного обьекта изучения
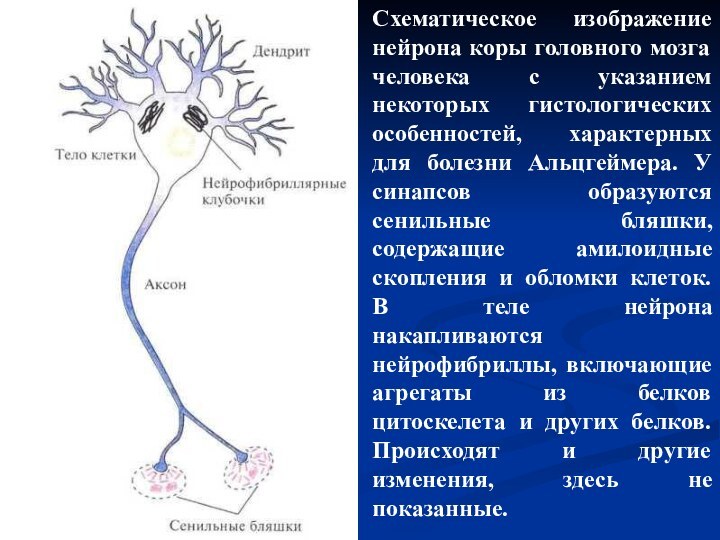
- 61. Схематическое изображение нейрона коры головного мозга человека
- 62. Основным компонентом сенильных и амилоидных бляшек является
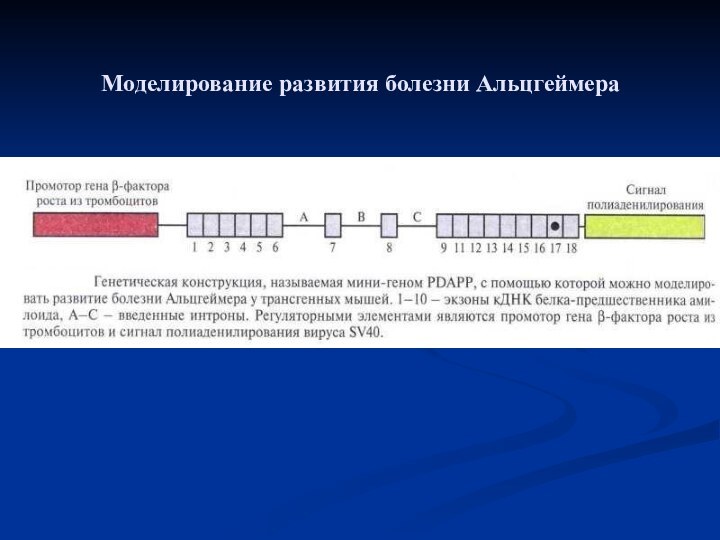
- 63. Моделирование развития болезни Альцгеймера
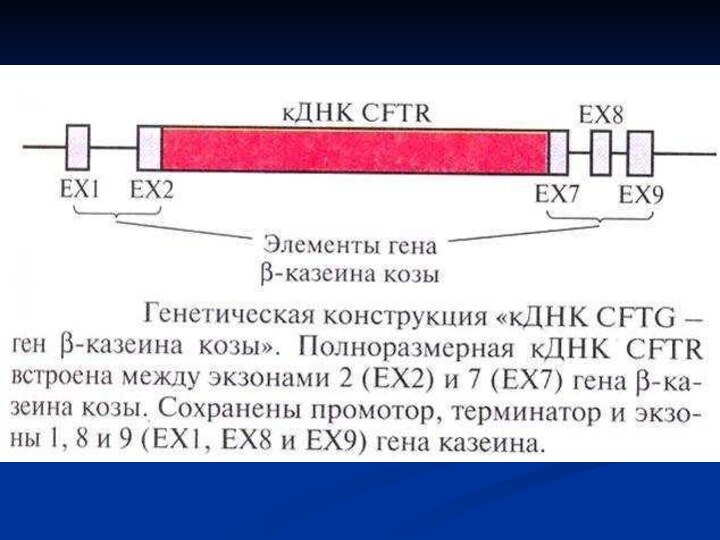
- 64. Муковисцидоз — распространенная генетическая болезнь, поражающая в
- 66. Гибридизация соматических клеток
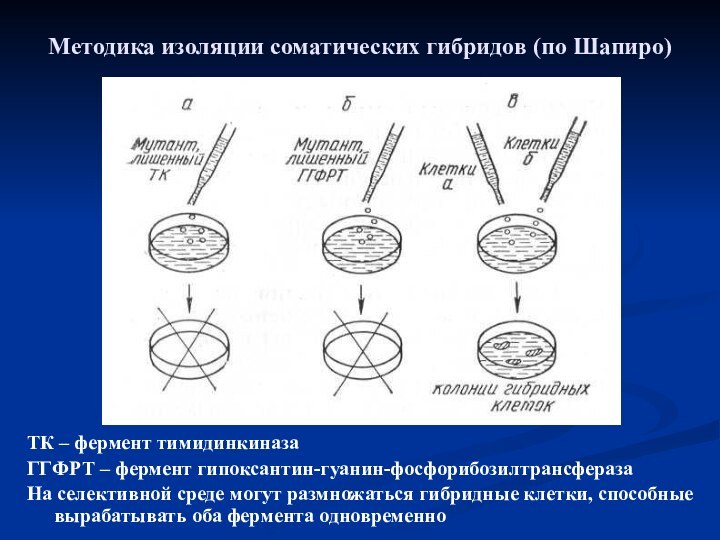
- 67. Методика изоляции соматических гибридов (по Шапиро)ТК –
- 68. Некоторые сочетания геномов, полученные слиянием соматических клеток
- 69. Скачать презентацию
- 70. Похожие презентации
Биотехнология – совокупность методов естественных и инженерных наук, использующих свойства биологических систем различного уровня организации в технологических процессах.





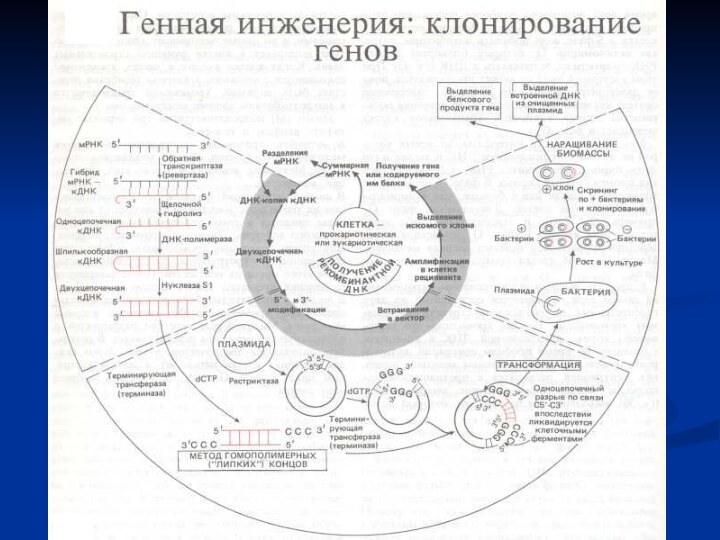




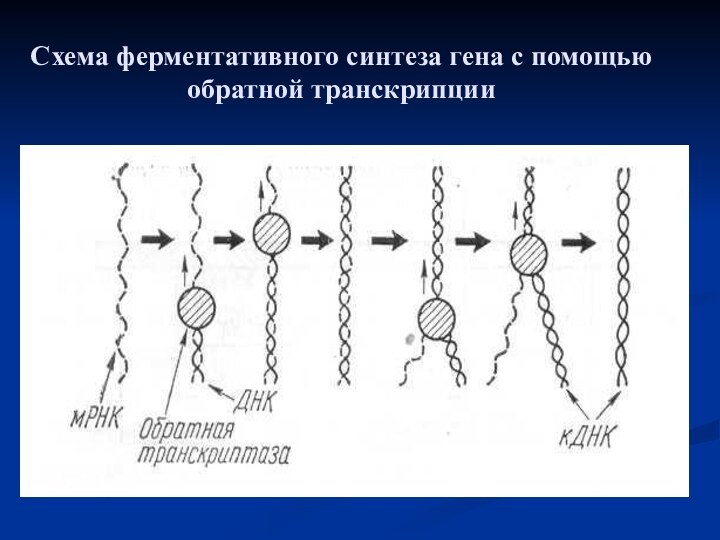





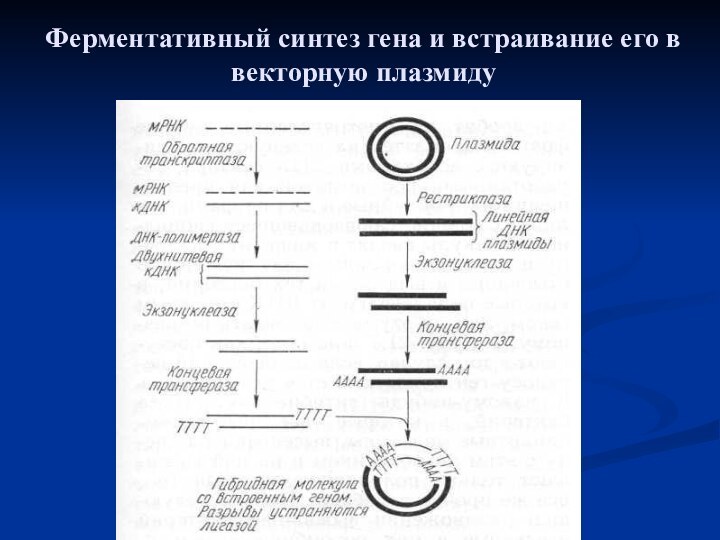


























Слайд 3 Генетической инженерией называют прикладную молекулярную и клеточную
генетику, разрабатывающую приемы экспериментального вмешательства, позволяющие по заранее намеченному
плану перестраивать геном организмов, изменяя содержащуюся в нем наследственную (генетическую) информацию.В понятие генетической инженерии не включают перестройку геномов обычными генетическими методами, т.е. искусственным вызыванием мутаций и получением рекомбинаций путем скрещивания.
Слайд 4
Разделы биотехнологии:
Генетическая инженерия – технологии основаны на получении
гибридных молекул ДНК и введении их в клетки бактерий,
растений и животных.Клеточная инженерия – технологии основаны на возможности выращивания тканей и клеток in vitro, слиянии соматических клеток или их протопластов.
Биологическая инженерия – технологии основаны на изучении биологических особенностей клеток и внедрении компьютерных методов контроля технологических режимов, позволяющих максимально реализовывать полезные свойства клеток.
Слайд 5
К генетической инженерии принято относить следующие операции:
1.
синтез генов вне организма;
2. выделение из клеток отдельных генов
или генетических структур (фрагментов хромосом, целых хромосом или даже целых клеточных ядер);3. направленную перестройку выделенных структур;
4. копирование и размножение выделенных или синтезированных генов или генетических структур;
5. перенос и включение таких генов или генетических структур в подлежащий изменению геном;
6. экспериментальное соединение разных геномов в одной клетке.
Слайд 7
Ферменты, используемые в генной инженерии.
Рестриктазы (рестрикционные нуклеазы)
– ферменты, способные узнавать специфические последовательности ДНК (4-6 нуклеотидов)
и расщепляющие их в строго определённых местах.Ревертаза (РНК-зависимая ДНК-полимераза) – фермент, синтезирующий ДНК по матрице РНК.
Нуклеазы – большой класс ферментов, расщепляющих молекулы нуклеиновых кислот; имеются нуклеазы, расщепляющие одно- или двуцепочечные ДНК или РНК путём отщепления по одному нуклеотиду или небольших олигонуклеотидов.
Терминальная трансфераза – наращивает на концах фрагментов ДНК однонитевые участки путём последовательного присоединения нуклеотидов; используется для создания на соединяемых фрагментах ДНК «липких» концов.
Слайд 8 Расщепление фрагмента ДНК рестрицирующей эндонуклеазой типа II EcoR1
с образованием липких концов
Слайд 12 Отжиг комплементарных липких концов фрагментов, образующихся при расщеплении
двух разных образцов ДНК рестрицирующей эндонуклеазой BamH1
Слайд 15 Структура химически синтезированного Хораной функционально активного отрезка ДНК
кишечной палочки
Цифры – нумерация нуклеотидов:
промотор от -52 до -1
ген
супрессорной тирозиновой тРНК от 1 до 125 терминатор от 127 до 146
на концах отрезка тетрануклеотиды ААТТ и ТТАА
Слайд 16
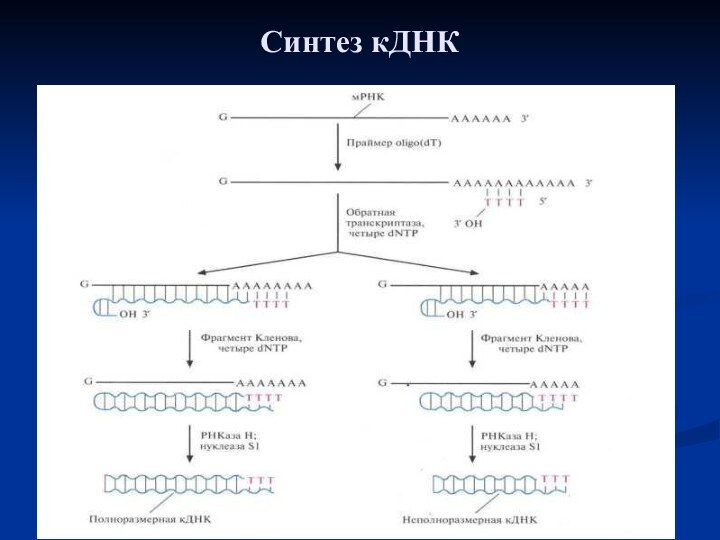
Синтез кДНК
Синтез кДНК. К препарату очищенной мРНК добавляют
праймер oligo(dT). Для синтеза ДНК на РНК-матрице используют фермент
обратную транскриптазу и четыре dNTP. In vitro обратная транскриптаза не обеспечивает синтез полноразмерных кДНК-копий на всех матрицах и образует на конце растущей цепи шпильку со свободной 3'-ОН-группой. Эта группа инициирует синтез второй цепи ДНК при участии фрагмента Клёнова. После завершения синтеза молекулы мРНК гидролизуют РНКазойН, а ДНК обрабатывают нуклеазой S1, в результате чего получаются линейные молекулы ДНК с тупыми концами без шпилек.
Слайд 19
Векторы в генной инженерии.
Для осуществления трансгеноза (введения
чужеродных генов в клетку реципиента) используются вектоы (переносчики). Векторы
– это своеобразные молекулярные такси способные самостоятельно проникать в клетку-мишень, встраиваться в ДНК и в ней реплицироваться. В качестве векторов используют ДНК фага или бактериальные плазмиды.
Слайд 21
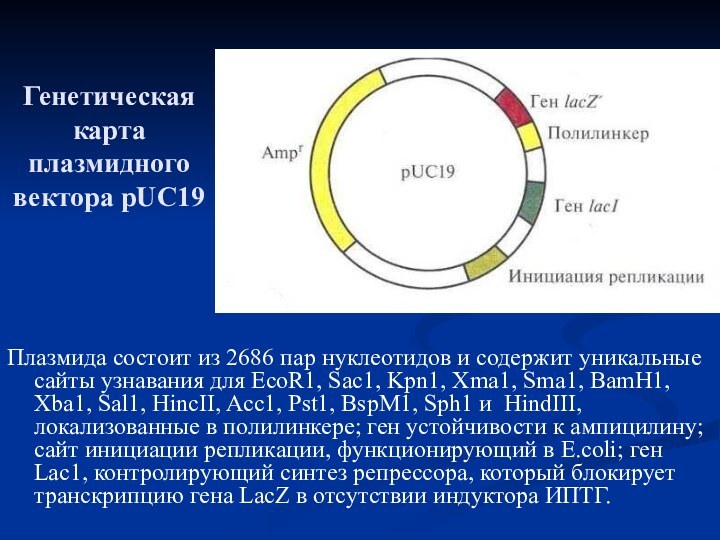
Генетическая карта плазмидного вектора pUC19
Плазмида состоит из 2686
пар нуклеотидов и содержит уникальные сайты узнавания для EcoR1,
Sac1, Kpn1, Xma1, Sma1, BamH1, Xba1, Sal1, HincII, Acc1, Pst1, BspM1, Sph1 и HindIII, локализованные в полилинкере; ген устойчивости к ампицилину; сайт инициации репликации, функционирующий в E.coli; ген Lac1, контролирующий синтез репрессора, который блокирует транскрипцию гена LacZ в отсутствии индуктора ИПТГ.
Слайд 22
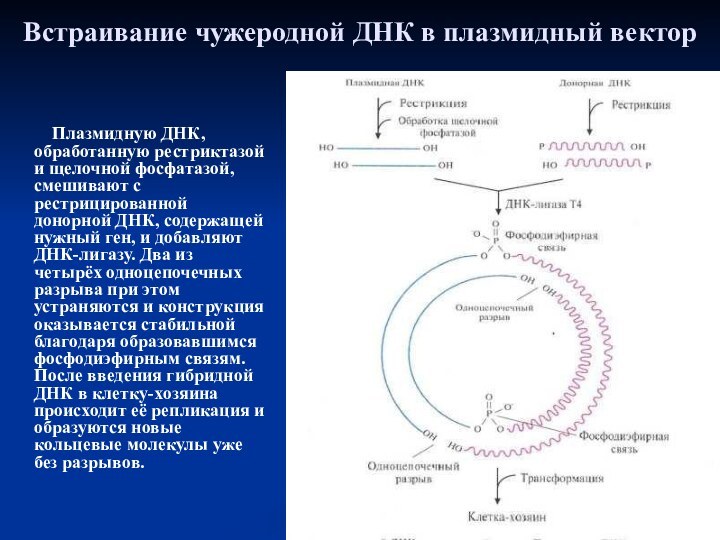
Встраивание чужеродной ДНК в плазмидный вектор
Плазмидную ДНК, обработанную рестриктазой и щелочной фосфатазой,
смешивают с рестрицированной донорной ДНК, содержащей нужный ген, и добавляют ДНК-лигазу. Два из четырёх одноцепочечных разрыва при этом устраняются и конструкция оказывается стабильной благодаря образовавшимся фосфодиэфирным связям. После введения гибридной ДНК в клетку-хозяина происходит её репликация и образуются новые кольцевые молекулы уже без разрывов.
Слайд 25
Интеграция чужеродной ДНК в хромосому хозяина
Процесс интеграции состоит
в следущем:
Идентификация подходящего сайта интеграции, т. е. сегмента хозяйской
ДНК, последовательность которого может быть прервана без ущерба для функционирования клетки. Выделение и клонирование всего хромосомного сайта интеграции или его части.
Встраивание нужного гена вместе с регулируемым промотором в клонированный сайт интеграции или вблизи него.
Перенос полученной генетической конструкции «хромосомный сайт интеграции/клонированный ген» в хозяйскую клетку в составе плазмиды, не способной к автономной репликации в клетках этого хозяина.
Отбор и сохранение тех хозяйских клеток, которые экспрессируют клонированный ген. Наследование клонированного гена возможно только в случае его интеграции в хромосому клеток хозяина.
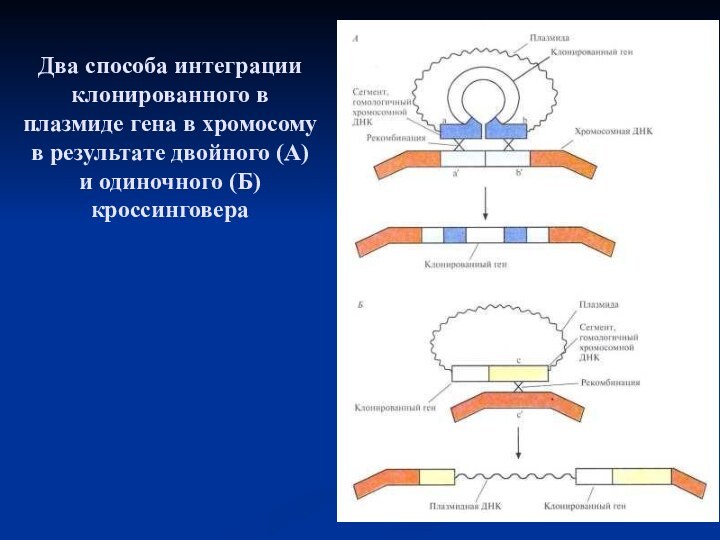
Слайд 26 Два способа интеграции клонированного в плазмиде гена в
хромосому в результате двойного (А) и одиночного (Б) кроссинговера
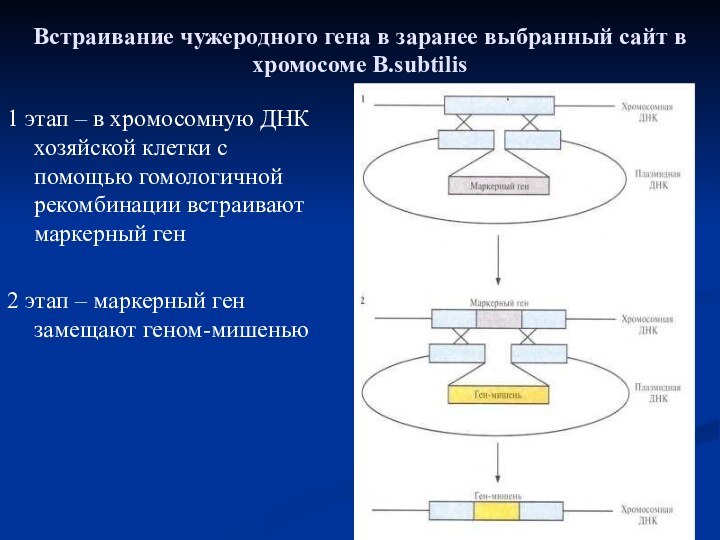
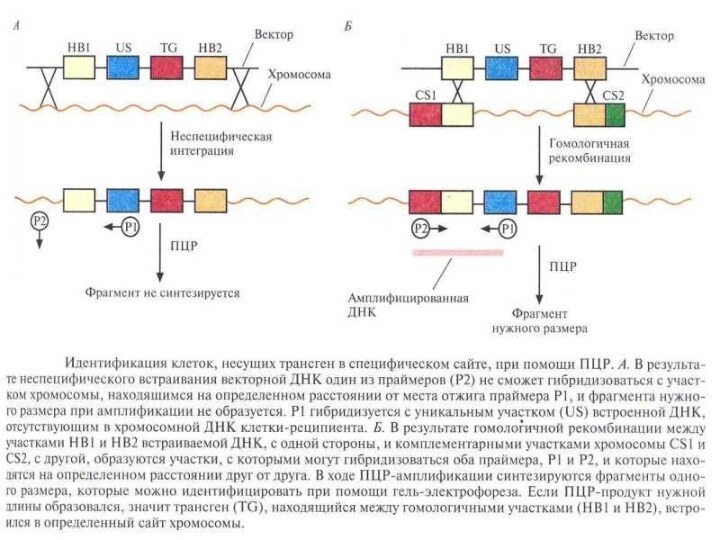
Слайд 27 Встраивание чужеродного гена в заранее выбранный сайт в
хромосоме B.subtilis
1 этап – в хромосомную ДНК хозяйской клетки
с помощью гомологичной рекомбинации встраивают маркерный ген2 этап – маркерный ген замещают геном-мишенью
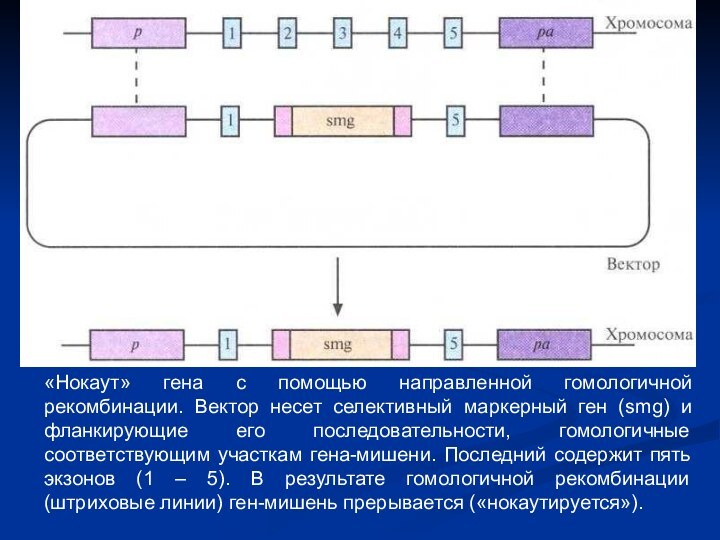
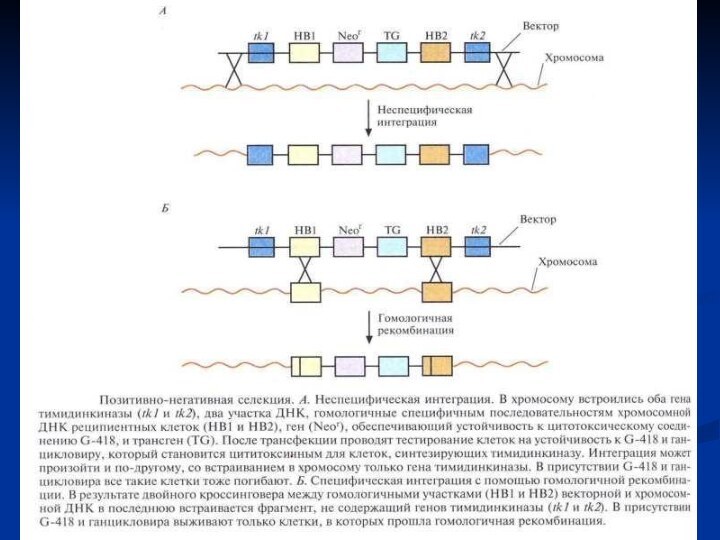
Слайд 28 «Нокаут» гена с помощью направленной гомологичной рекомбинации. Вектор
несет селективный маркерный ген (smg) и фланкирующие его последовательности,
гомологичные соответствующим участкам гена-мишени. Последний содержит пять экзонов (1 – 5). В результате гомологичной рекомбинации (штриховые линии) ген-мишень прерывается («нокаутируется»).
Слайд 29
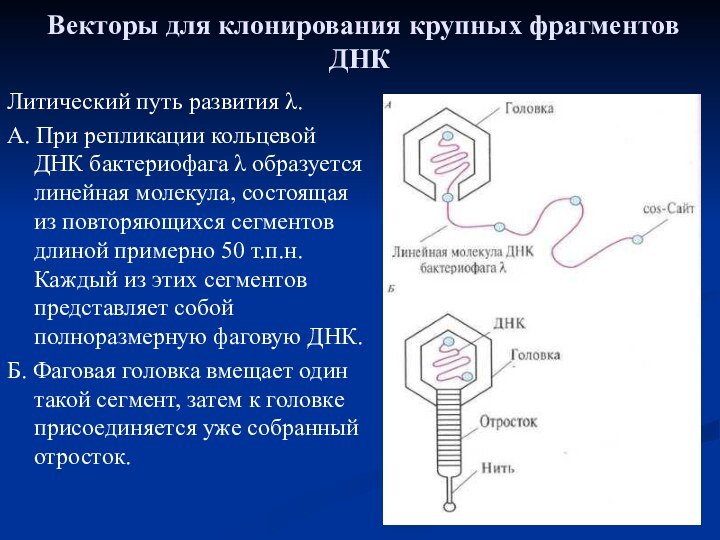
Векторы для клонирования крупных фрагментов ДНК
Литический путь развития
λ.
А. При репликации кольцевой ДНК бактериофага λ образуется
линейная молекула, состоящая из повторяющихся сегментов длиной примерно 50 т.п.н. Каждый из этих сегментов представляет собой полноразмерную фаговую ДНК.Б. Фаговая головка вмещает один такой сегмент, затем к головке присоединяется уже собранный отросток.
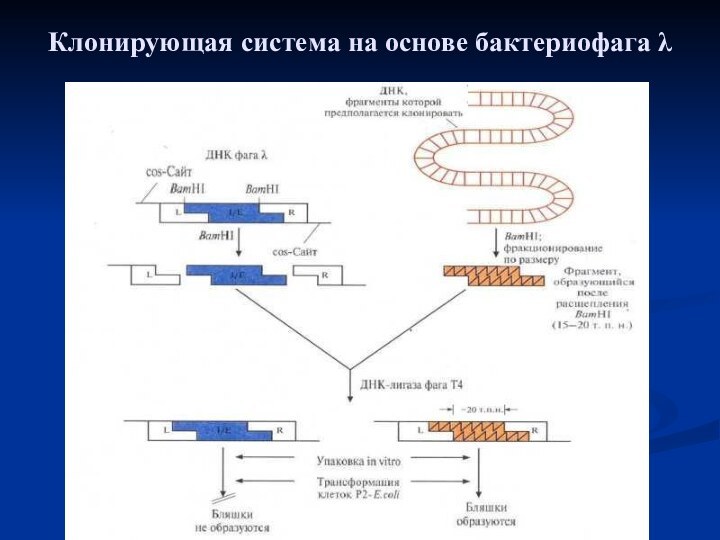
Слайд 30 Клонирующая система на основе бактериофага λ.
Фаговая ДНК имеет два BamH1-сайта, фланкирующих её I/E-сегмент. Клонируемую
ДНК расщепляют с помощью BamH1, фракционируют полученные фрагменты по размеру и выделяют из них те, которые имеют размер от 15 до 20т.п.н. Фаговую ДНК обрабатывают этим же ферментом. Оба препарата ДНК смешивают и обрабатывают ДНК-лигазой фага Т4. Лигированная смесь содержит самые разные комбинации ДНК, в том числе (1) восстановленную ДНК фага λ и (2) рекомбинантные молекулы, содержащие R- и L-области фаговой ДНК и вставку клонируемой ДНК размером ≈ 20 т.п.н., занявшую место области I/E фагового генома. Рекомбинантные молекулы упаковывают в головки бактерифага λ in vitro, и после добавления отростков получают инфекционные фаговые частицы. В инфицированных рекомбинантным фагом клетках E.coli, в хромосому которых интегрирована ДНК бактериофага Р2, могут реплицироваться и образовывать инфекционные частицы только молекулы ДНК, составленные из R- и L-областей фаговой ДНК и клонированной вставки размером ≈ 20 т.п.н.Слайд 32 Лигирование липких и тупых концов в молекуле ДНК
фагом Т4
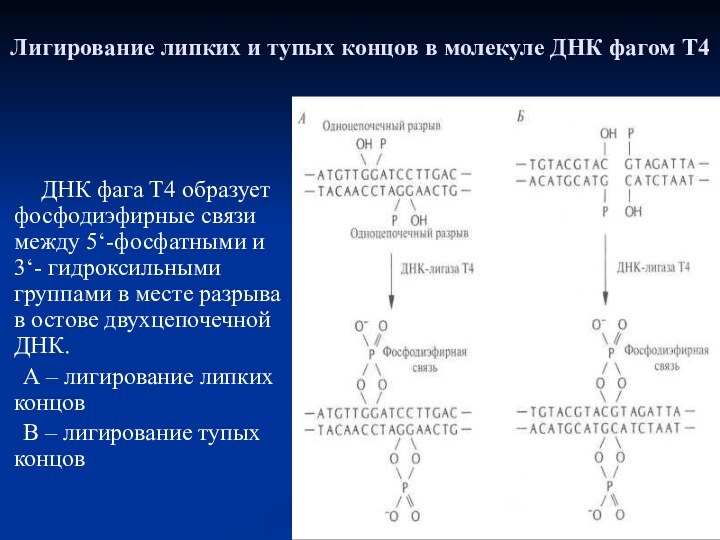
ДНК фага Т4
образует фосфодиэфирные связи между 5‘-фосфатными и 3‘- гидроксильными группами в месте разрыва в остове двухцепочечной ДНК.А – лигирование липких концов
В – лигирование тупых концов
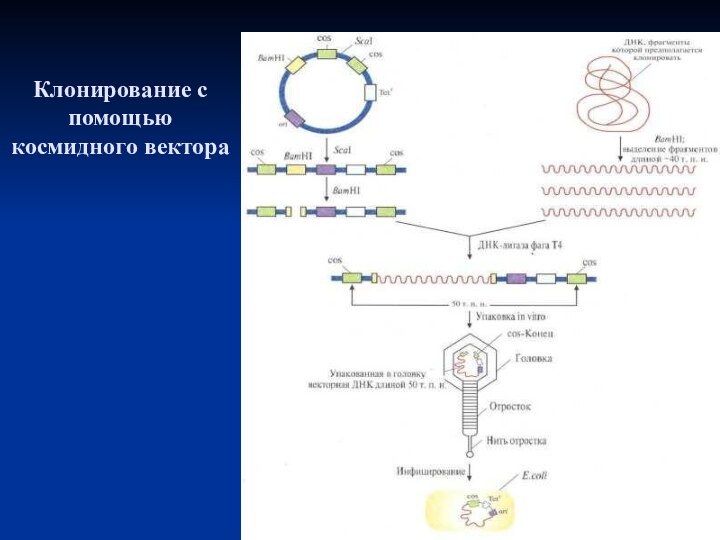
Слайд 33
Клонирование с помощью космидного вектора
Космида имеет точку
начала репликации (ori), обеспечивающую её существование в E.coli в
виде плазмиды;два интактных соs-конца, разделённых уникальным сайтом для Sca1; BamH1-сайт вбдизи одного из соs-сайтов и ген устойчивости к тетрациклину (Теtr). ДНК, которую хотят клонировать, расщепляют рестриктазой BamH1 и фракционируют по размеру,чтобы выделить молекулы длиной примерно 40 т.п.н. Плазмидную ДНК расщепляют с помощью Sca1 и BamH1. Оба препарата ДНК смешивают и обрабатывают ДНК-лигазой фага Т-4. Некоторые из гибридных молекул, образовавшихся после лигирования, содержат вставку размером около 40 т.п.н., так что их суммарная длина составляет примерно 50 т.п.н. Эти молекулы упаковываются in vitro в головки бактериофага λ, затем к головкам прикрепляются отростки, и образуются инфекционные частицы. При инфицировании этим фагом E.coli в бактериальной клетке оказывается линейная молекула ДНК с cos-концами, которые спариваются друг с другом. ДНК-лигаза клетки-хозяина зашивает одноцепочечные разрывы, и образовавшаяся кольцевая молекула существует в клетке-хозяине как автономно реплицирующаяся единица. Трансформированные клетки можно идентифицировать по признаку устойчивости к тетрациклину.
Слайд 39
Методы получения трансгенных животных:
1. Метод микроиньекции
2. Вирусный метод
3. Эмбриональный метод
Слайд 40
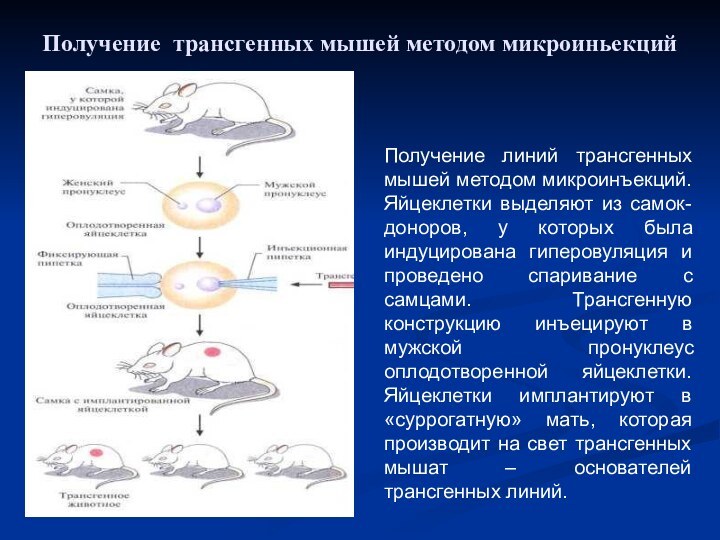
Метод микроиньекции
У самок вызывают гиперовуляцию после чего проводят
спаривание с самцами. Из самок-доноров выделяют яйцеклетки.В мужской пронуклеус
оплодотворённой яйцеклетки иньецируют трансгенную конструкцию. Яйцеклетки имплантируют «суррогатной» матери, которая производит на свет мышей – основателей трансгенной линии.Слайд 41 Получение линий трансгенных мышей методом микроинъекций. Яйцеклетки выделяют
из самок-доноров, у которых была индуцирована гиперовуляция и проведено
спаривание с самцами. Трансгенную конструкцию инъецируют в мужской пронуклеус оплодотворенной яйцеклетки. Яйцеклетки имплантируют в «суррогатную» мать, которая производит на свет трансгенных мышат – основателей трансгенных линий.Получение трансгенных мышей методом микроиньекций
Слайд 42
Метод микроинъекций ДНК
Увеличение числа яйцеклеток, в которых будет
инъецирована чужеродная ДНК, путем стимуляции гиперовуляции у самок-доноров. Сначала
самкам вводят сыворотку беременной кобылы, а спустя примерно 48 ч — хорионический гонадотропин человека. В результате гиперовуляции образуется примерно 35 яйцеклеток вместо обычных 5—10.Скрещивание с самцами самок с гиперовуляцией и их умерщвление. Вымывание из яйцеводов оплодотворенных яйцеклеток.
Микроинъекция ДНК в оплодотворенные яйцеклетки - как правило, сразу после выделения. Часто вводимая трансгенная конструкция находится в линейной форме и не содержит прокариотических векторных последовательностей.
Слайд 43
Вирусный метод
Эмбрион, находящийся на стадии 8 клеток, инфицируют
рекомбинантным ретровирусом, несущим трансген. Самки, которым был имплантирован эмбрион,
производят на свет трансгенное потомство. Для идентификации мышей, несущих трансген в клетках зародышевой линии, проводят ряд скрещиваний.
Слайд 44
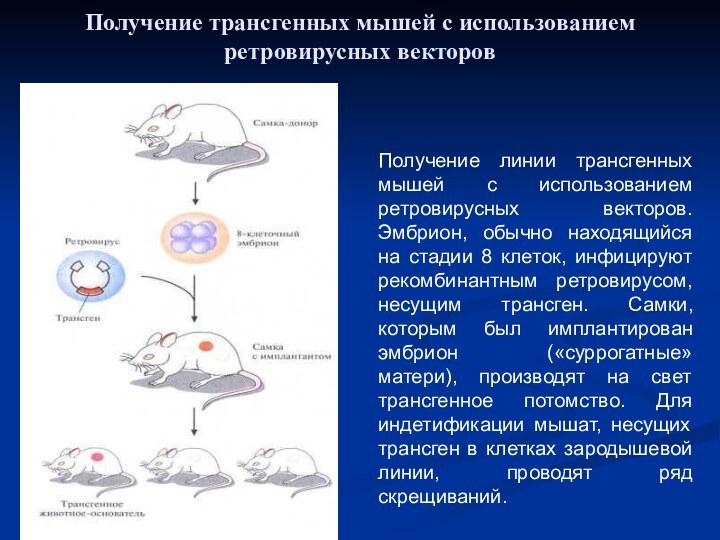
Получение трансгенных мышей с использованием ретровирусных векторов
Получение линии
трансгенных мышей с использованием ретровирусных векторов. Эмбрион, обычно находящийся
на стадии 8 клеток, инфицируют рекомбинантным ретровирусом, несущим трансген. Самки, которым был имплантирован эмбрион («суррогатные» матери), производят на свет трансгенное потомство. Для индетификации мышат, несущих трансген в клетках зародышевой линии, проводят ряд скрещиваний.
Слайд 45
Эмбриональный метод
Эмбриональные стволовые клетки получают из внутренней клеточной
массы бластоцисты мыши. Их трансфицируют вектором, несущим трансген, культивируют.
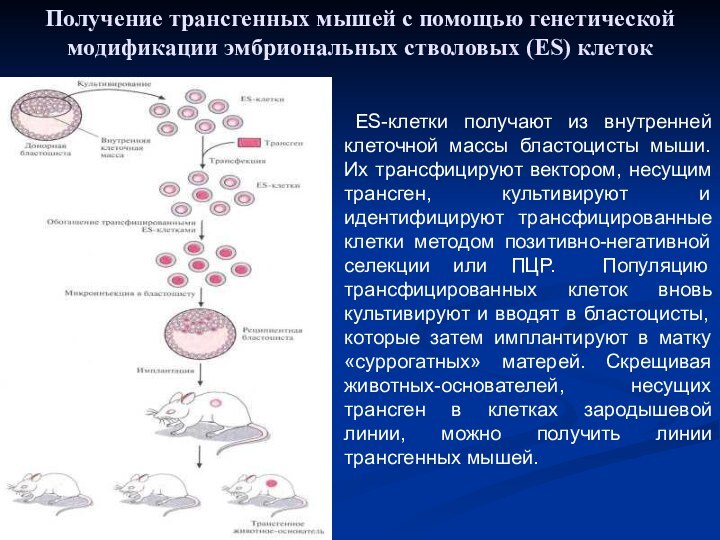
Трансфицированные клетки идентифицируют методом позитивно-негативной селекции (ПЦР). Популяцию трансфицированных клеток вновь культивируют и вводят в бластоцисты, которые затем имплантируют в матку «суррогатной» матери. Скрещивая животных-основателей, несущих трансген в клетках зародышевой линии, можно получить трансгенных мышей.Слайд 46 ES-клетки получают из внутренней клеточной массы бластоцисты
мыши. Их трансфицируют вектором, несущим трансген, культивируют и идентифицируют
трансфицированные клетки методом позитивно-негативной селекции или ПЦР. Популяцию трансфицированных клеток вновь культивируют и вводят в бластоцисты, которые затем имплантируют в матку «суррогатных» матерей. Скрещивая животных-основателей, несущих трансген в клетках зародышевой линии, можно получить линии трансгенных мышей.Получение трансгенных мышей с помощью генетической модификации эмбриональных стволовых (ES) клеток
Слайд 47
Использование модифицированных эмбриональных стволовых клеток
Клетки, выделенные из мышиных
эмбрионов на стадии бластоцисты, могут пролиферировать в культуре, сохраняя
способность к дифференцировке в любые типы клеток, в том числе и в клетки зародышевой линии, при введении в другой эмбрион на стадии бластоцисты. Такие клетки называются плюрипотентными эмбриональными стволовыми клетками (ES). ES-клетки в культуре легко модифицировать методами генной инженерии без нарушения их плюрипотентности. Например, в определенный сайт несущественного гена в их геноме можно встроить функциональный трансген. Затем можно отобрать измененные клетки, культивировать их и использовать для получения трансгенных животных. Это позволяет избежать случайного встраивания, характерного для метода микроинъекций и ретровирусных векторных систем.Слайд 49 Стратегия по введению чужеродных генов в клетки млекопитающих
состоит в следующем:
Клонированный ген вводят в ядро оплодотворенной яйцеклетки.
Инокулированные оплодотворенные яйцеклетки имплантируют в реципиентную женскую особь (поскольку успешное завершение развития эмбриона млекопитающих в иных условиях невозможно).
Отбирают потомков, развившихся из имплантированных яйцеклеток, которые содержат клонированный ген во всех клетках.
Скрещивают животных, которые несут клонированный ген в клетках зародышевой линии, и получают новую генетическую линию.
Слайд 50
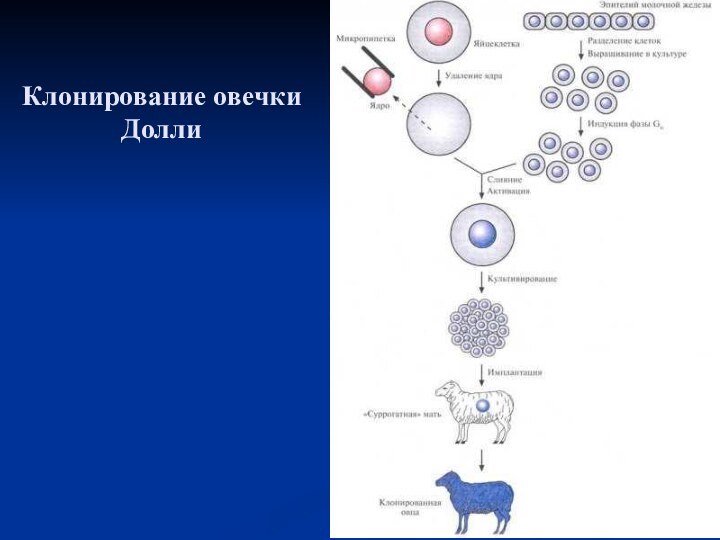
Клонирование овцы методом переноса ядра
Клонирование овцы методом переноса
ядра. Ядро яйцеклетки удаляют с помощью микропипетки. Культивируют эпителиальные
клетки молочной железы взрослой особи и индуцируют их переход в фазу G0. Осуществляют слияние клеток в G0-фазе и яйцеклеток, лишенных ядра, и выращивают восстановленные яйцеклетки в культуре или в яйцеводе с наложенной лигатурой до ранних стадий эмбриогенеза, а затем имплантируют их в матку «суррогатной» матери, где и происходит дальнейшее развитие. В эксперименте, описанном Уилмутом и др. (1997), было проведено слияние 277 яйцеклеток с удаленными ядрами с клетками молочной железы в фазе G0; из 29 эмбрионов только один развился до жизнеспособного плода.
Слайд 52
Трансгенный крупный рогатый скот
Если предполагается использовать молочную железу
в качестве «биореактора», то наиболее предпочтительным животным для трансгеноза
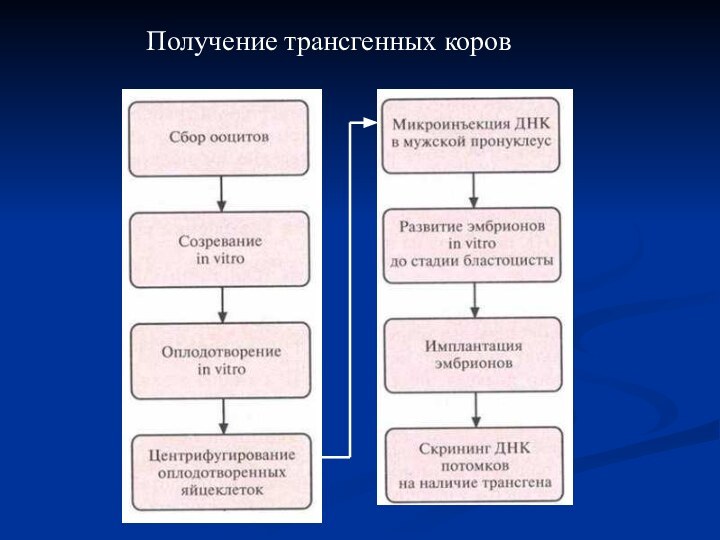
является крупный рогатый скот, который ежегодно дает до 10 000 л молока, содержащего примерно 35 г белка на 1 л. Если в молоке будет содержаться такое количество рекомбинантного белка и эффективность его очистки составит 50%, то от 20 трансгенных коров можно будет получать примерно 100 кг такого белка в год. По случайному совпадению, именно столько белка С, использующегося для предотвращения тромбообразования, требуется ежегодно. С другой стороны, одной трансгенной коровы будет более чем достаточно для получения требуемого ежегодно количества фактора IX (фактора Кристмаса) каскадного механизма свертывания крови, который вводят больным гемофилией для повышения свертываемости крови.Слайд 53 Для создания трансгенных коров использовали модифицированную схему трансгеноза
мышей методом микроинъекций ДНК. Процедура включала следующие основные этапы:
Сбор
ооцитов коров, забитых на скотобойне.Созревание ооцитов in vitro.
Оплодотворение бычьей спермой in vitro.
Центрифугирование оплодотворенных яйцеклеток для концентрирования желтка, который в нормальных яйцеклетках мешает визуализации мужского пронуклеуса с помощью секционного микроскопа.
Микроинъекция ДНК в мужской пронуклеус.
Развитие эмбрионов in vitro.
Нехирургическая имплантация одного эмбриона реципиентной самке во время течки.
Скрининг ДНК потомков на наличие трансгена.
Слайд 56
Трансгенные птицы
Микроинъекция ДНК в оплодотворенные яйцеклетки птиц с
целью получения трансгенных линий - непростая процедура. Это связано
с некоторыми особенностями воспроизводства и развития птиц. Так, при оплодотворении у птиц в яйцеклетку могут проникнуть сразу несколько сперматозоидов, а не один, как это обычно бывает у млекопитающих, и идентифицировать тот мужской пронуклеус, который соединится с женским, становится невозможно. Метод микроинъекции ДНК в цитоплазму тоже не подходит, поскольку в этом случае ДНК не интегрируется в геном оплодотворенной яйцеклетки. Наконец, даже если удастся осуществить микроинъекцию ДНК в ядро, дальнейшие операции будет трудно осуществить, поскольку у птиц яйцеклетка после оплодотворения достаточно быстро обволакивается прочной мембраной, покрывается слоем альбумина и внутренней и наружной известковыми оболочками.Слайд 57 Получение трансгенных цыплят трансфекцией изолированных клеток бластодермы. Выделенные
клетки трансфицируют трансгеном с помощью липосом и вводят в
подзародышевую область облученной бластодермы реципиента. Часть полученных потомков являются химерами, а некоторые из них, несущие трансген в клетках зародышевой линии, при скрещивании могут дать начало трансгенным линиям.Получение трансгенных цыплят
Слайд 58
Трансгенные рыбы
По мере истощения природных рыбных запасов все
большую роль будет приобретать разведение рыбы в искусственных условиях.
Основная цель исследований в этой области — создание рекомбинантных рыб путем трансгеноза. До настоящего времени трансгены вводили микроинъекцией ДНК или электропорацией оплодотворенных яйцеклеток различных видов рыб - карпа, зубатки, форели, лосося и т. д. Поскольку у рыб пронуклеус в оплодотворенной яйцеклетке плохо различим в обычный микроскоп, линеаризованную трансгенную ДНК вводят в цитоплазму оплодотворенных яйцеклеток или клеток эмбрионов, достигших стадии четырех бластомеров. Эмбриогенез у рыб протекает в водной среде вне организма, поэтому в имплантации нет необходимости. Все дальнейшие процессы могут протекать в резервуарах с регулируемой температурой. Выживаемость эмбрионов рыб после микроинъекций довольно высока, от 35 до 80%, а доля трансгенных потомков колеблется от 10 до 70%. Трансген можно обнаружить с помощью ПЦР с использованием либо препаратов эритроцитов зародышей, либо суммарной ДНК. Скрещивая трансгенных рыб, можно вывести трансгенные линии.
Слайд 59
Трансгенные мыши: методология
Введение чужеродной ДНК мышам можно осуществить
разными методами:
С помощью ретровирусных векторов, инфицирующих клетки эмбриона на
ранних стадиях развития перед имплантацией эмбриона в самку-реципиента;Микроинъекцией в увеличенное ядро спермия (мужской пронуклеус) оплодотворенной яйцеклетки;
Введением генетически модифицированных эмбриональных стволовых клеток в предимпланированный эмбрион на ранних стадиях развития.





























