- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Насыщенный пар
Содержание
- 2. Испарение и конденсацияИспарение – процесс превращения жидкости
- 3. Насыщенный парНасыщенный пар – пар, находящийся в
- 4. Давление насыщенного параКонцентрация молекул насыщенного пара при
- 5. Ненасыщенный парНенасыщенный пар – когда при постепенном
- 6. Зависимость давления насыщенного пара от температуры. Кипение.
- 7. Зависимость давления насыщенного пара от температурыС ростом
- 8. Главное различие в поведении идеального газа и
- 9. КипениеКипение - превращение жидкости в пар по
- 10. Особенности жидкости при кипении: 1)при постоянном внешнем
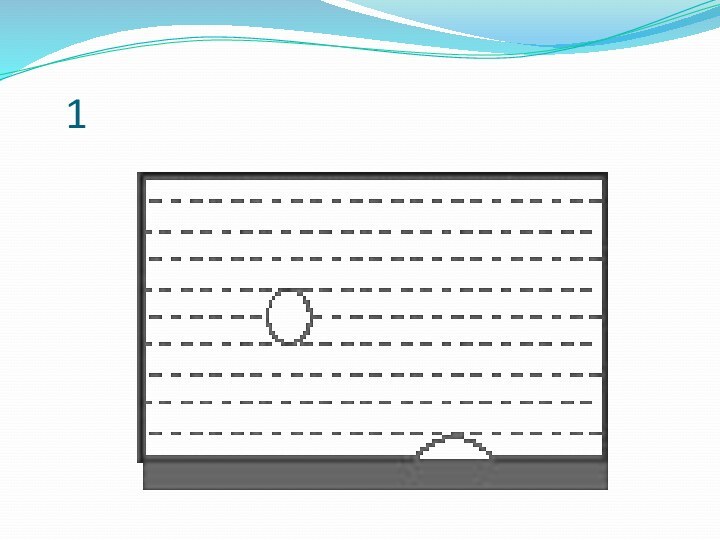
- 11. Процесс кипения
- 12. 1
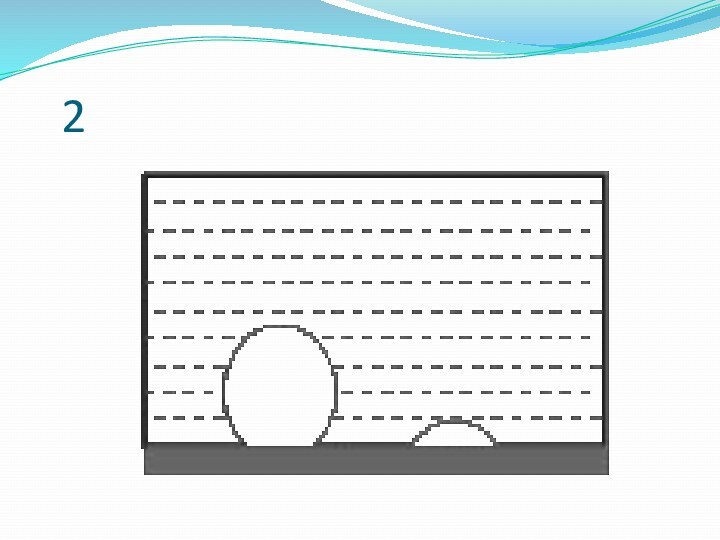
- 13. 2
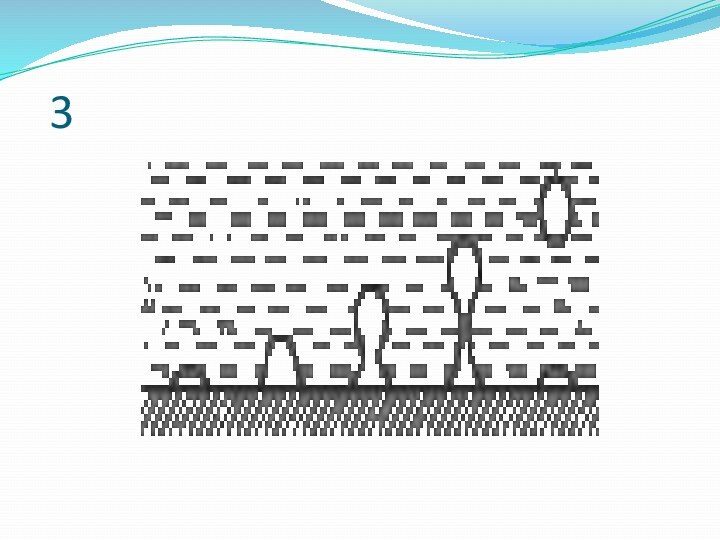
- 14. 3
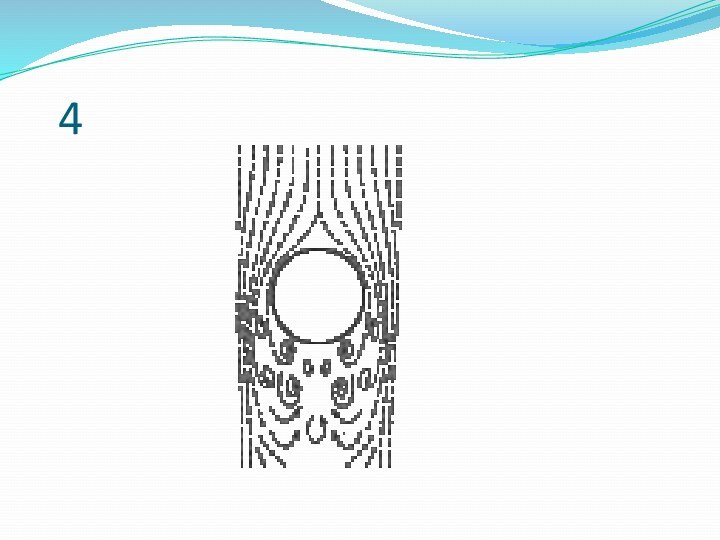
- 15. 4
- 16. 5
- 17. Скачать презентацию
- 18. Похожие презентации
Испарение и конденсацияИспарение – процесс превращения жидкости в парКонденсация – процесс превращения пара в жидкостьИспарение и Конденсация – взаимно компенсирующие процессы.












Слайд 2
Испарение и конденсация
Испарение – процесс превращения жидкости в
пар
– взаимно компенсирующие процессы.
Слайд 3
Насыщенный пар
Насыщенный пар – пар, находящийся в динамическом
равновесии со своей жидкостью.
Динамическое равновесие – когда число молекул,
покидающих поверхность жидкости за некоторый промежуток времени, будет равно в среднем числу молекул пара, возвратившихся за то же время в жидкость.
Слайд 4
Давление насыщенного пара
Концентрация молекул насыщенного пара при постоянной
температуре не зависит от его объёма.
Так как давление пропорционально
концентрации молекул(p=nkT), то из этого следует, что давление насыщенного пара не зависит от занимаемого им объёма.Давление насыщенного пара(pн.п.) – такое давление пара, при котором жидкость находится в равновесии со своим паром.
Слайд 5
Ненасыщенный пар
Ненасыщенный пар – когда при постепенном сжатии
пара, превращения в жидкость(конденсации) не происходит.
Однако пар превращается в
жидкость не при любой температуре. Если температура выше некоторого значения, то, как бы мы ни сжимали газ, он никогда не превратится в жидкость(такая норма называется критической температурой).Критическая температура(Ткр.) – максимальная температура, при которой пар ещё может превратиться в жидкость. У каждого вещества своя Ткр.
Т>Ткр(газ); Т<Ткр(пар);
Слайд 7
Зависимость давления насыщенного пара от температуры
С ростом температуры
давление растёт. Так как давление насыщенного пара не зависит
от объёма, то, следовательно, оно зависит только от температуры.При нагревании жидкости в закрытом сосуде часть жидкости превращается в пар. В результате, согласно формуле(p=nkT), давление насыщенного пара растет не только вследствие повышения температуры, но и вследствие увеличения концентрации молекул(плотности) пара.
Слайд 8
Главное различие в поведении идеального газа и насыщенного
пара состоит в том, что при изменении температуры в
закрытом сосуде (или при изменении объёма при постоянной температуре) меняется масса пара. Жидкость частично превращается в пар, или, напротив, пар частично конденсируется. С идеальным газом ничего подобного не происходит.
Слайд 9
Кипение
Кипение - превращение жидкости в пар по всему
объёму жидкости при постоянной температуре.
Зависимость температуры кипения от давления.
Жидкость
кипит тогда, когда давление её насыщенного пара = внешнему давлению. Температура кипения - температура жидкости, при которой давление её насыщенного пара равно или превышает внешнее давление.
Слайд 10
Особенности жидкости при кипении:
1)при постоянном внешнем давлении
Т жидкости постоянна.
2)с повышением внешнего давления температура кипения
повышается, с понижением – понижается.3)температура кипения зависит от наличия примесей.





























