в кельвинах?
Почему не может быть Т < 0 ?
От
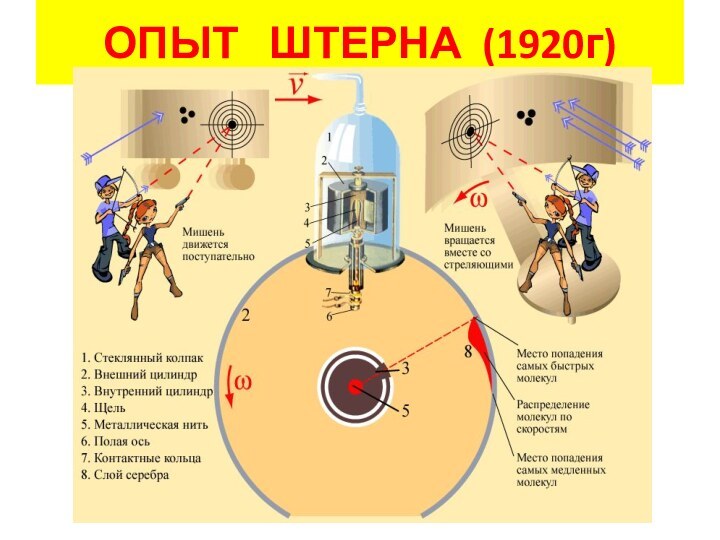
чего зависит энергия молекул?Как измерили скорость молекул?
Почему полоска серебра в опыте Штерна оказалась размытой?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть

















– 23
– 1
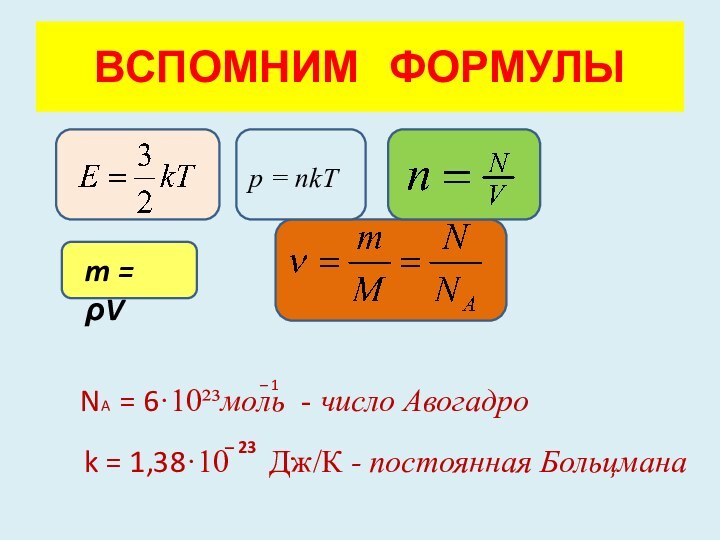
р = nkT
-23
23
УРАВНЕНИЕ СОСТОЯНИЯ
5
5
ЗАДАЧА
5
4
ЗАДАЧА
5
4
ЗАДАЧА
5
4