твердых тел
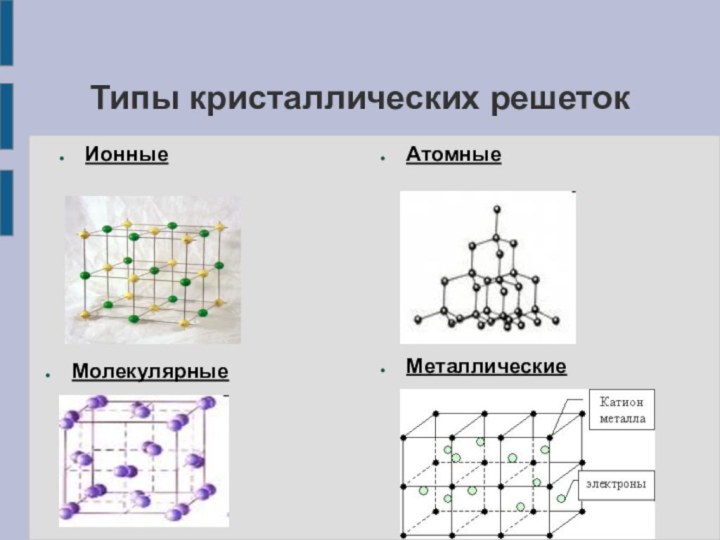
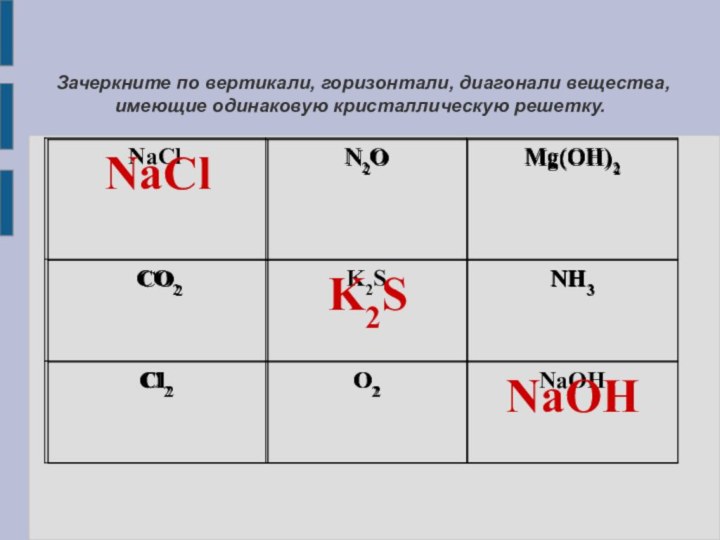
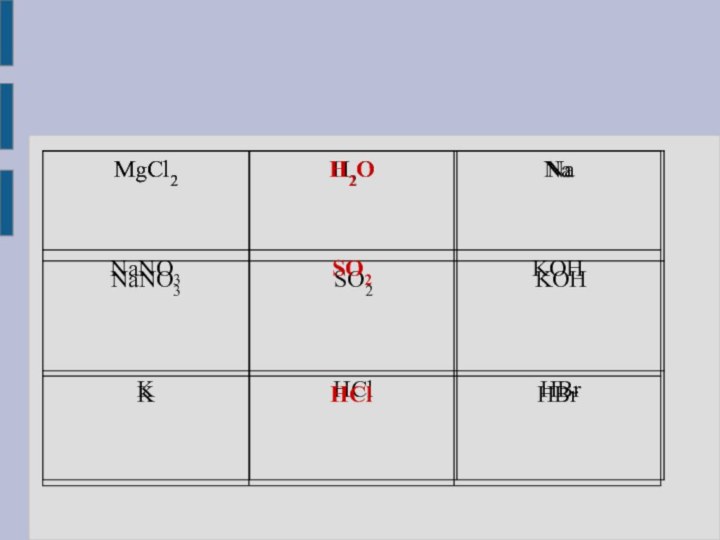
Дать представления о типах кристаллических решеток
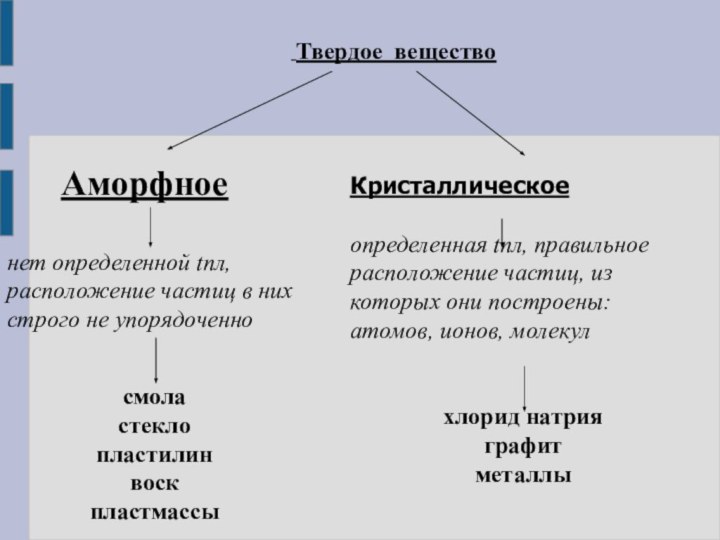
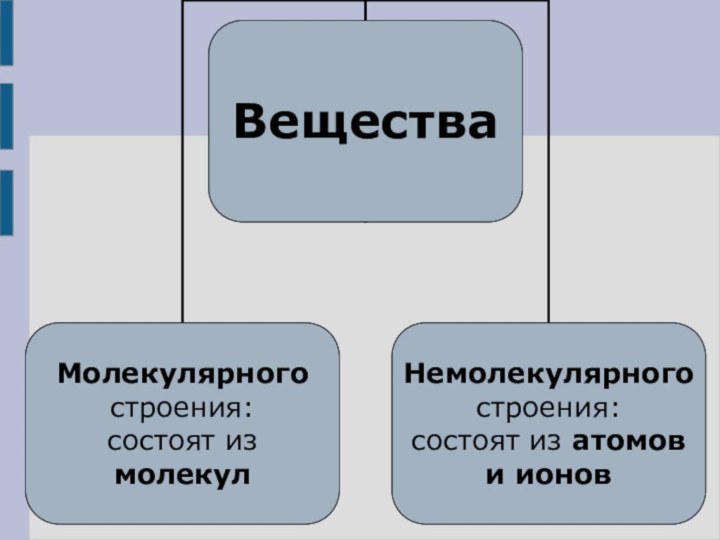
Установить взаимосвязь между
строением и свойствами веществДать представление о законе постоянства состава