- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Строение Бензола
Содержание
- 2. Бензол С6Н6 – родоначальник ароматических углеводородов.Каждый из
- 3. р-электроны всех атомов углерода взаимодействуют между собой
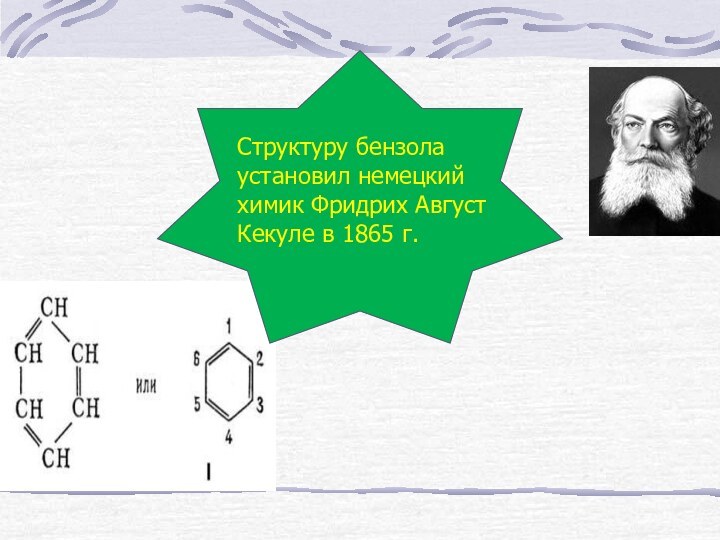
- 4. Структуру бензола установил немецкий химик Фридрих Август Кекуле в 1865 г.
- 5. Электронное строение бензолаСовременное представление об электронной природе
- 6. У Бензола изомеров нет.У Метилбензола изомеров нет.А у Этилбензола есть изомеры.И у Пропилбензола тоже есть изомеры
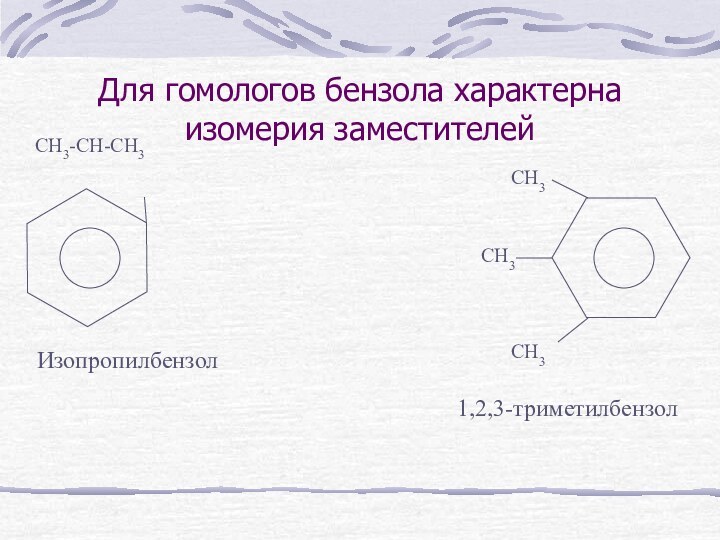
- 7. Для гомологов бензола характерна изомерия заместителейCH3-CH-CH3 Изопропилбензол CH3CH3CH31,2,3-триметилбензол
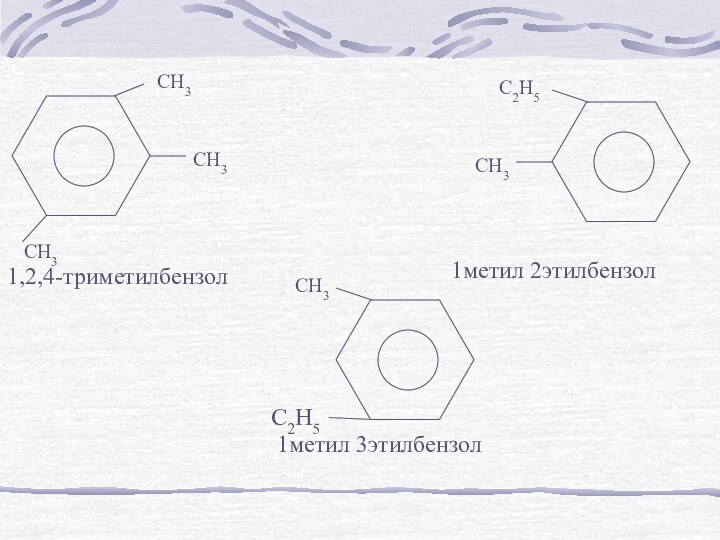
- 8. CH3CH3CH31,2,4-триметилбензол CH3C2H51метил 2этилбензол CH31метил 3этилбензол C2H5
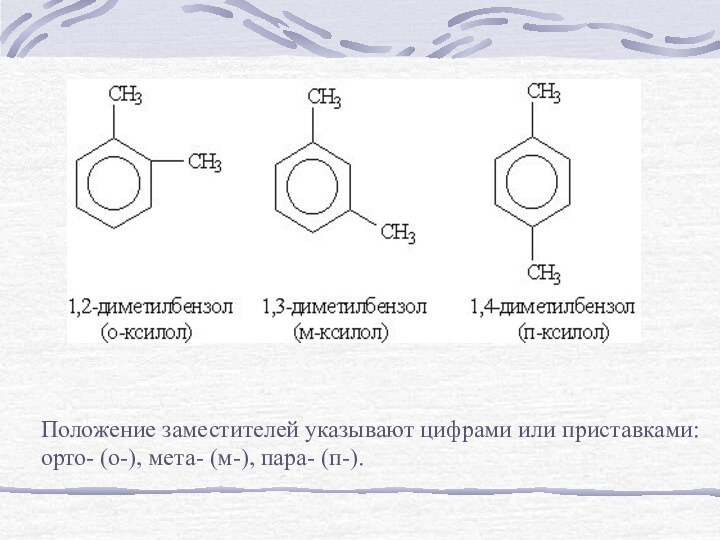
- 9. Структурная изомерия в гомологическом ряду бензола обусловлена
- 10. Скачать презентацию
- 11. Похожие презентации
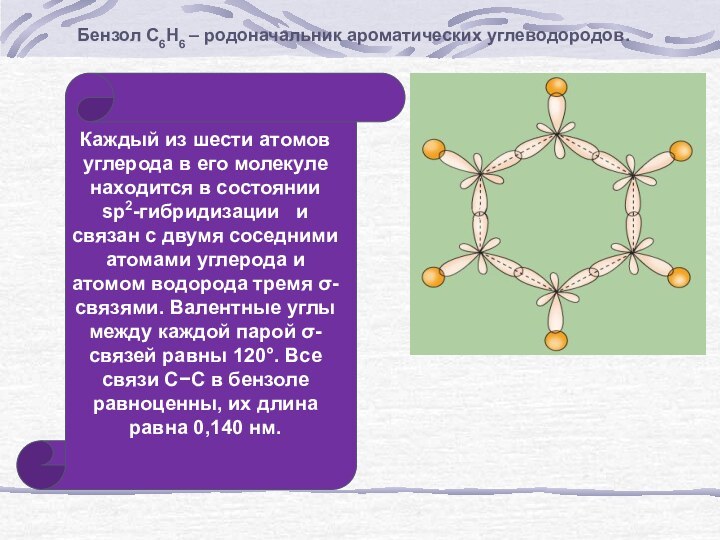
Бензол С6Н6 – родоначальник ароматических углеводородов.Каждый из шести атомов углерода в его молекуле находится в состоянии sp2-гибридизации и связан с двумя соседними атомами углерода и атомом водорода тремя -связями. Валентные углы между каждой парой -связей

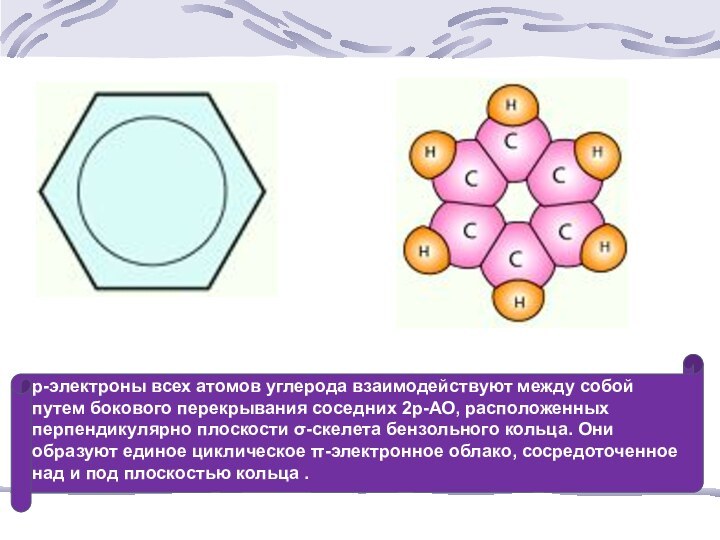


Слайд 3 р-электроны всех атомов углерода взаимодействуют между собой путем
бокового перекрывания соседних 2р-АО, расположенных перпендикулярно плоскости -скелета бензольного
кольца. Они образуют единое циклическое -электронное облако, сосредоточенное над и под плоскостью кольца .
Слайд 5
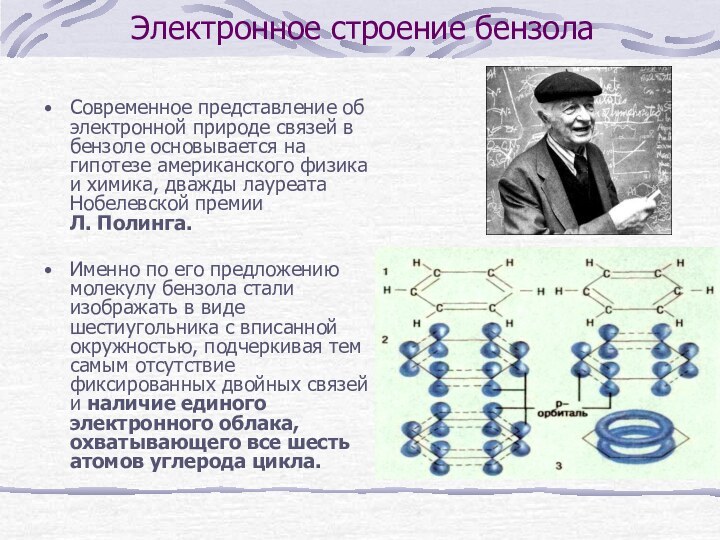
Электронное строение бензола
Современное представление об электронной природе связей
в бензоле основывается на гипотезе американского физика и химика,
дважды лауреата Нобелевской премии Л. Полинга.Именно по его предложению молекулу бензола стали изображать в виде шестиугольника с вписанной окружностью, подчеркивая тем самым отсутствие фиксированных двойных связей и наличие единого электронного облака, охватывающего все шесть атомов углерода цикла.