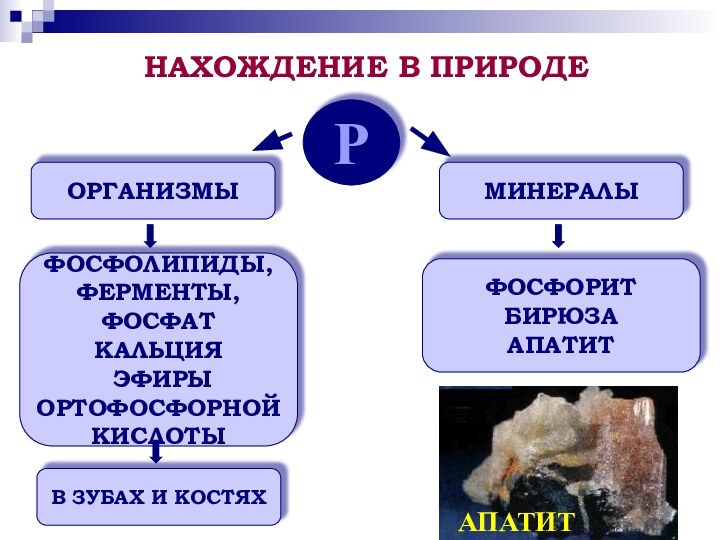
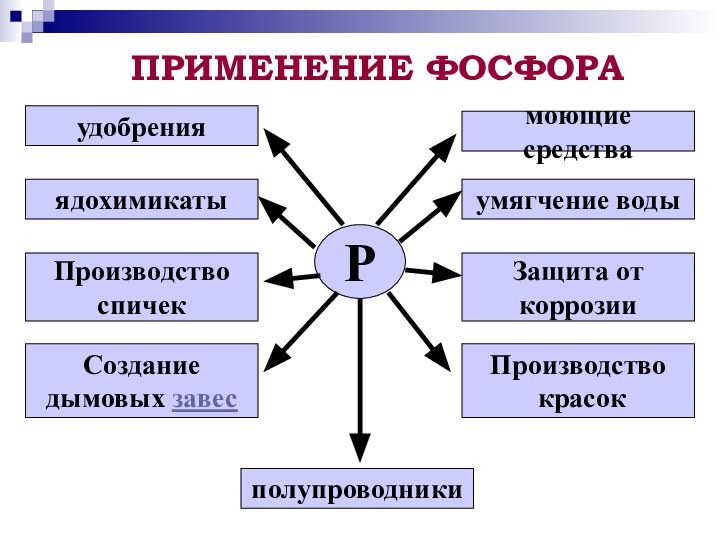
как о химическом элементе и простом веществе;
аллотропных видоизменениях
фосфора; повторить зависимость свойств вещества от его состава и строения;
развивать умение сравнивать;
способствовать формированию материалистического мировоззрения, нравственному воспитанию школьников.