- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Карбоновые кислоты 11 класс
Содержание
- 2. ПЛАН ИЗУЧЕНИЯ ТЕМЫ:Определение.Классификация карбоновых кислот.Номенклатура .Изомерия.Физические свойства.
- 3. ПЛАН ИЗУЧЕНИЯ ТЕМЫ:6. Химические свойства.7. Получение.8. Применение.9. Самостоятельная работа.10. Домашнее задание.
- 4. Карбоновые кислоты – это органические вещества, молекулы которых содержат одну или несколько карбоксильных групп(- СООН)
- 5. КЛАССИФИКАЦИЯ КИСЛОТ:По числу карбоксильных групп делятся на
- 6. ИЗОМЕРИЯ ОДНООСНОВНЫХ КАРБОНОВЫХ КИСЛОТУглеводородного радикала:СН3СН2СН2СООН – бутановая
- 7. АЛГОРИТМ СОСТАВЛЕНИЯ НАЗВАНИЙ КАРБОНОВЫХ КИСЛОТНайдите главную (самую
- 8. ФИЗИЧЕСКИЕ СВОЙСТВАНаличие водородных связей между молекулами обусловливает
- 9. ХИМИЧЕСКИЕ СВОЙСТВА1. Горение: СН3СООН +2О2=2СО2+2Н2О2. Свойства слабых кислот:a. Mg+2CH3COOH=(CH3COO)2Mg+H2b. CaO+2CH3COOH=(CH3COO)2Ca+H2Oc. NaOH+CH3COOH=CH3COONa+H2Od. K2CO3+CH3COOH=CH3COOK+H2O+CO2
- 10. ХИМИЧЕСКИЕ СВОЙСТВА3. Этерификация (реакция со спиртами, приводящая
- 11. ХИМИЧЕСКИЕ СВОЙСТВА:4. Замещение в углеводородном радикале:СН3-СН2-СООН+Cl2=CH3-CHCl-COOH+HCL5. Качественная реакция на муравьиную кислоту – реакция серебряного зеркала:HCOOH+Ag2O=CO2+H2O+2Ag
- 12. ПОЛУЧЕНИЕ КАРБОНОВЫХ КИСЛОТ1.Окисление альдегидов:
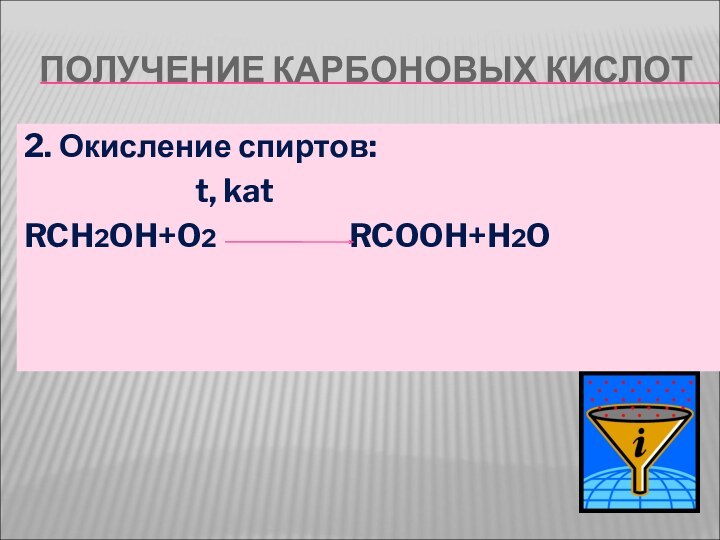
- 13. ПОЛУЧЕНИЕ КАРБОНОВЫХ КИСЛОТ2. Окисление спиртов:
- 14. ПОЛУЧЕНИЕ КАРБОНОВЫХ КИСЛОТ3. Окисление углеводородов:
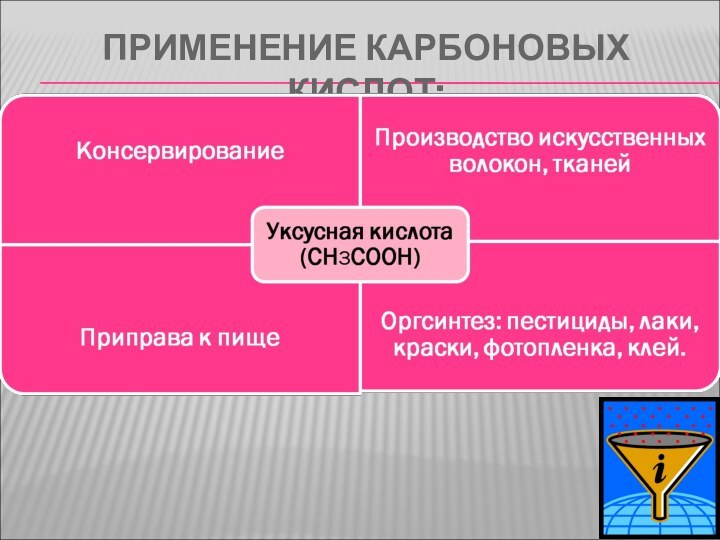
- 15. ПРИМЕНЕНИЕ КАРБОНОВЫХ КИСЛОТ:
- 16. ПРИМЕНЕНИЕ КАРБОНОВЫХ КИСЛОТ:
- 17. ПРИМЕНЕНИЕ КАРБОНОВЫХ КИСЛОТ:Высшие карбоновые кислоты ( пальмитиновая
- 18. САМОСТОЯТЕЛЬНАЯ РАБОТА:1.Выписать формулы веществ, с которыми может
- 19. 2. Записать структурную формулу вещества - 2-метилгексановая кислота.
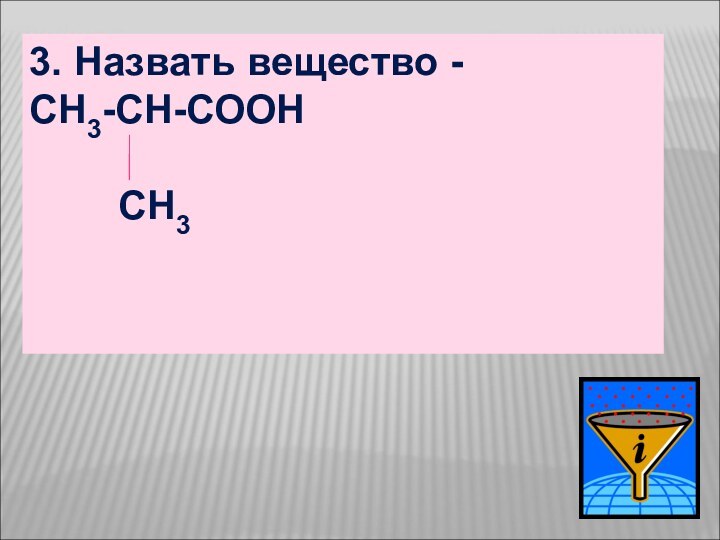
- 20. 3. Назвать вещество -
- 21. 4. В пищевой промышленности уксусная кислота
- 22. ДОМАШНЕЕ ЗАДАНИЕ:Параграф 14 учебника. (Уровень А).Упражнения 5, 7, 8. (Уровень Б).Упражнения 6, 10. (Уровень С).
- 23. Скачать презентацию
- 24. Похожие презентации
ПЛАН ИЗУЧЕНИЯ ТЕМЫ:Определение.Классификация карбоновых кислот.Номенклатура .Изомерия.Физические свойства.




















Слайд 2
ПЛАН ИЗУЧЕНИЯ ТЕМЫ:
Определение.
Классификация карбоновых кислот.
Номенклатура .
Изомерия.
Физические свойства.
Слайд 3
ПЛАН ИЗУЧЕНИЯ ТЕМЫ:
6. Химические свойства.
7. Получение.
8. Применение.
9. Самостоятельная
работа.
Слайд 4
Карбоновые кислоты –
это органические вещества,
молекулы которых
содержат одну или
несколько карбоксильных групп
(- СООН)
Слайд 5
КЛАССИФИКАЦИЯ КИСЛОТ:
По числу карбоксильных групп делятся на одноосновные
– НСООН – муравьиная кислота; двухосновные – НООС-СООН –
щавелевая кислота, трехосновные и т.д.По типу углеводородного радикала они делятся на предельные, непредельные и ароматические.
Слайд 6
ИЗОМЕРИЯ ОДНООСНОВНЫХ КАРБОНОВЫХ КИСЛОТ
Углеводородного радикала:
СН3СН2СН2СООН – бутановая кислота
СН3СНСООН
2-метилпропановая кислота
Межклассовая со сложными эфирами:
СН3СН2СООН – пропановая кислота
СН3СООСН3 – метиловый эфир уксусной кислоты
Слайд 7
АЛГОРИТМ СОСТАВЛЕНИЯ НАЗВАНИЙ КАРБОНОВЫХ КИСЛОТ
Найдите главную (самую длинную)
цепь углеродных атомов (включая атом карбоксильной группы).
Пронумеруйте углеродные атомы
главной цепи, начиная с углерода карбоксильной группы.Назовите соединение по алгоритму углеводородов.
В конце названия допишите суффикс «ов», окончание «ая» и слово «кислота»
Слайд 8
ФИЗИЧЕСКИЕ СВОЙСТВА
Наличие водородных связей между молекулами обусловливает высокие
температуры кипения и хорошую растворимость в воде карбоновых кислот.
Слайд 9
ХИМИЧЕСКИЕ СВОЙСТВА
1. Горение: СН3СООН +2О2=2СО2+2Н2О
2. Свойства слабых кислот:
a.
Mg+2CH3COOH=(CH3COO)2Mg+H2
b. CaO+2CH3COOH=(CH3COO)2Ca+H2O
c. NaOH+CH3COOH=CH3COONa+H2O
d. K2CO3+CH3COOH=CH3COOK+H2O+CO2
Слайд 10
ХИМИЧЕСКИЕ СВОЙСТВА
3. Этерификация (реакция со спиртами, приводящая к
образованию сложного эфира):
НСООН+С2Н5ОН=НСООС2Н5+Н2О
Муравьиная этанол
этиловый эфир кислота муравьиной кислоты
Слайд 11
ХИМИЧЕСКИЕ СВОЙСТВА:
4. Замещение в углеводородном радикале:
СН3-СН2-СООН+Cl2=CH3-CHCl-COOH+HCL
5. Качественная реакция
на муравьиную кислоту – реакция серебряного зеркала:
HCOOH+Ag2O=CO2+H2O+2Ag
Слайд 12
ПОЛУЧЕНИЕ КАРБОНОВЫХ КИСЛОТ
1.Окисление альдегидов:
kat, t
RCHO+O2
2RCOOH(лабораторные окислители: Ag2O, Cu(OH)2, KMnO4 и др.)
Слайд 14
ПОЛУЧЕНИЕ КАРБОНОВЫХ КИСЛОТ
3. Окисление углеводородов:
t, kat
2С4Н10+5О2 4СН3СОН+2Н2О
4. Из солей (лабораторный способ):
CH3COONa+H2SO4=CH3COOH + NaHSO4
Крист. Конц.





























