Ba(ОН)2
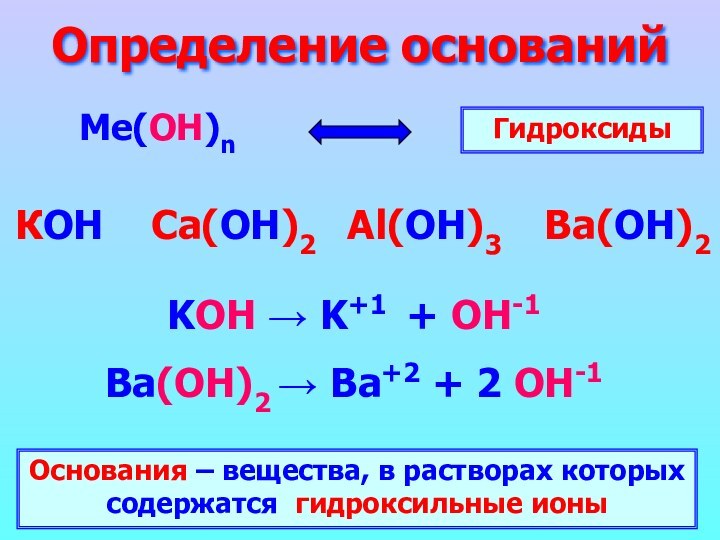
Гидроксиды
KOH → K+1 + OH-1
Ba(ОН)2 → Ba+2 +
2 OH-1Основания – вещества, в растворах которых содержатся гидроксильные ионы
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть

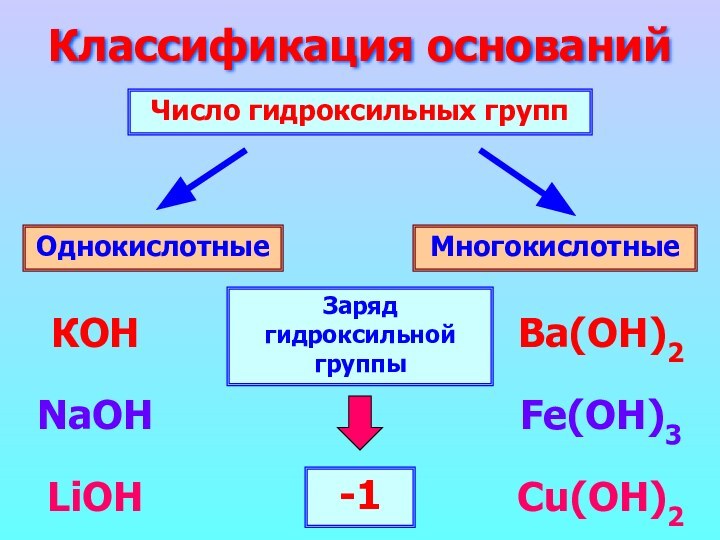
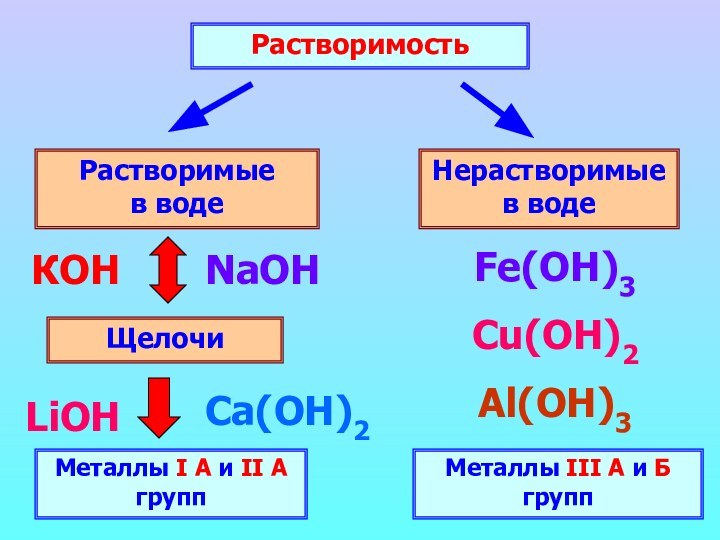


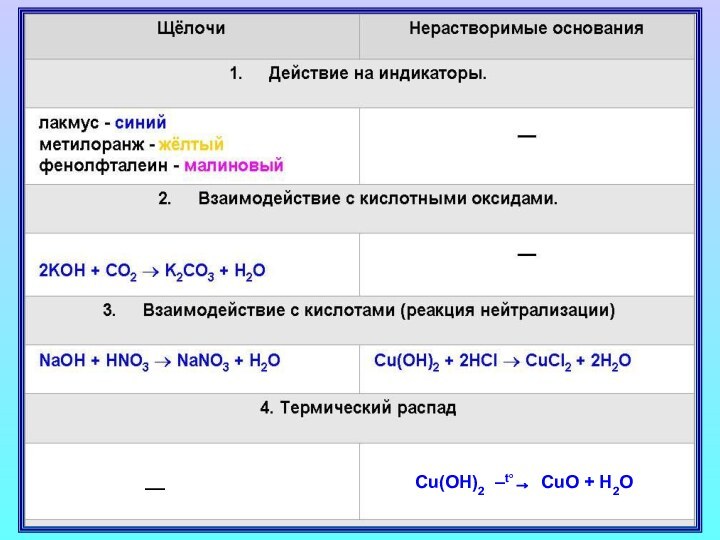
Основания – вещества, в растворах которых содержатся гидроксильные ионы
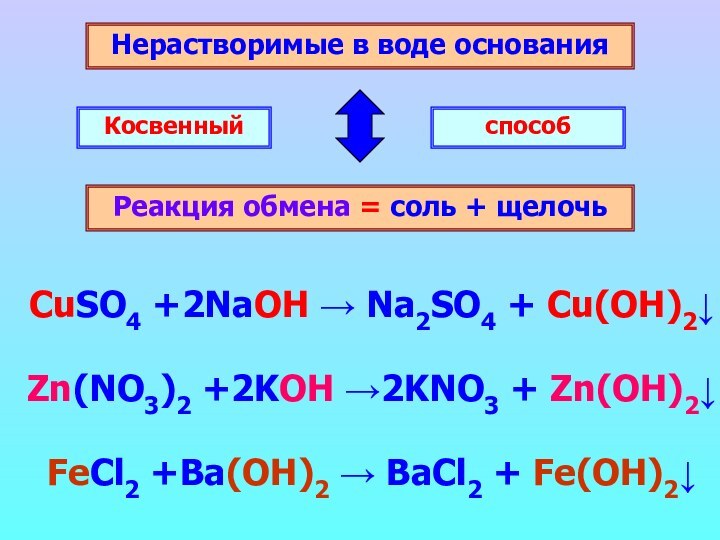
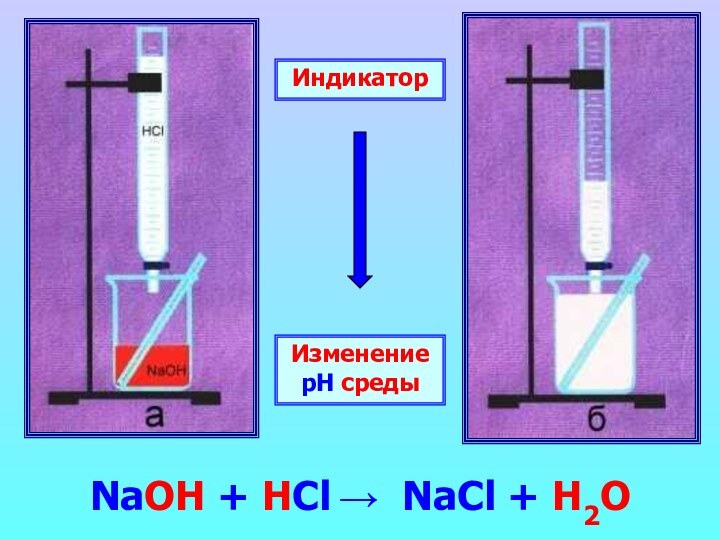
FeCl2 +Ba(OH)2 → BaCl2 + Fe(OH)2↓
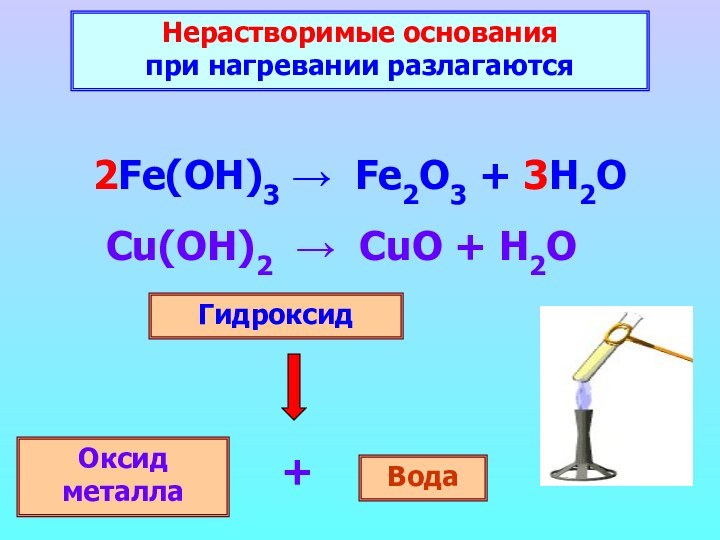
2Fe(OH)3 → Fe2O3 + 3H2O
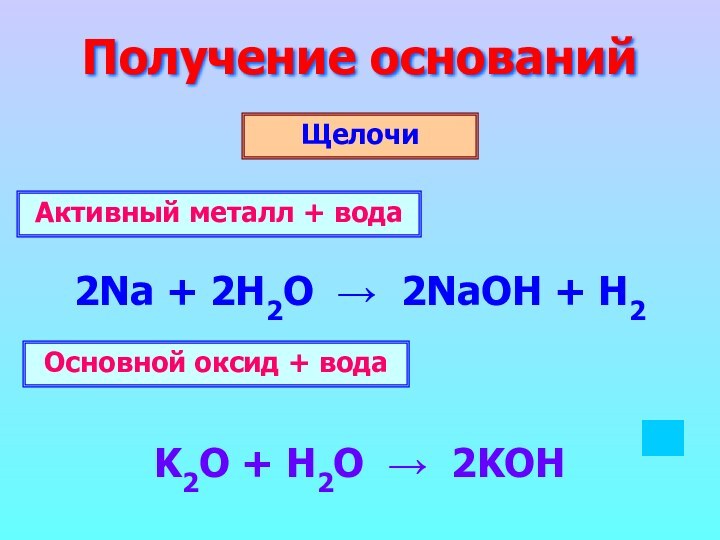
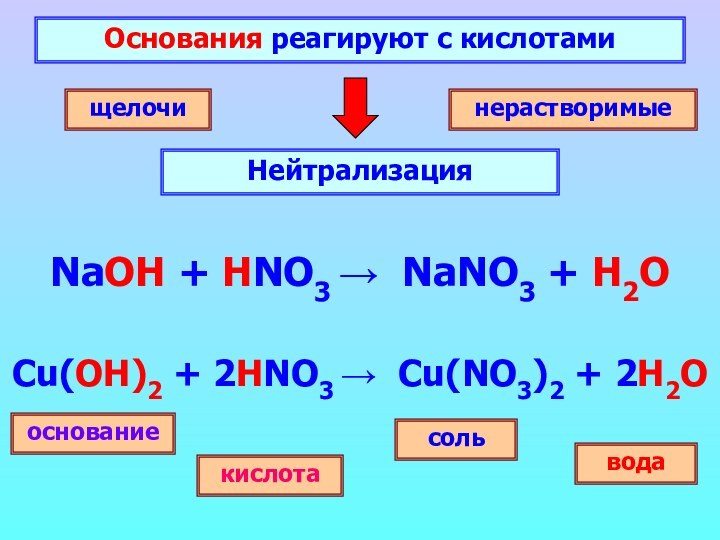
Гидроксид
Оксид металла
Вода
+