в окислительно-восстановительных процессах в живых организмах:
Витамин В12
Способы получения
комплексных соединений кобальта(III):реакции комплексообразования
в присутствии реагента-окислителя
(F2, O2, H2O2, KMnO4, ClO-…)
Смешаннолигандные комплексные соединения кобальта(III) с ацетилацетоном, этилендиамином и соединениями ряда витамина РР (никотиновая кислота)
оказывают противоопухолевое действие
Термодинамическая устойчивость комплексных соединений кобальта(III) значительно превосходит таковую для координационных соединений других 3d-элементов


![СФ- И ЯМР-ИССЛЕДОВАНИЕ РЕДОКС-ПРОЦЕССОВ В СИСТЕМЕ Со(II)-ЭДТА-H2O2 Комплексные соединения кобальта(III) с ЭДТАCo2+ + H2O2 + Edta → [CoEdta]- +](/img/tmb/15/1419834/0b1b69710c688ea539c3894906bda2a6-720x.jpg)

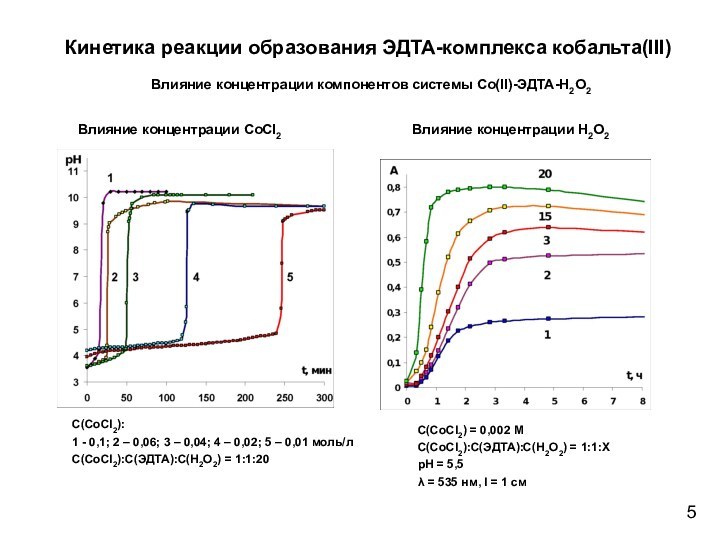

![СФ- И ЯМР-ИССЛЕДОВАНИЕ РЕДОКС-ПРОЦЕССОВ В СИСТЕМЕ Со(II)-ЭДТА-H2O2 Co2+ + ЭДТА4- → [CoЭДТА]2-[CoЭДТА]2- + H2O2 → [CoЭДТА]- + 2OH-](/img/tmb/15/1419834/34d916d059acaeb6bb9f58b506e9a83a-720x.jpg)