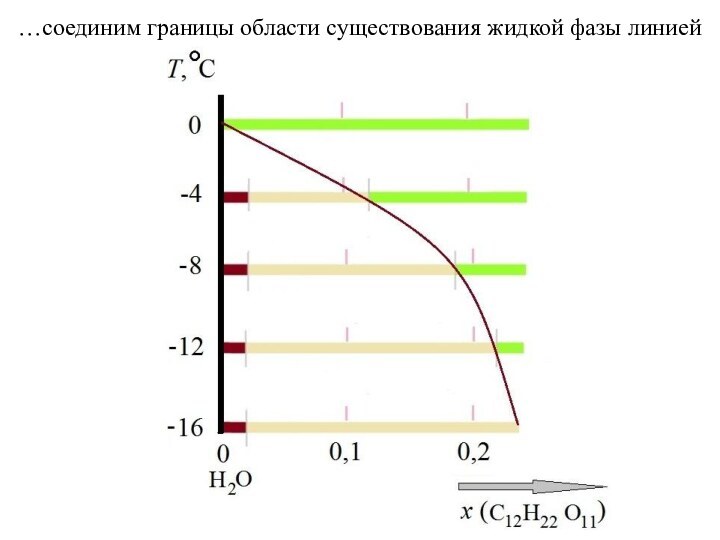
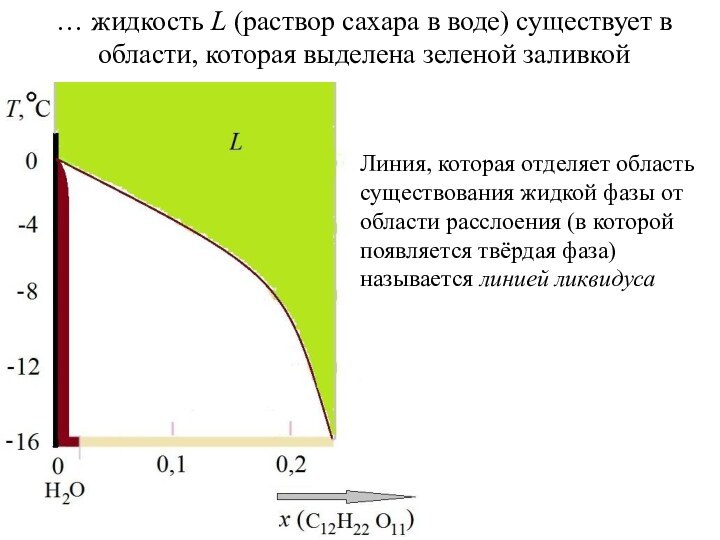
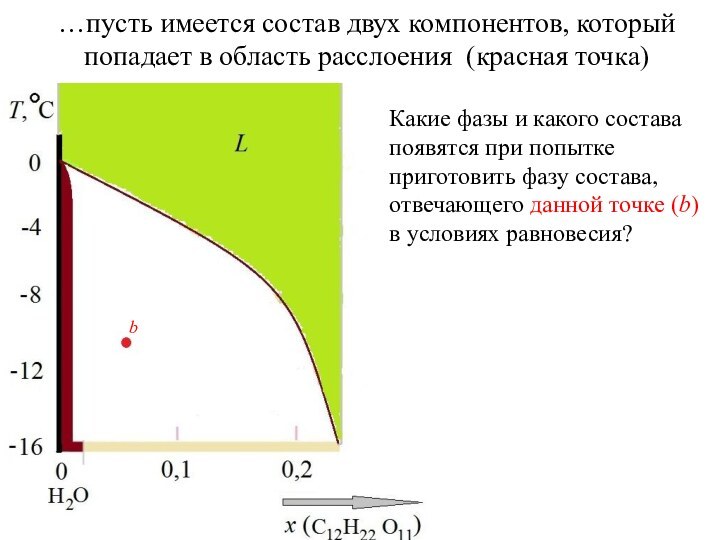
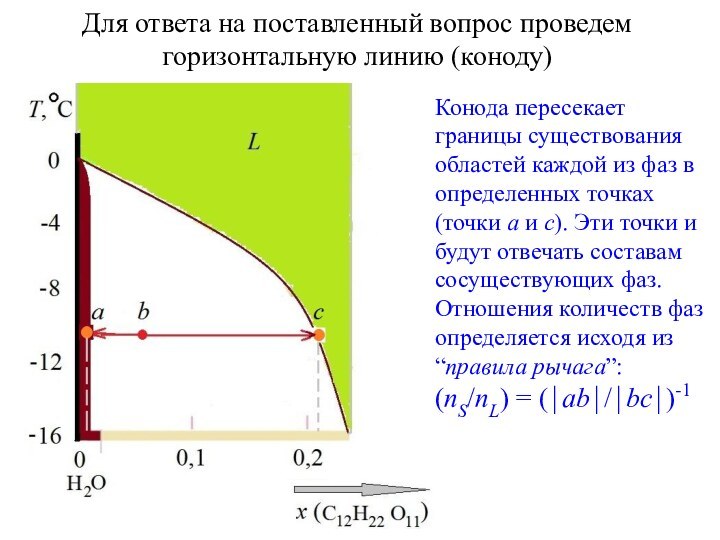
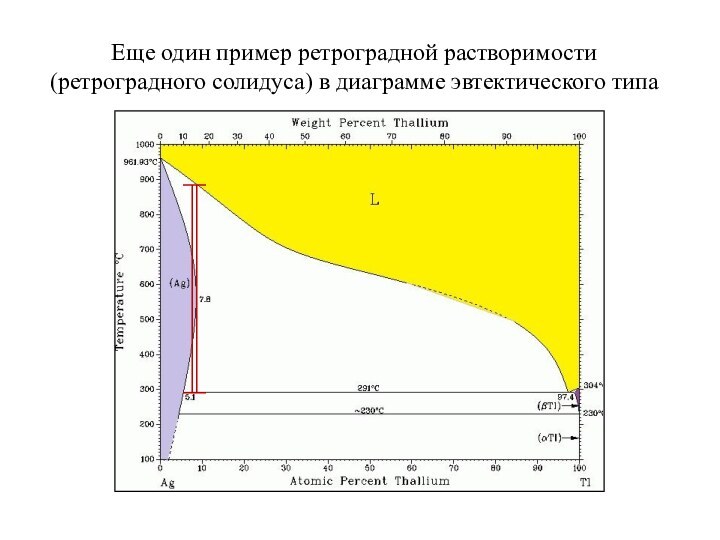
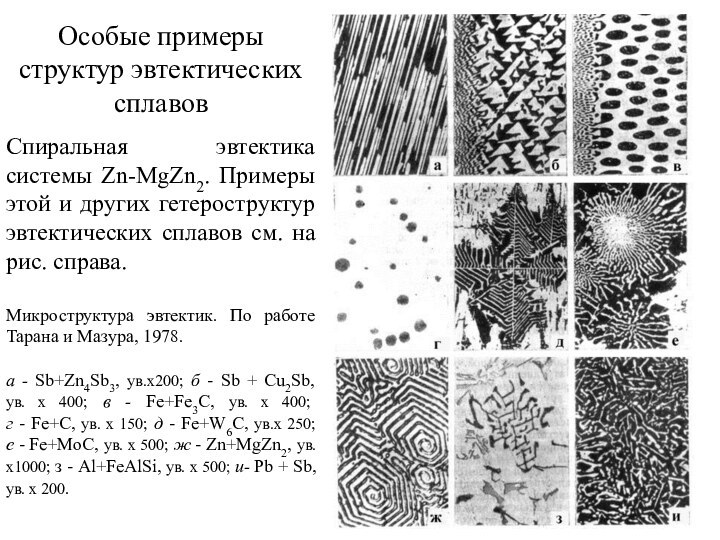
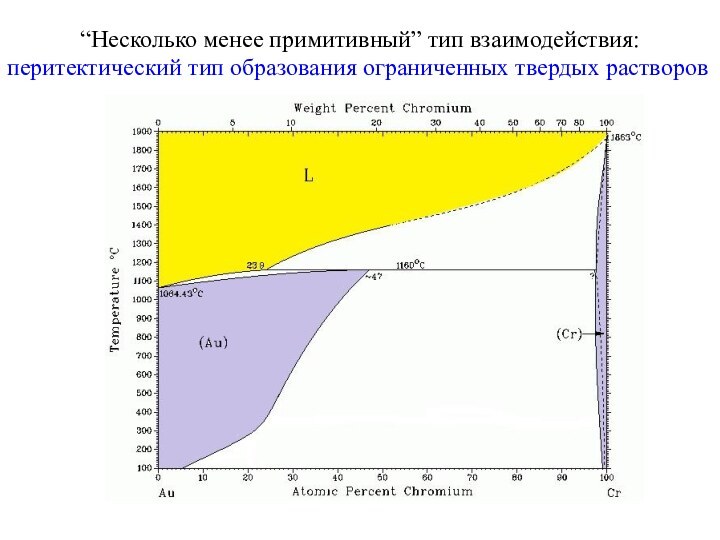
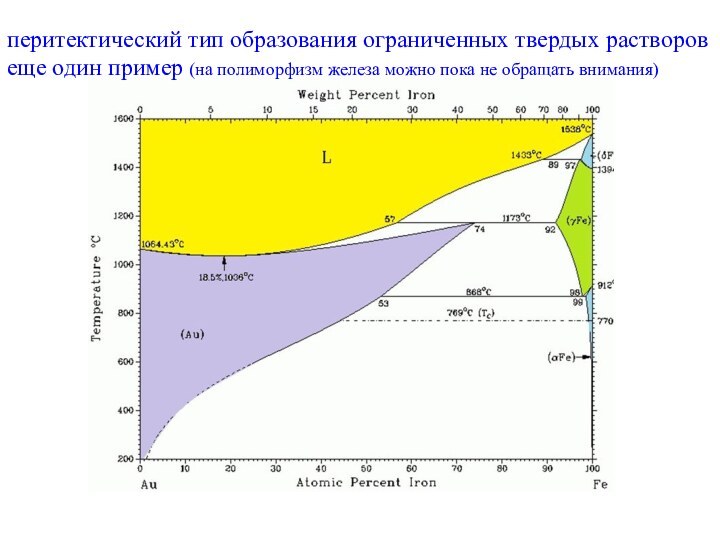
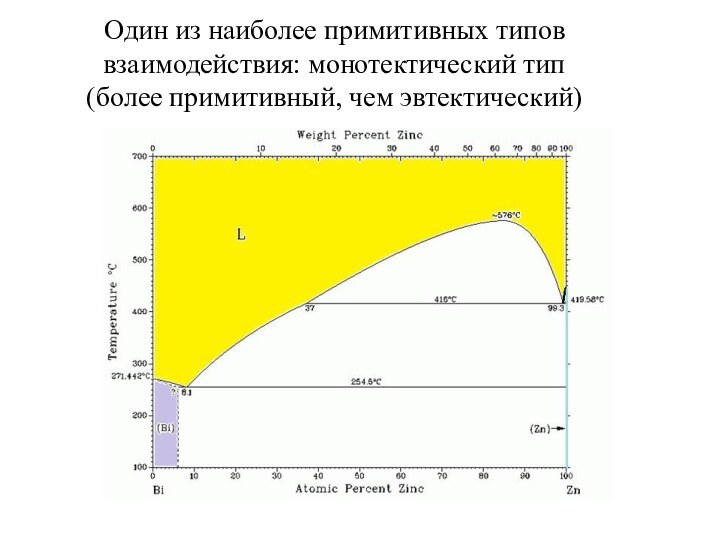
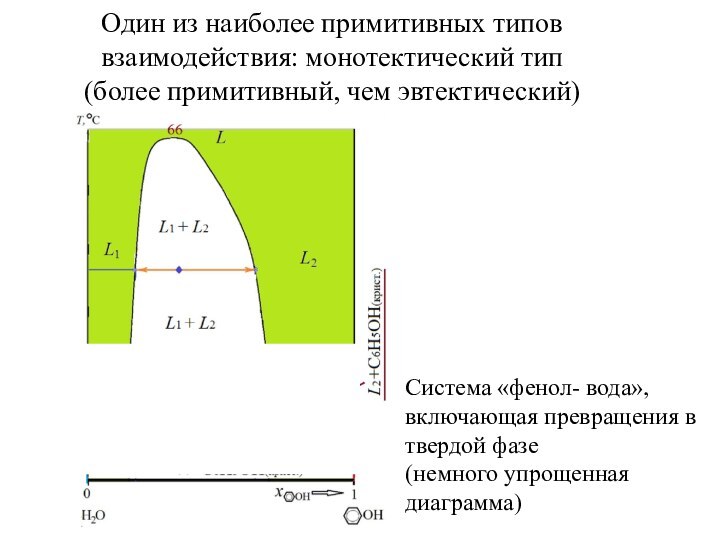
фаз
Компоненты: A, B. Должны быть переменные: P, T, xA,
xBНо можно обойтись набором трёх (а не четырех) переменных: P, T, xB, т.к. xB = 1 – xA
Должна быть трехмерная диаграмма с осями P, T, xB.
Зафиксируем первые две переменные: P = const, T=const′.
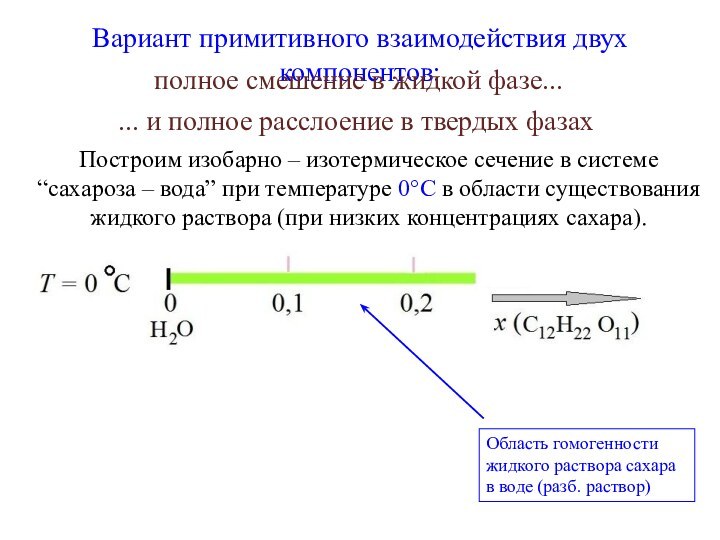
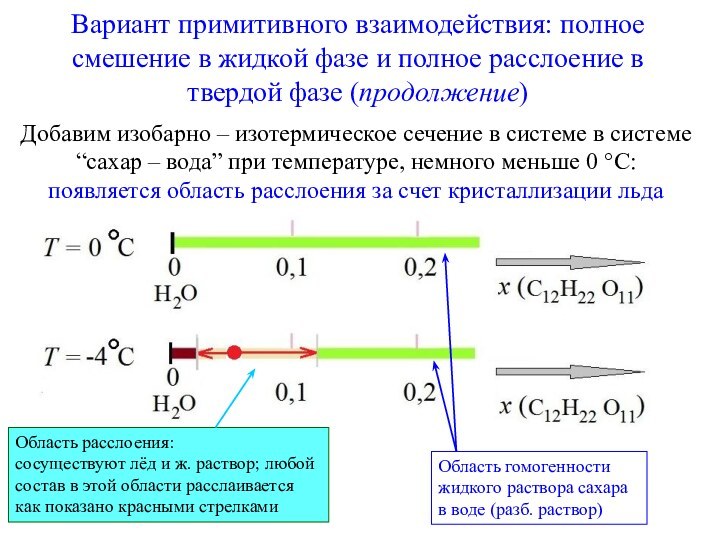
Пространство состояний в этом случае представлено числовым отрезком. Если происходит полное смешивание A и B при P = const, T=const′, то весь этот числовой отрезок [0, 1] и представляет собой P, T – фиксированную области гомогенности. A B
0 xB→ 1