- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Химические свойства оксидов
Содержание
- 2. Актуализация знанийОксиды — это простые или сложные
- 4. Знакомы с детства мы с водою,Она есть
- 5. Актуализация знанийОксиды — это простые или сложные
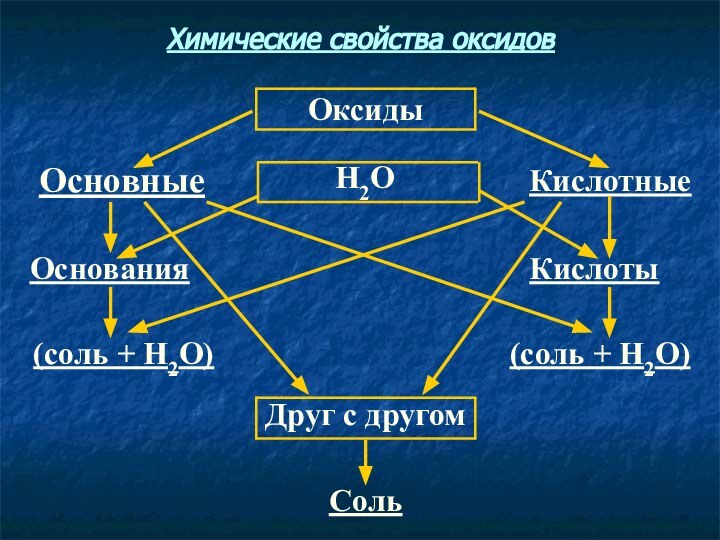
- 6. СольДруг с другом(соль + Н2О)(соль + Н2О)КислотыОснованияКислотныеН2ООсновныеОксидыХимические свойства оксидов
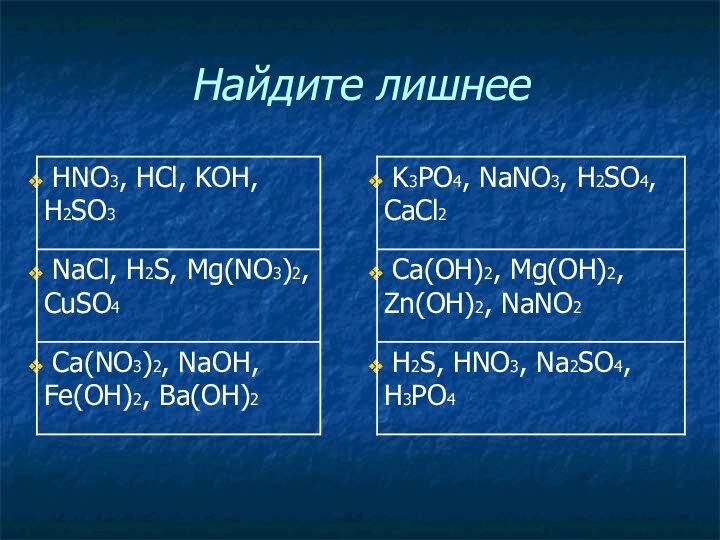
- 7. Найдите лишнее
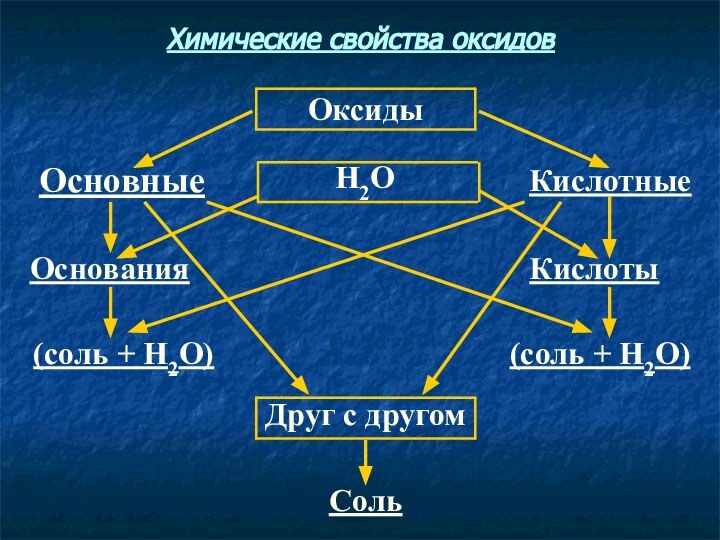
- 8. СольДруг с другом(соль + Н2О)(соль + Н2О)КислотыОснованияКислотныеН2ООсновныеОксидыХимические свойства оксидов
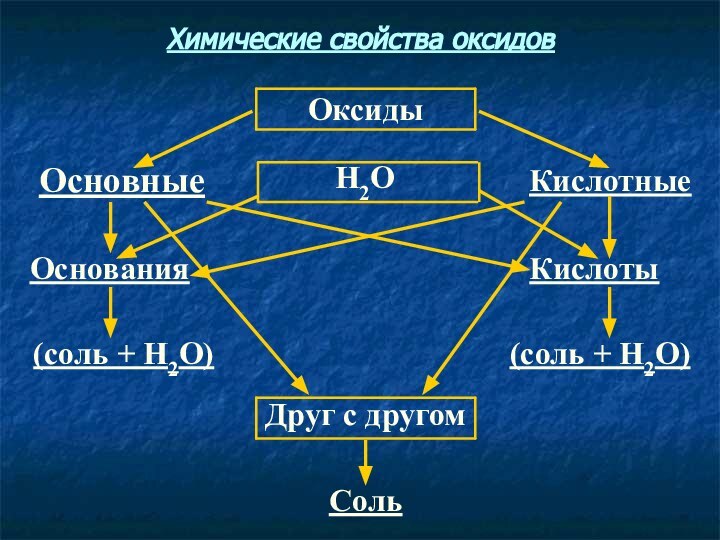
- 10. СольДруг с другом(соль + Н2О)(соль + Н2О)КислотыОснованияКислотныеН2ООсновныеОксидыХимические свойства оксидов
- 11. Запомните!Каждому кислотному оксиду соответствует определенная кислота. Например: СО2 → Н2СО3 SО2 → H2SО3 SО3 → Н2SО4 N2О5 → HNO3 P2О5 → H3PO4
- 12. Запомните!Каждому основному оксиду соответствует определенное основание. Например: Na2O → NaOH CaO → Ca(OH)2 Al2O3 → Al(OH)3 FeO → Fe(OH)2 Fe2O3 → Fe(OH)3
- 13. СаО + Н2O → Ca(OH)2 (Осн. оксид +
- 14. Самостоятельная работаНапишите уравнения реакций химических свойств следующих оксидов:
- 15. Домашнее задание:Выучить схему. Составить уравнения реакций химических свойств следующих оксидов: N2O5 и Al2O3.
- 16. Узнай "загадочный "оксид
- 17. Чтоб появиться я сумел,Прокаливают белый мел.Меня дает
- 18. Применение оксидовВ литосфере содержится оксид кремния -
- 19. Применение оксидовОксид кальция необходим для получения гашеной извести, которая используется для побелки.Драгоценные камни
- 20. Скачать презентацию
- 21. Похожие презентации
Актуализация знанийОксиды — это простые или сложные вещества? Свой ответ объясните.Дайте определение оксидов.В каком агрегатном состоянии могут находиться оксиды?
















Слайд 2
Актуализация знаний
Оксиды — это простые или сложные вещества?
Свой ответ объясните.
находиться оксиды?
Слайд 4
Знакомы с детства мы с водою,
Она есть всюду
на Земле -
И в облаках над головою,
И в чайной
чашке на столе...Она повсюду рядом с нами,
И так нас радует порой
Хрустящим снегом под ногами,
И речки быстрою струей...
Всяк зверь стремится к водопою,
Ей рады птица и цветок...
Где есть вода - там все живое,
Где нет - пыль камень и песок.
Н2О
Слайд 5
Актуализация знаний
Оксиды — это простые или сложные вещества?
Свой ответ объясните.
Дайте определение оксидов.
В каком агрегатном состоянии могут
находиться оксиды?Какие виды оксидов вы знаете?
Слайд 6
Соль
Друг с другом
(соль + Н2О)
(соль + Н2О)
Кислоты
Основания
Кислотные
Н2О
Основные
Оксиды
Химические свойства
оксидов
Слайд 8
Соль
Друг с другом
(соль + Н2О)
(соль + Н2О)
Кислоты
Основания
Кислотные
Н2О
Основные
Оксиды
Химические свойства
оксидов
Слайд 10
Соль
Друг с другом
(соль + Н2О)
(соль + Н2О)
Кислоты
Основания
Кислотные
Н2О
Основные
Оксиды
Химические свойства
оксидов
Слайд 11
Запомните!
Каждому кислотному оксиду соответствует определенная кислота. Например:
СО2 → Н2СО3
SО2 → H2SО3
SО3 → Н2SО4
N2О5 → HNO3
P2О5 → H3PO4
Слайд 12
Запомните!
Каждому основному оксиду соответствует определенное основание. Например:
Na2O → NaOH
CaO → Ca(OH)2
Al2O3 → Al(OH)3
FeO → Fe(OH)2
Fe2O3 → Fe(OH)3
Слайд 13
СаО + Н2O → Ca(OH)2
(Осн. оксид + вода
= основание)
СаО + H2SO4 → CaSO4 + H2O
(Осн. оксид
+ кислота = соль + вода)SO3 + H2O → H2SO4
(Кисл. оксид + вода = кислота)
SO3 + Са(ОН)2 → CaSO4 + Н2O
(Кисл. оксид + осн-е = соль + вода)
СаО + SO3 → CaSO4
(Осн. оксид + кисл. оксид = соль)
Слайд 15
Домашнее задание:
Выучить схему.
Составить уравнения реакций химических свойств
следующих оксидов: N2O5 и Al2O3.
Слайд 17
Чтоб появиться я сумел,
Прокаливают белый мел.
Меня дает огонь
в печи
И пламя маленькой свечи.
И стоит только сделать вдох,
Чтоб
я на свет явиться мог.Я в газированной воде,
Я в хлебе, дыме, я везде!
Слайд 18
Применение оксидов
В литосфере содержится оксид кремния - песок,
оксид алюминия - глина. Они незаменимы в строительстве.
Из глины
делают керамическую посудуОксид железа (III) - красный железняк и Fe3O4 - магнетит используют для получения железа.





























