- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Ионные уравнения.
Содержание
- 2. Р-ции между ионами называют ионными реакциями, а
- 3. .Реакции ионного обмена записывают тремя уравнениями:1)Молекулярное
- 4. 1) Написать молекулярное уравнение реакции:Na2SO4 + BaCl2
- 5. 5) Выписываем формулы и знаки тех ионов,
- 6. Реакции ионного обмена протекают до конца, если в результате реакции образуется вода (1), осадок(2) или газ(3).
- 7. Вода, как правило, образуется при реакции нейтрализации
- 8. 2) Образование осадка:
- 9. 3) Образование газа:1)2)3)
- 11. Вариант № 1(1а,б,в, 2а) Вариант № 2 (1г,д,е, 2б)
- 12. Скачать презентацию
- 13. Похожие презентации
Р-ции между ионами называют ионными реакциями, а уравнения таких р-ций – ионными уравнениями.Большинство хим. р-ий протекает в р-рах. Р-ры эл-тов содержат ионы ⇒р-ции в р-рах эл-тов = р-ции между ионами.











Слайд 2 Р-ции между ионами называют ионными реакциями, а уравнения
таких р-ций – ионными уравнениями.
р-рах. Р-ры эл-тов содержат ионы ⇒р-ции в р-рах эл-тов = р-ции между ионами.
Слайд 3
.
Реакции ионного обмена записывают
тремя уравнениями:
1)Молекулярное
2) Полное ионно-молекулярное
3) сокращенное ионно-молекулярное
Слайд 4
1) Написать молекулярное уравнение реакции:
Na2SO4 + BaCl2 →
2NaCl + BaSO4
2) С помощью таблицы растворимости определить растворимость
каждого вещества (около осадка ↓ , около газа ↑ ).3) Составляем полное ионное уравнение: сильные электролиты расписываются в виде ионов (! Не забудьте про заряды и индексы! Индексы становятся коэффициентами !). Слабые электролиты, нерастворимые (Н) и газообразные вещества записываются в молекулярном виде:
2Na+ + SO42- + Ba2+ + 2Cl- → 2Na+ + 2Cl- + BaSO4 ↓
Алгоритм написания ионного уравнения:
Слайд 5 5) Выписываем формулы и знаки тех ионов, которые
остались и участвовали в реакции:
SO42- + Ba2+ →
BaSO4 ↓4) Находим одинаковые ионы в левой и правой частях и «сокращаем» их (это ионы, которые в реакции не участвуют)
2Na+ + SO42- + Ba2+ + 2Cl- → 2Na+ + 2Cl- + BaSO4 ↓
Слайд 6 Реакции ионного обмена протекают до конца, если в
результате реакции образуется вода (1), осадок(2) или газ(3).
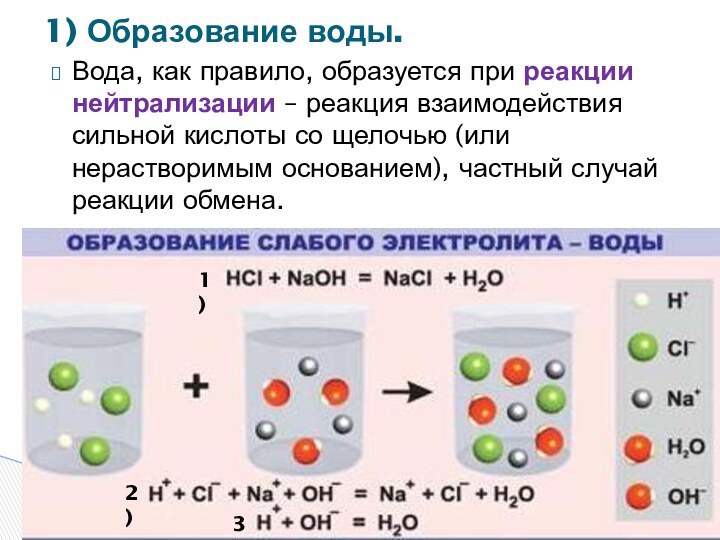
Слайд 7 Вода, как правило, образуется при реакции нейтрализации –
реакция взаимодействия сильной кислоты со щелочью (или нерастворимым основанием),
частный случай реакции обмена.1) Образование воды.
1)
2)
3)