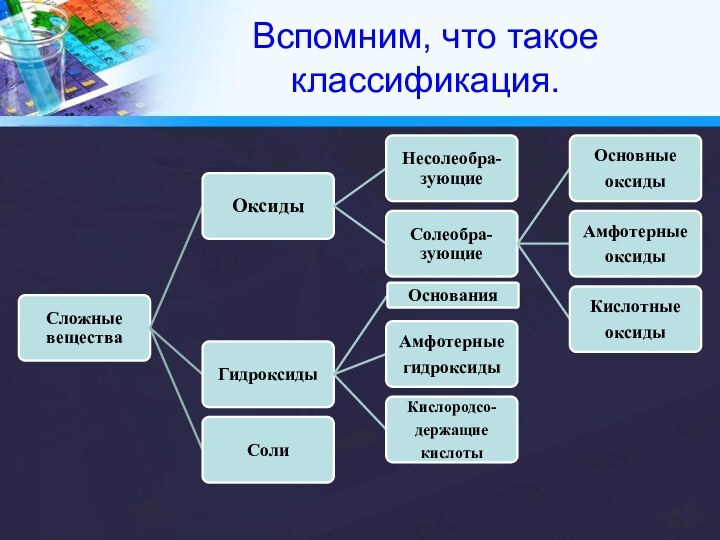
с понятием «классификация» на примере классификации химический элементов
Познакомиться с
группами сходных элементовПознакомить с периодическим законом Д.И.Менделеева и уметь его использовать для объяснения свойств элементов и образованных ими соединений.