Слайд 2
История исследований
в молекулярной биологии
Апрель 1953 г. - предложена
модель пространственной структуры ДНК - двойная спираль (журнал “Nature”
"Структура ДНК" Д. Уотсон и Ф. Крик)
В биологии начался новый отсчет времени – развитие молекулярной биологии
На этом пути сделаны серии блестящих открытий, большинство из которых отмечены Нобелевскими премиями
Слайд 3
Джеймс Уотсон (р. 1928)
Френсис Крик (1916-2004)
1952 г
работа
над моделированием ДНК
Основа: правило Чаргаффа
и рентгенограммы Р. Франклин
и М.
Уилкинса
1953 г – публикация результатов
1962 г – Нобелевская премия
Слайд 4
"...выдающийся харизматический символ нашего времени - спиральная лестница,
ведущая, я надеюсь, в небеса, - была разрекламирована с
поистине выдающейся интенсивностью. Она использовалась как эмблема, ее рисовали на галстуках, она украшала фирменные бланки, ее устанавливали перед зданиями.... Она даже вторглась в высокие формы изящного искусства" .
Апрель 2013 г – 60 лет с момента открытия структуры ДНК
Какова роль молекулярной биологии в развитии современной медицины?
Е. Чаргафф
Слайд 5
Актуальность темы лекции:
открытия молекулярной биологии играют важную роль
в развитии современной медицины
Использование ДНК-технологий
выявление мутаций генов
выявление наследственных заболеваний
определение
особенностей генома
установление родства
диагностика бактериальных и вирусных заболеваний
производство рекомбинантных белков, гормонов….
производство лекарственных препаратов – ингибиторов матричных биосинтезов в опухолевых и бактериальных клетках
расшифровка генома человека (международный проект под рук. Д. Уотсона, 1990-2003 г) с целью ранней диагностики и лечения заболеваний
Слайд 6
Генная и клеточная терапия – «небеса», к которым
привела спиральная лестница ДНК
Генная терапия – лечение путем введения
в клетки пациентов генов, устраняющих генные дефекты или придающие им новые функции
Первый клинический опыт
1990 г, США, 4-х летняя девочка с иммунодефицитным состоянием
Причина заболевания:
мутация гена аденозиндезаминазы → нарушение обмена нуклеотидов → нарушение пролиферации и созревания лимфоцитов
Лечение: пересадка собственных лимфоцитов с предварительно введенным in vitro ретровирусом, содержащим нормальный ген фермента
Слайд 7
Клеточная терапия
Терапия с использованием стволовых клеток
С помощью определенных
генов можно перепрограммировать клетку и изменить путь ее дифференцировки
Разработана
технология получения плюрипотентных стволовых клеток из фибробластов кожи человека с помощью генов Myc, Oct3/4, Sox2, Klf4 и их дальнейшая дифференцировка в кардиомиоциты
(Шинья Яманака, Япония, Нобелевская премия 2012)
Слайд 8
Цель лекции
Знать:
строение и функции нуклеиновых кислот
химико-биологическую сущность
процессов репликации, транскрипции, трансляции
Использовать знания о матричных биосинтезах
для понимания химико-биологической сущности
процессов роста и развития организма
механизмов устойчивости организма к воздействиям внешней среды
механизмов действия противоопухолевых и антибактериальных препаратов
Использовать знания о матричных биосинтезах для формирования представлений
о принципах ДНК-технологий в диагностике и терапии
о механизме действия некоторых ядов и бактериальных токсинов
о генетических аспектах полиморфизма генов и белков, наследственных заболеваний и канцерогенеза
Слайд 9
План лекции
1. Строение и функции ДНК и РНК
(повторение курса химии)
2. Репликация и репарация
3. Транскрипция
4. Трансляция
Слайд 10
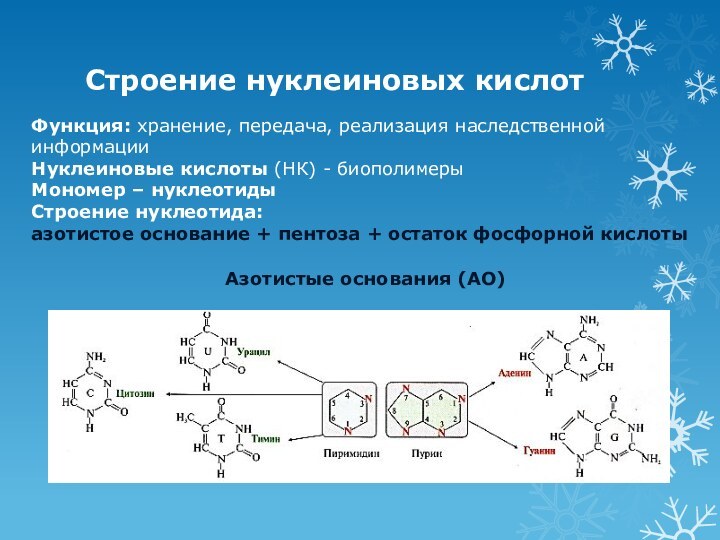
Строение нуклеиновых кислот
Функция: хранение, передача, реализация наследственной информации
Нуклеиновые
кислоты (НК) - биополимеры
Мономер – нуклеотиды
Строение нуклеотида:
азотистое основание +
пентоза + остаток фосфорной кислоты
Азотистые основания (АО)
Слайд 11
Пентозы в структуре нуклеиновых кислот
Слайд 12
Первичная структура НК: последовательность нуклеотидов
Химические связи:
1 - 5′-фосфоэфирная
2
– N-гликозидная
3 - 3′,5′ - фосфодиэфирная
Условные обозначения:
Х – водород
в ДНК
или -ОН в РНК
Слайд 13
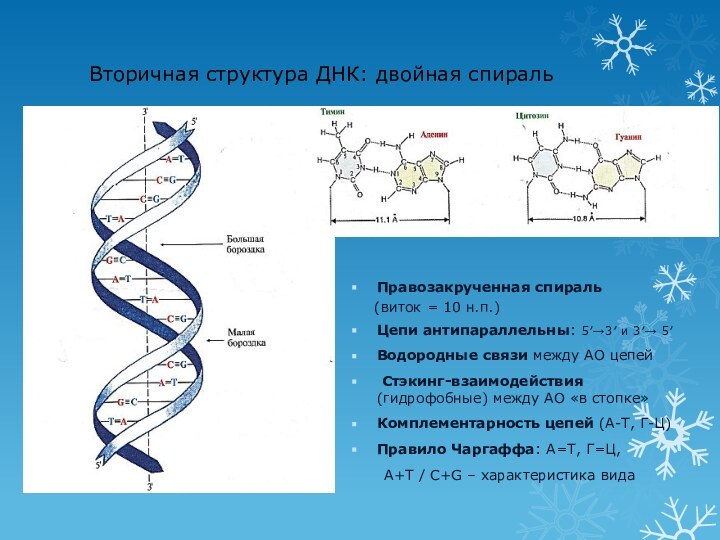
Вторичная структура ДНК: двойная спираль
Правозакрученная спираль
(виток = 10 н.п.)
Цепи антипараллельны: 5′→3′ и 3′→ 5′
Водородные
связи между АО цепей
Стэкинг-взаимодействия (гидрофобные) между АО «в стопке»
Комплементарность цепей (А-Т, Г-Ц)
Правило Чаргаффа: А=Т, Г=Ц,
А+Т / C+G – характеристика вида
Слайд 14
Третичная структура ДНК: нуклеопротеидные комплексы (хромосомы)
Гистоновые белки: белки
с высоким содержанием лиз и арг
5 типов: Н1, Н2А,
Н2В, Н3, Н4
Негистоновые белки: белки и ферменты, участвующие в матричных биосинтезах
Роль белков: обеспечивают суперспирализацию и компактизацию ДНК
Нуклеосома
ДНК (≈146 н.п.) + 8 молекул гистонов (Н2А, Н2В, Н3, Н4)2
Структура удерживается ионными связями между лиз, арг и остатками фосфорной кислоты
Линкерные участки
Участок ДНК (≈30 н.п.) между нуклеосомами, с которым связаны молекулы гистона Н1
Гетерохроматин – «компактный» хроматин, транскрипционно неактивный
Эухроматин – деспирализованный хроматин с низким содержанием гистонов и высоким содержанием негистоновых белков (период транскрипции)
Слайд 16
Пространственная структура РНК
Одноцепочечная
Шпильки – спирализованные участки (водородные связи)
Не
соблюдается правило Чаргаффа
Виды РНК:
мРНК
матрица в синтезе белка
2-4% от общего
количества РНК, разнообразная первичная структура
5′ - «кэп»-конец: 7-метил ГТФ (защита от нуклеаз, участие в инициации трансляции)
3′ - поли(А)-«хвост»: 150-200 остатков АМФ (выход из ядра, защита от нуклеаз)
Слайд 17
тРНК
Структура тРНК:
1 – шпильки
2 - петли
молекулы-адапторы: переводят информацию
мРНК в последовательность аминокислот в белке
15%
содержат
минорные нуклеотиды
(например,
метилированные АО)
Слайд 18
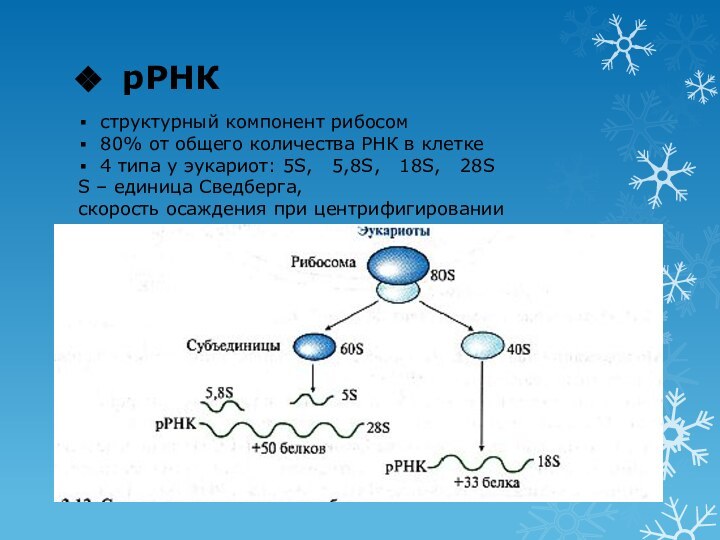
рРНК
структурный компонент рибосом
80% от общего количества РНК в
клетке
4 типа у эукариот: 5S, 5,8S, 18S,
28S
S – единица Сведберга,
скорость осаждения при центрифигировании
Слайд 19
РЕПЛИКАЦИЯ: синтез ДНК
Протекает в ядре в S-фазу клеточного
цикла перед митозом
Стимулы: гормоны, ростовые факторы, белки-циклины
Матрица: обе нити
ДНК, образуются 2 репликативные вилки
Направление синтеза новых цепей: 5′ - 3′ по принципу комплиментарности и антипараллельности
Участки синтеза – ориджины репликации
Участок ДНК между соседними ориджинами - репликон
Этапы репликации: инициация, элонгация, терминация
Субстраты и источники энергии: дАТФ, дГТФ, дТТФ, дЦТФ
Кофактор: Mg2+
Полуконсервативный процесс синтеза: каждая дочерняя молекула ДНК содержит одну родительскую нить и одну синтезированную
Образуется идентичная молекула ДНК (клетка 4n)
Слайд 20
1 этап репликации: инициация
Формирование репликативной вилки:
ДНК-топоизомераза гидролизует 3′,5′-фосфодиэфирную
связь в одной из цепей ДНК и присоединяется к
5′-концу в точке разрыва
2. ДНК-хеликаза, используя энергию АТФ, разрывает водородные связи и обеспечивает локальное разделение двойной спирали ДНК
ДНК-топоизомераза восстанавливает 3′,5′-фосфодиэфирную связь и отделяется
SSB (single strand binding)–белки связываются с одноцепочечными участками, препятствуя комплементарному скручиванию цепей
Слайд 22
2 этап репликации: элонгация
Синтез новых цепей ДНК
Лидирующая цепь:
3′ - 5′ (синтез непрерывный по ходу движения репликативной
вилки)
Отстающая цепь: 5′ - 3′ (рост этой цепи начинается после того, как на лидирующей цепи синтезируется участок из ≈200 нуклеотидов, синтез идет против движения репликативной вилки в виде фрагментов Оказаки)
Синтез цепей начинается с образования «затравки» (РНК-праймера из ≈10 нуклеотидов)
Ферменты:
ДНК-полимераза α синтезирует РНК-праймер и небольшой участок ДНК
ДНК-полимераза δ удлиняет лидирующую цепь
ДНК-полимераза δ или ε удлиняют отстающую цепь
Слайд 23
3 этап репликации: терминация
Исключение праймеров
Завершение формирования отстающей цепи
ДНК
Эндонуклеаза (РНКаза) удаляет РНК-праймер
ДНК-полимераза β заполняет «брешь»
ДНК-лигаза объединяет фрагменты,
затрачивая энергию АТФ
Слайд 25
Репарация ошибок и повреждений ДНК
Причина повреждений ДНК:
действие факторов
окружающей и внутренней среды
Повреждение ДНК происходит с частотой от
нескольких сотен до 1000 случаев в каждой клетке, каждый час
Виды повреждений:
дезаминирование АО (цитозин превращается в урацил), метилирование АО
депуринизация, депиримидинизация
образование пиримидиновых димеров (действие УФО)
разрыв цепей, ковалентные сшивки между цепями
ошибки репликации
Система репарации – ферменты (нуклеазы, полимеразы, лигазы)
Слайд 26
Схема работы системы репарации ДНК
Слайд 27
Роль системы репарации
Репарация необходима для сохранения генома и
возможна благодаря существованию 2-х цепей ДНК
Снижение активности ферментов репарации
приводит к накоплению мутаций
Полагают, что от 80 % до 90 % всех раковых заболеваний связаны с нарушением репарации ДНК
ПРИМЕР: пигментная ксеродерма – наследственное заболевание, связанное с мутацией генов системы репарации ДНК; УФО таких больных приводит к накоплению мутаций в клетках кожи и развитию рака
Слайд 28
ТРАНСКРИПЦИЯ: синтез РНК
Протекает в ядре вне зависимости от
фаз клеточного цикла
Матрица: нить ДНК 3′ - 5′
Субстраты и
источники энергии: АТФ, ГТФ, ЦТФ, УТФ
Направление синтеза: 5′ - 3′ по принципу комплиментарности и антипараллельности
Этапы: инициация, элонгация, терминация
Участвуют факторы инициации, элонгации и терминации
Образуются комплиментарные матрице продукты: мРНК, тРНК, рРНК
Ферменты:
РНК-полимераза I (синтез пре-рРНК)
РНК-полимераза II (синтез пре-мРНК)
РНК-полимераза III (синтез пре-тРНК)
Слайд 29
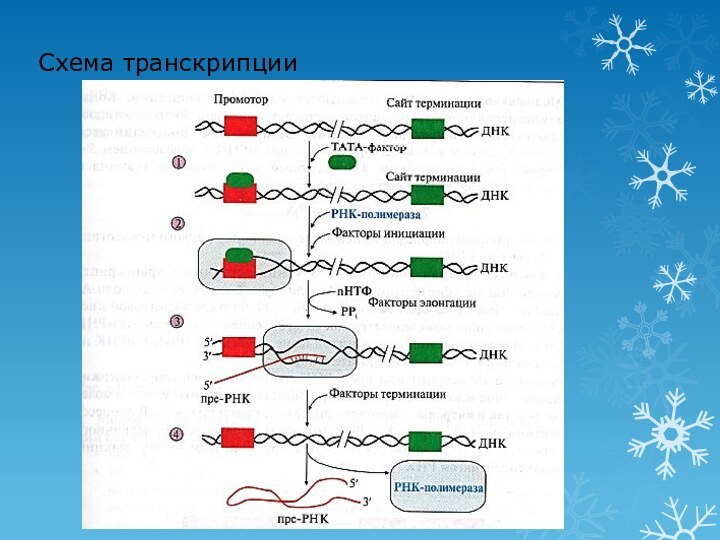
1 этап транскрипции: инициация
Промотор – последовательность ДНК (ТАТА),
с которой связывается РНК-полимераза
Сайт терминации – участок завершения синтеза
РНК
Транскриптон – участок ДНК ограниченный промотором и сайтом терминации
«Активация» промотора с помощью ТАТА-фактора
Взаимодействие промотора с РНК-полимеразой и факторами инициации
Факторы инициации обеспечивают расплетение двойной нити ДНК длиной в один виток (10 н.п.)
Слайд 30
2 этап транскрипции:
элонгация и терминация
Элонгация: рост нити пре-РНК
Факторы
элонгации (E, H, F) повышают активность РНК-полимеразы и облегчают
расхождение цепей. Один ген может одновременно транскрибироваться несколькими молекулами РНК-полимеразы
Терминация: прекращение транскрипции
Факторы терминации облегчают отделение пре-РНК и РНК-полимеразы от матрицы ДНК
Слайд 32
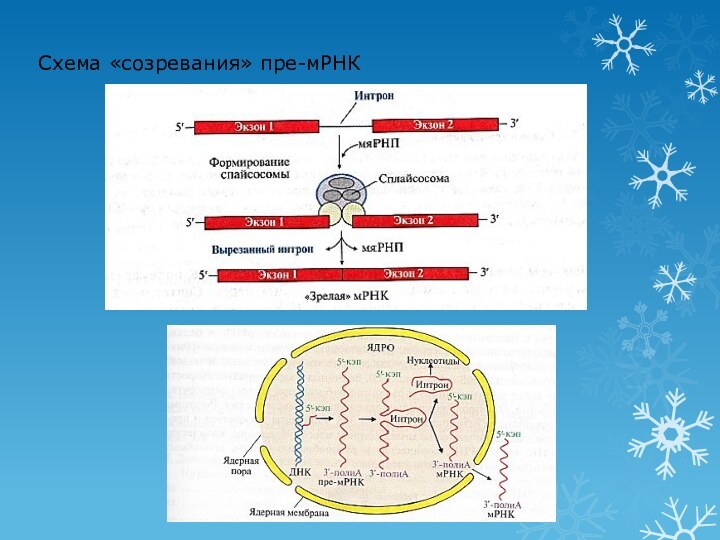
Посттранскрипционные модификации пре-РНК
«Созревание» пре-мРНК
«Кэпирование» на стадии элонгации
Образование поли(А)-
«хвоста» после транскрипции
Сплайсинг – удаление интронов (некодирующих последовательностей) и
соединение экзонов
Участвуют малые ядерные рибонуклеопротеины (мяРНП), образующие комплексы – сплайсосомы
Выход «зрелой» мРНК в цитоплазму
Альтернативный сплайсинг – механизм образования различных видов «зрелой» мРНК из одной и той же молекулы пре-мРНК в разных тканях
В результате в разных тканях при считывании информации с одного и того же гена образуются различные мРНК, а соответственно и различные белки
Слайд 34
«Созревание» пре-тРНК
Удаление интронов
Модификация азотистых оснований (10-15%)
Формирование
акцепторного участка и антикодона
3. Выход зрелых тРНК в цитоплазму
Слайд 36
ТРАНСЛЯЦИЯ: синтез белка
Место синтеза: рибосомы
Матрица: мРНК
Субстраты: аминокислоты (АК) Адапторы: тРНК
Источники энергии:
АТФ, ГТФ
Кофактор: Mg 2+ (стабилизирует структуру рибосом)
Факторы инициации (IF), элонгации (EF), терминации (RF)
Активация АК: связывание с тРНК (аминоацил-тРНК-синтетазы)
Инициирующая аминоацил-тРНК (аа-тРНК): мет-тРНК
Инициирующий кодон мРНК: AUG
Этапы: инициации, элонгации, терминации
Образуется колинеарный матрице продукт – белок (последовательность АК соответствует последовательности кодонов мРНК)
Биологический код: запись информации о последовательности АК в белке с помощью последовательности нуклеотидов
Из школьного курса биологии вспомните и объясните свойства биологического кода!
Слайд 37
Свойства биологического кода
Триплетность
Наличие терминирующих кодонов (UAA, UAG, UGA)
Специфичность
Вырожденность
Универсальность
Однонаправленность
Колинеарность
Слайд 39
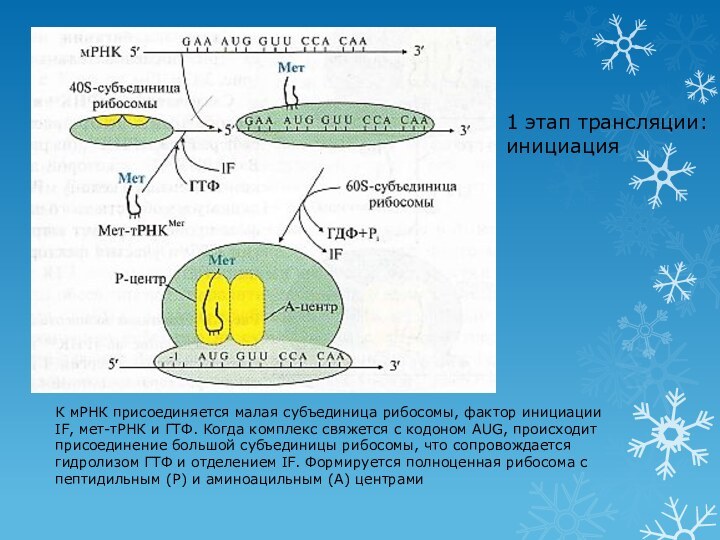
1 этап трансляции: инициация
К мРНК присоединяется малая субъединица
рибосомы, фактор инициации IF, мет-тРНК и ГТФ. Когда комплекс
свяжется с кодоном AUG, происходит присоединение большой субъединицы рибосомы, что сопровождается гидролизом ГТФ и отделением IF. Формируется полноценная рибосома с пептидильным (Р) и аминоацильным (А) центрами
Слайд 40
2 этап трансляции: элонгация (рост пептидной цепи)
Стадии элонгации:
Связывание
аа-тРНК в А-центре при участии фактора элонгации EF1 и
с затратой энергии ГТФ
Образование пептидной связи между АК Р-центра и АК А-центра при участии пептидилтрансферазы
Перемещение рибосомы по мРНК (транслокация) в направлении от 5′- к 3′-концу с использованием энергии ГТФ и при участии фактора элонгации EF2
Многократное повторение стадий
Слайд 41
3 этап трансляции: терминация
Высвобождение пептида из связи
с тРНК
и рибосомой:
Стоп-кодоны UAA, UAG, UGA попадают в А-центр
Высвобождение полипептида
при участии
факторов терминации RF1, RF3 и энергии ГТФ
Слайд 42
Посттрансляционные модификации белков – образование функционально активных белков
Частичный
протеолиз
Фолдинг – формирование пространственной структуры (II, III) при участии
белков-шаперонов
Модификация аминокислот (гликозилирование, фосфорилирование, ацилирование, метилирование……)
Образование дисульфидных связей (цистеин-цистеин)
Присоединение простетической группы (сложные белки)
Сборка протомеров в олигомерные белки (формирование IV структуры)
Слайд 43
Регуляция матричных биосинтезов
Экспрессия генов — процесс, в ходе
которого наследственная информация от гена (последовательности нуклеотидов ДНК) преобразуется
в функциональный продукт — РНК или белок
Гены белков «домашнего хозяйства» (конститутивные) экспрессируются с постоянной скоростью и обеспечивают жизнеспособность клеток (например, гены ферментов энергетического обмена)
Слайд 44
Адаптивная регуляция обеспечивает изменение скорости экспрессии генов в
ответ на меняющиеся условия среды (индуцибельная экспрессия). Осуществляется при
участии:
регуляторных белков, взаимодействующих с участками ДНК
индукторов (стимулируют экспрессию) или корепрессоров (подавляют экспрессию)
Индукторы или корепрессоры стимулируют присоединение регуляторных белков к регуляторным участкам ДНК
В качестве индукторов и корепрессоров выступают гормоны, ростовые факторы, продукты метаболических путей
Регуляторные участки ДНК:
Энхансер – «усилитель» транскрипции
Сайленсер – «тушитель» транскрипции
ПРИМЕР:
ХОЛЕСТЕРИН (как корепрессор) → БЕЛОК-РЕГУЛЯТОР → САЙЛЕНСЕР → ПОДАВЛЕНИЕ ЭКСПРЕССИИ ГМГ-КоА-РЕДУКТАЗЫ (ключевой фермент синтеза холестерина) → СНИЖЕНИЕ СИНТЕЗА ХОЛЕСТЕРИНА
Слайд 45
Примеры ингибиторов матричных биосинтезов
Токсин белой поганки аманитин ингибирует
РНК-полимеразу II (синтез мРНК)
Энтеротоксин возбудителя дифтерии ингибирует трансляцию, модифицируя
фактор элонгации EF2 и нарушая транслокацию рибосом
Интерфероны (гликопротеины лимфоцитов и макрофагов, обладающие противовирусной активностью):
активируют РНК-азу, расщепляющую мРНК и рРНК
стимулируют синтез протеинкиназы, которая фосфорилирует и тем самым инактивирует фактор инициации трансляции IF2
прекращается синтез белков в инфицированных клетках человека, клетка погибает, но останавливается размножение вирусов
Слайд 46
Задание для самостоятельной работы
1. Ознакомиться с принципом метода
полимеразной цепной реакции и его применением в медицине
2. Выяснить
роль нерепарированных изменений ДНК (мутаций) в развитии биохимической индивидуальности человека (полиморфизме генов и белков), наследственных заболеваний, канцерогенезе
3. Найти информацию по теме «Лекарственные препараты – ингибиторы матричных биосинтезов», заполнить таблицу (см. следующий слайд)
Слайд 47
Противоопухолевые и антибактериальные препараты – ингибиторы матричных биосинтезов
Слайд 48
Заключение
Процессы репликации, транскрипции, трансляции (матричные биосинтезы) лежат в
основе «производства» белков и ферментов, функционирование которых является основой
жизни
Регуляция данных процессов лежит в основе адаптации
Нарушение данных процессов приводит к развитию заболеваний
Знания о нуклеиновых кислотах и механизмах матричных биосинтезов являются основой создания лекарственных препаратов, методов диагностики и терапии