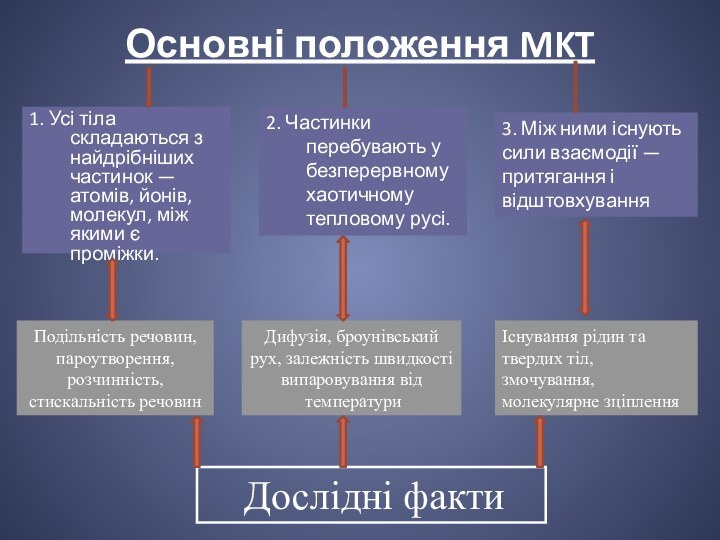
дослідне підтвердження.
Що таке атом (молекула)?
Що називається молярною масою?
Що таке
кількість речовини (одиниці виміру)?Дати визначення поняття концентрації; назвати числове значення сталої Авогадро.
Що називається дифузією; броунівським рухом?
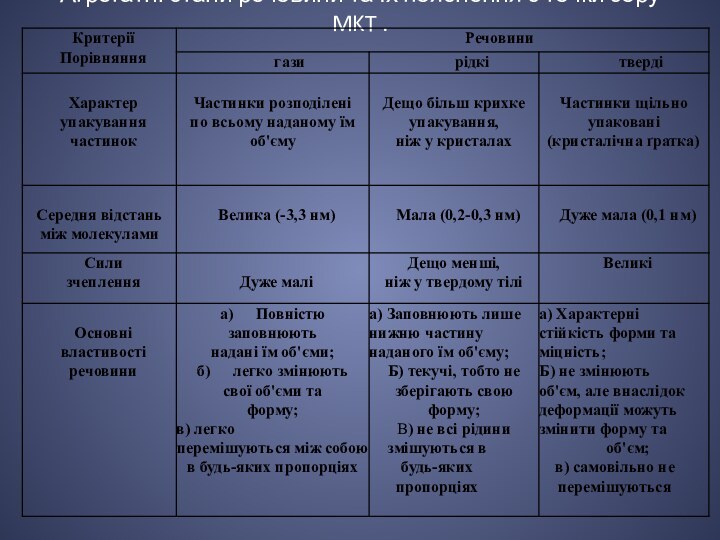
Агрегатні стани речовини та їх пояснення з точки зору MKT (основні властивості).
Швидкість молекул, дослід Штерна.
Основне рівняння MKT; фізичний смисл рівняння.
Температура, теплова рівновага; абсолютний нуль.
Ідеальний газ; параметри, що характеризують ідеальний газ.
Стала Больцмана; універсальна газова стала.
Рівняння стану ідеального газу (Менделєєва-Клапейрона).
Газові закони (ізопроцеси в газах); графіки, що характеризують закони.
Прилади, що вимірюють параметри газів.