- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Пропуск экзона при МДД
Содержание
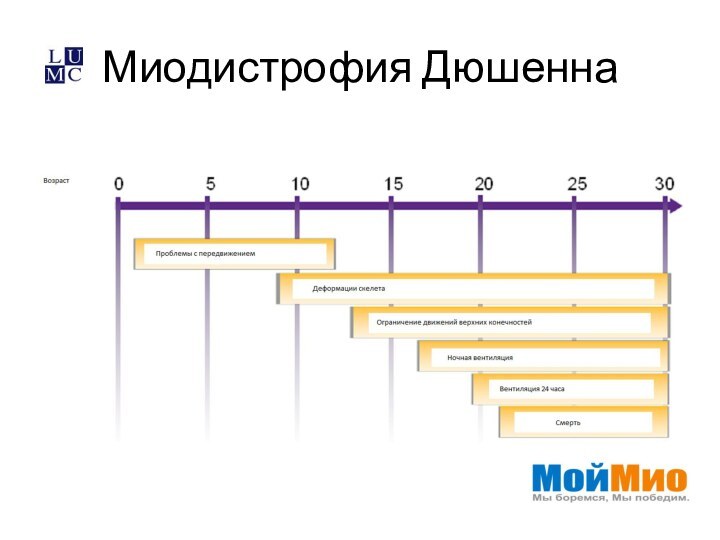
- 2. Миодистрофия Дюшенна
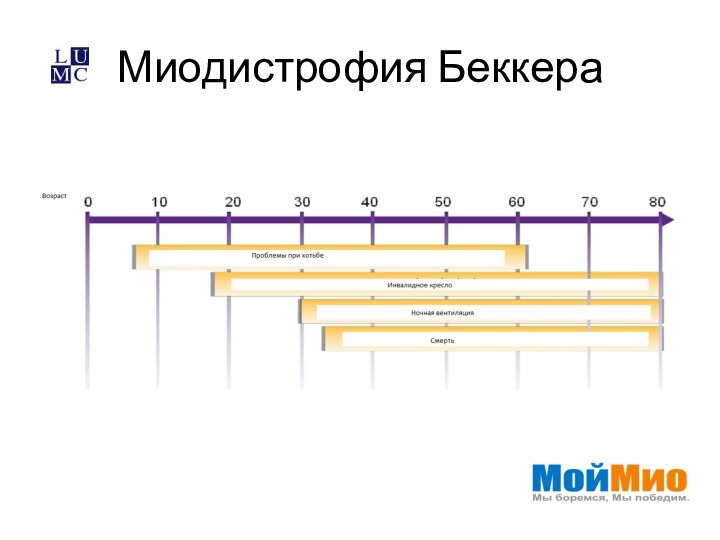
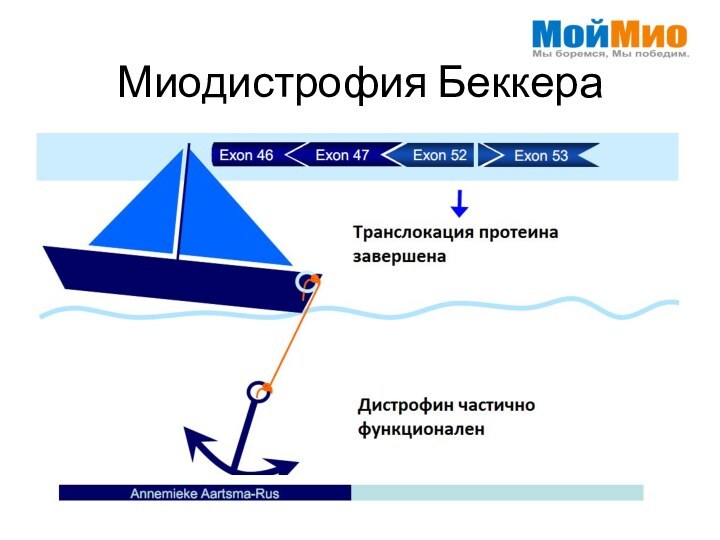
- 3. Миодистрофия Беккера
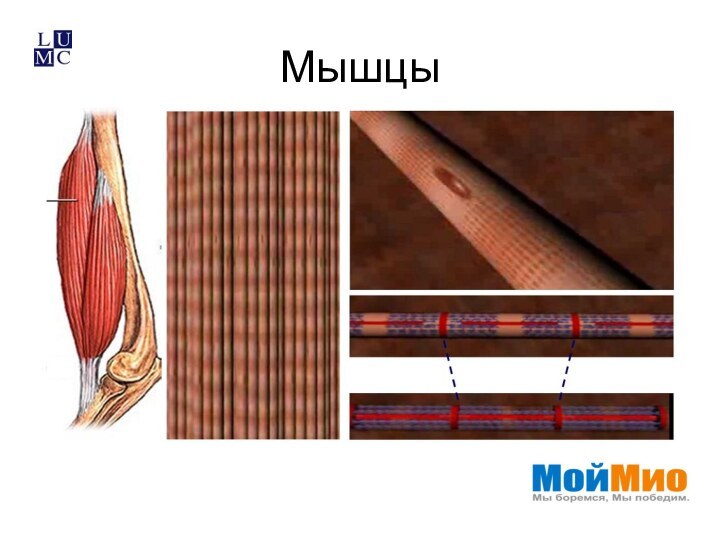
- 4. Мышцы
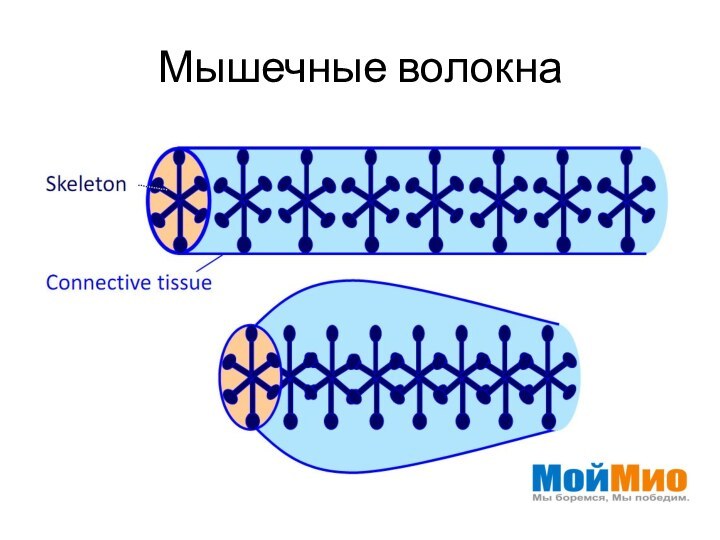
- 5. Мышечные волокна
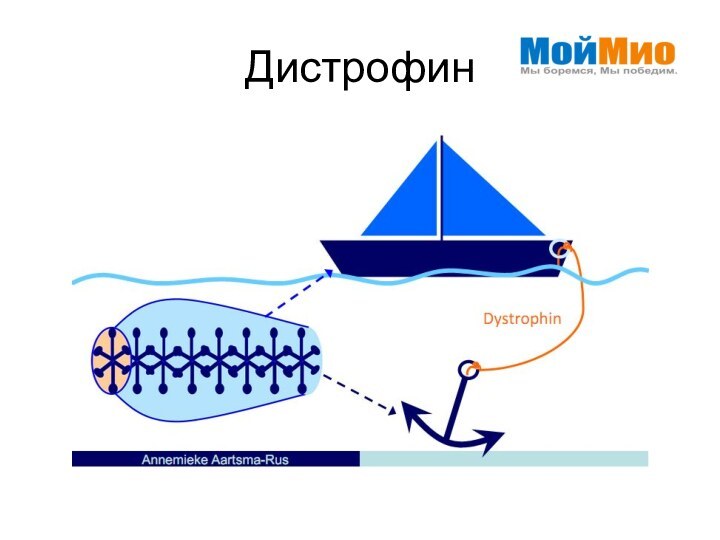
- 6. Дистрофин
- 7. Ген дистрофина
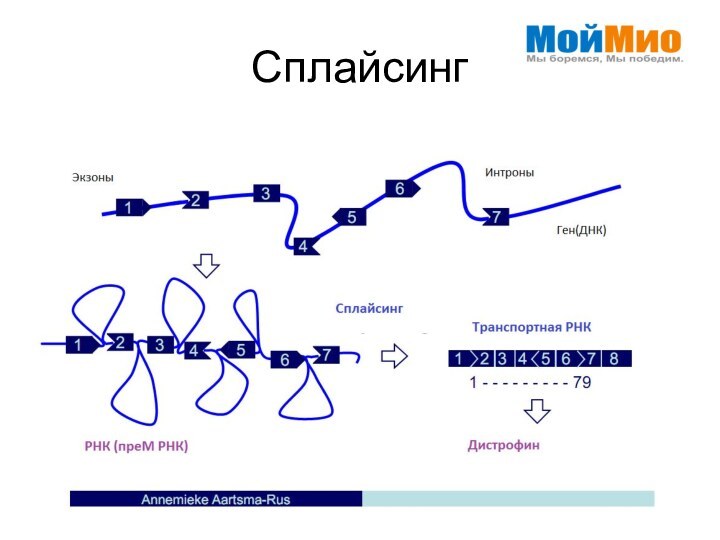
- 8. Сплайсинг
- 9. Нарушение рамки считывания
- 10. Нарушение рамки считывания
- 11. Рамка считывания сохранена. Миодистрофия Беккера
- 12. Миодистрофия Беккера
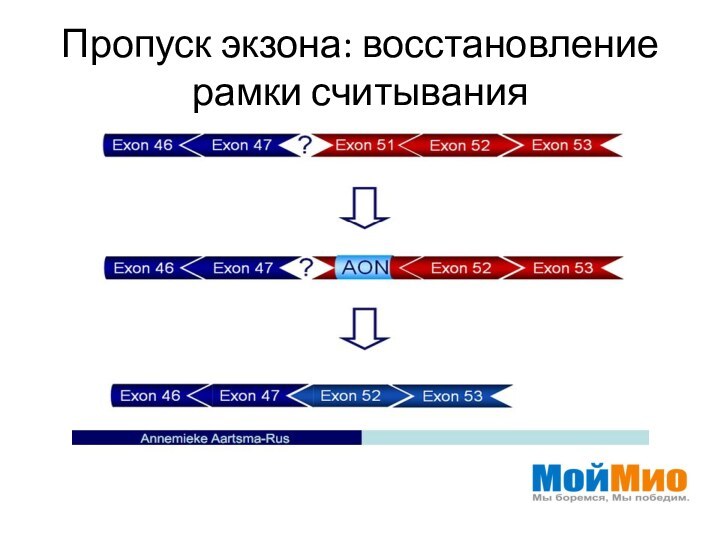
- 13. Пропуск экзона: восстановление рамки считывания
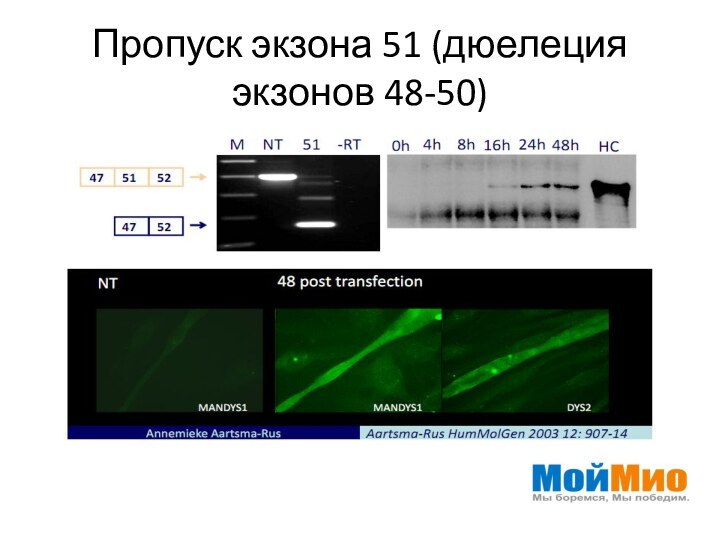
- 14. Пропуск экзона 51 (дюелеция экзонов 48-50)
- 15. MDX мышиЕстественная модельДелеция экзона 23Дефицит дистрофинаНарушение мышечной
- 16. Пропуск экзонаПропуск экзона и синтез дистрофина подтверждены
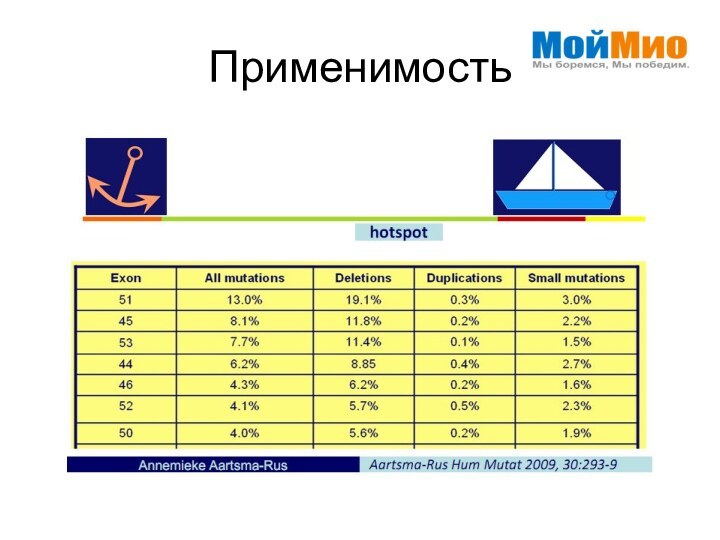
- 17. Применимость
- 19. Первые клинические испытания Одна доза, один центр
- 20. Первые клинические испытания
- 22. Внутримышечные исследованияПропуск экзона у всех пациентовНе наблюдалось токсических эффектовУровень дистрофина 17-35%Уровень дистрофин-положительных волокон 64-97%Необходимо системное лечение
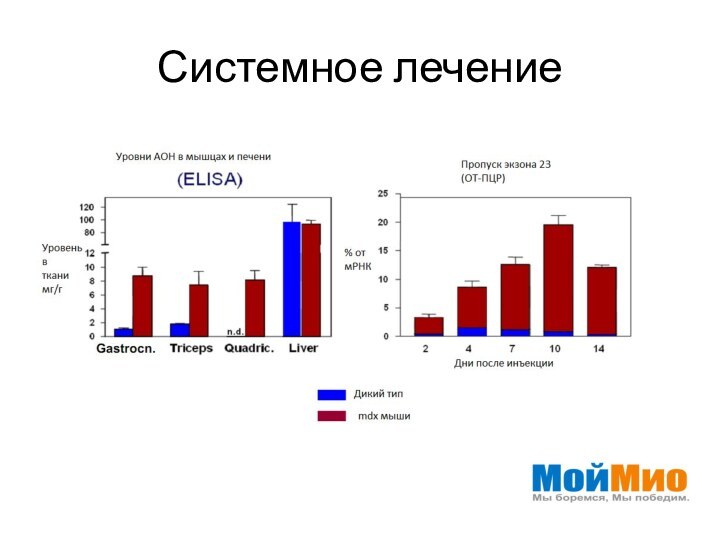
- 23. Системное лечение
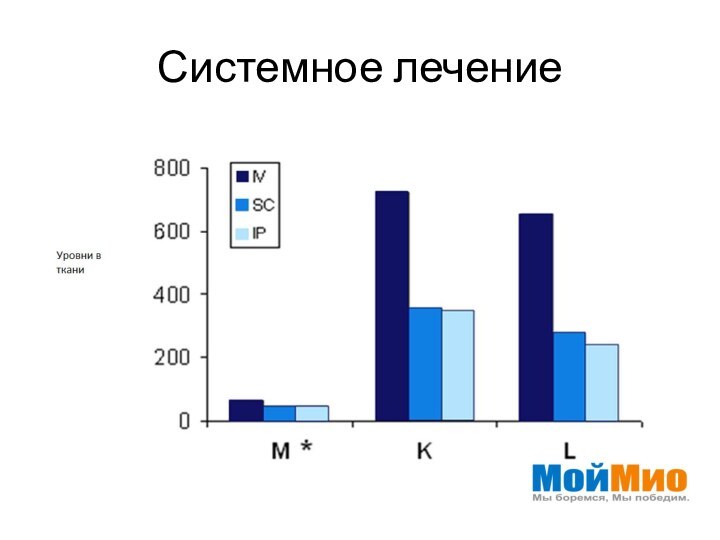
- 24. Системное лечение
- 25. Системное исследование 2OMEPS (GSK|Prosena)Подкожные инъекцииЕженедельно 5 недель3
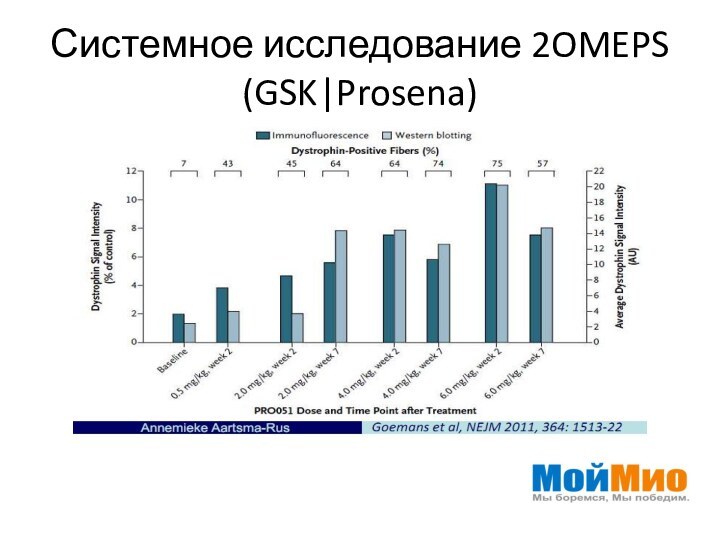
- 26. Системное исследование 2OMEPS (GSK|Prosena)
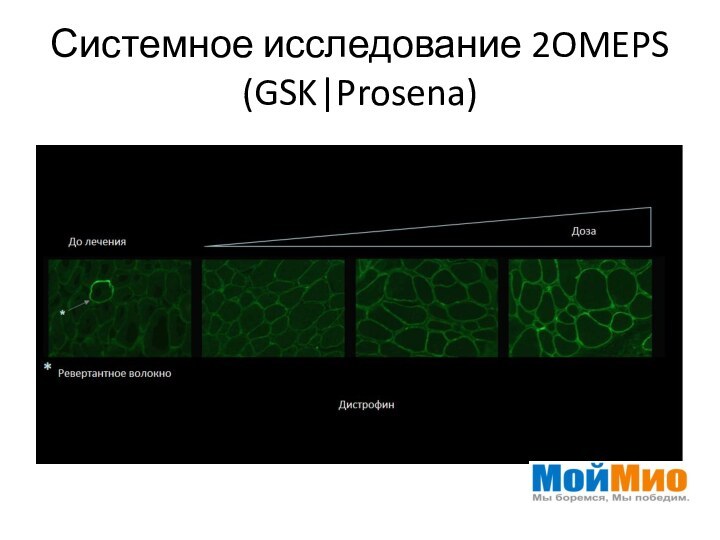
- 27. Системное исследование 2OMEPS (GSK|Prosena)
- 28. Характеристики субъектовВсе 12 пациентов начали исследованиеСтадия МДДНе
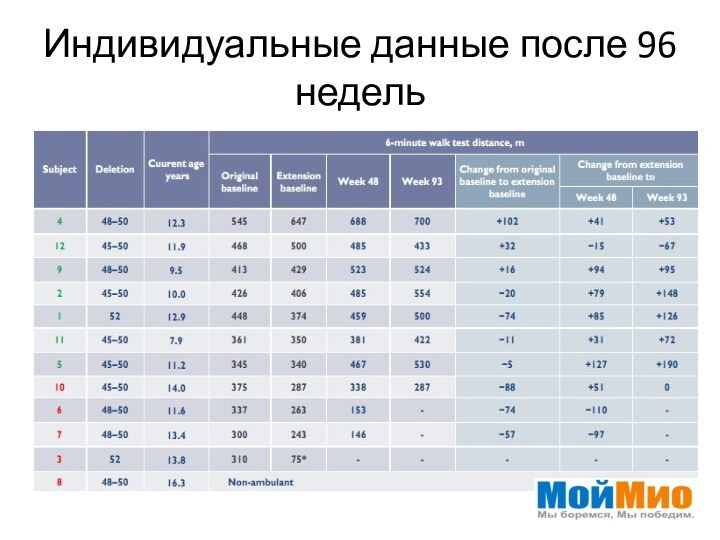
- 29. Индивидуальные данные после 96 недель
- 30. Безопасность и переносимость после 96недельМестные реакции на
- 31. Безопасность и переносимость после 96недельЛабораторные данные (продолжение) Снижение C3 (
- 32. В итоге:GSK2402968 как правило, хорошо переносится после
- 33. Планируемые последующие исследования Пропуск экзона 51Исследования пациентов
- 34. Скачать презентацию
- 35. Похожие презентации
Миодистрофия Дюшенна

















Слайд 15
MDX мыши
Естественная модель
Делеция экзона 23
Дефицит дистрофина
Нарушение мышечной функции
Меньшие
проявления болезни, чем у человека
синтез дистрофина и функциональные нарушения после внутримышечной инъекции АОН
Слайд 16
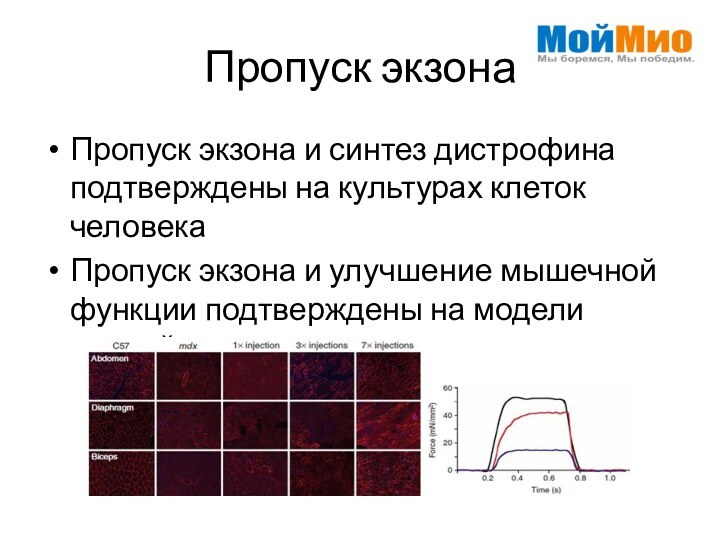
Пропуск экзона
Пропуск экзона и синтез дистрофина подтверждены на
культурах клеток человека
Пропуск экзона и улучшение мышечной функции подтверждены
на модели мышей
Слайд 19
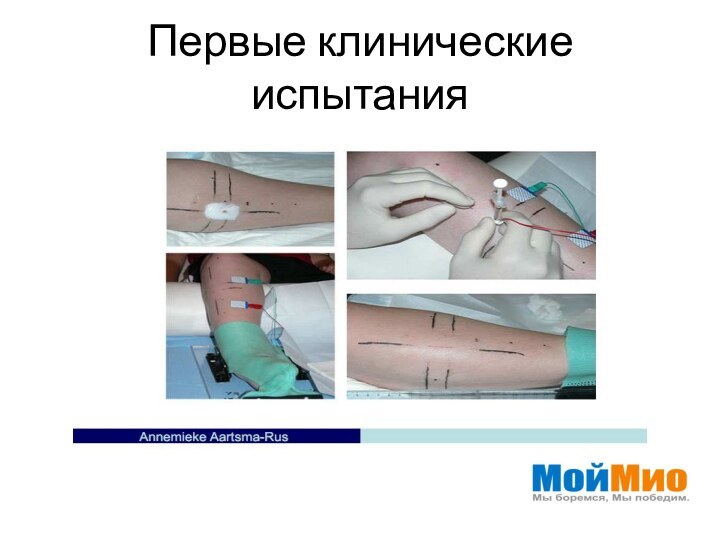
Первые клинические испытания
Одна доза, один центр исследования
4
пациента в возрасте 8-16 лет
Одна инъекция препарата в мышцы
Биопсия
через 4 неделиПропуск экзона? Дистрофин? Безопасность?
Слайд 22
Внутримышечные исследования
Пропуск экзона у всех пациентов
Не наблюдалось токсических
эффектов
Уровень дистрофина 17-35%
Уровень дистрофин-положительных волокон 64-97%
Необходимо системное лечение
Слайд 25
Системное исследование 2OMEPS (GSK|Prosena)
Подкожные инъекции
Еженедельно 5 недель
3 пациента
в группе
Биопсия через месяц после последней инъекции
Не сообщалось о
побочных эффектахОткрытое исследование
Все пациенты получили 6 мг\кг подкожно
Слайд 28
Характеристики субъектов
Все 12 пациентов начали исследование
Стадия МДД
Не передвигающийся
самостоятельно- 1
Стабильные, способные к передвижению – 7
Способные к передвижению
с признаками ухудшения- 4Все принимали стероиды один год до исследования
Слайд 30
Безопасность и переносимость после 96недель
Местные реакции на введение
12
Включают признаки воспаления и пигментацию
Развивались после длительного введения и
были у всех пациентовВо всех случаях реакции считались слабыми
Лабораторные данные
Почки
Увеличение в моче альфа 1 макроглобулина 12
Свидетельство об обратимости процесса(73-80 недель, 89-92)
Переменная протеинурия по спот-образцам мочи (n = 12)- Подтвержденная в последующей 24-часовой моче (n = 4) все> 0,15 г/24 часа, но <0,3 г/24
Повышение уровня цистатина C (> ULN) (п = 6)
Печеночная
Повышение (> ULN) гглутамилтрансферазы (п = 3)
Гематологии и коагуляция
Снижение тромбоцитов (п = 3)
Слайд 31
Безопасность и переносимость после 96недель
Лабораторные данные (продолжение)
Снижение
C3 (
(24 недель)Клинически значимые эффекты не обнаружены с помощью эхокардиографии или ЭКГ
4 серьезных осложнения не связанных с лечением
5 субъектов имели 1 или 2 перерыва в лечении
Снижение тромбоцитов (п = 3)
Изменения почечных маркеров (п = 1)
Изменения почечных / печеночных маркеров (п = 1)
Воспалительные реакции (п = 2)
Слайд 32
В итоге:
GSK2402968 как правило, хорошо переносится после 96
недель
Нарушение функции почек, тромбоцитов и местные реакции в месте
инъекции обуславливает продолжение мониторинга. Обратимость почечных эффектов в период отсутствия лечения
Учитывая ожидаемое развитие болезни, обнадеживающие результаты шестиминутного теста наблюдалось у 7 из 10 мальчиков(P4.27)
Плацебо-контролируемые исследования (DMD114117 и DMD114044) в настоящее время продолжаются
Слайд 33
Планируемые последующие исследования
Пропуск экзона 51
Исследования пациентов неспособных
передвигаться в США (GSK / Prosensa)
Исследования Доза /Частота продолжаются
(GSK / Prosensa)Фаза 3 испытания (GSK / Prosensa)
Пропуск экзона 44 фазы I / II продолжаются (Prosensa)
Планируется исследование пропуска экзонов 45 и 53 (Prosensa)
Оптимизация пропуска других экзонов (52 и 55)