и т.д., R= 3,21015ּ Гц
R - "постоянная Ридберга"
Из коллекции www.eduspb.com
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть
















Из коллекции www.eduspb.com
Из коллекции www.eduspb.com
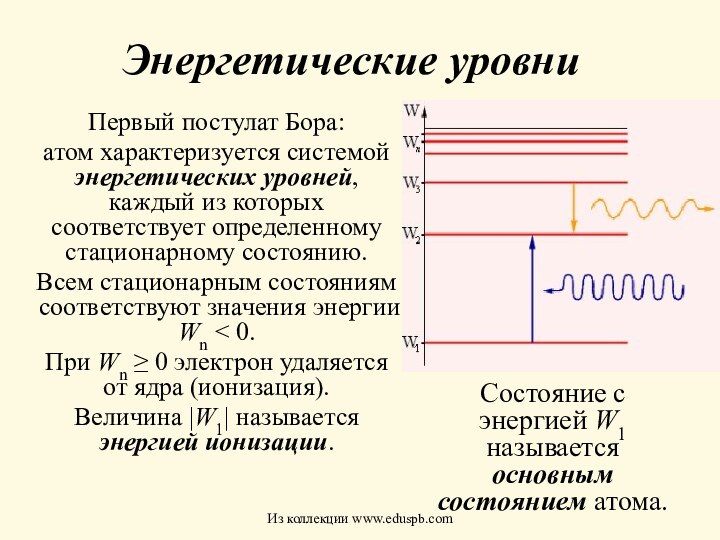
Состояние с энергией W1 называется основным состоянием атома.
Из коллекции www.eduspb.com
Из коллекции www.eduspb.com
Момент импульса
Постоянная Планка
Из коллекции www.eduspb.com