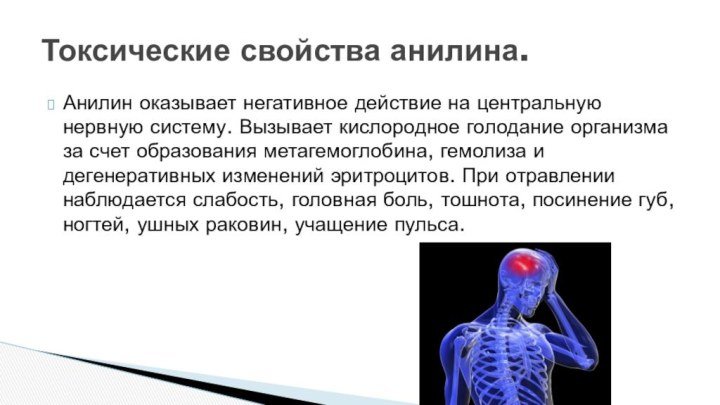
с щелочью синяя окраска индигоисчезает и образуется вязкая масса
коричневого цвета. Очистив это в-во, Фрицше получил быстро желтеющую на воздухе маслянистую жидкость и назвал её анилином.Примерно в то же время О.Унфердорбен нагреванием кристаллического индиго получил продукт, который он назвал кристаллином.
Фридлиб Фердинанд Рунге в продуктах перегонки каменноугольной смолы открыл в-во, названное им кианолом.
Н.Н.Зинин в 1841 году открыл способ восстановления нитробензола до соответствующего ароматического амина – бензидама.
1843 г. – Гофман установил, что бензидам, кианол, кристаллин и анилин – одно и то же соединение. Остановились на анилине.
История создания



![Презентация по химии Применение анилина Нитрование: C6H5NH2+NaNO2+2HCl [C6H5-NN]+Cl- +NaCl + 2H2O хлорид диазония Диазосоединения можно выделить](/img/tmb/6/510287/d11680106d793ae7d4ded62dfc95a932-720x.jpg)