- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Решение задач по теме Массовая доля
Содержание
- 2. ДЕВИЗ УРОКА: «Только из союза
- 3. ЦЕЛИ УРОКА: Объединить знания по химии
- 4. ТЕМА УРОКА: «Массовая доля растворенного вещества в растворе.»
- 5. « Что такое доля?».« Мы делили апельсин, много нас , а он один….»
- 6. Актуализация знаний и умений Что такое доля?
- 7. Выполните задание №1 на листе «Заполните таблицу»,
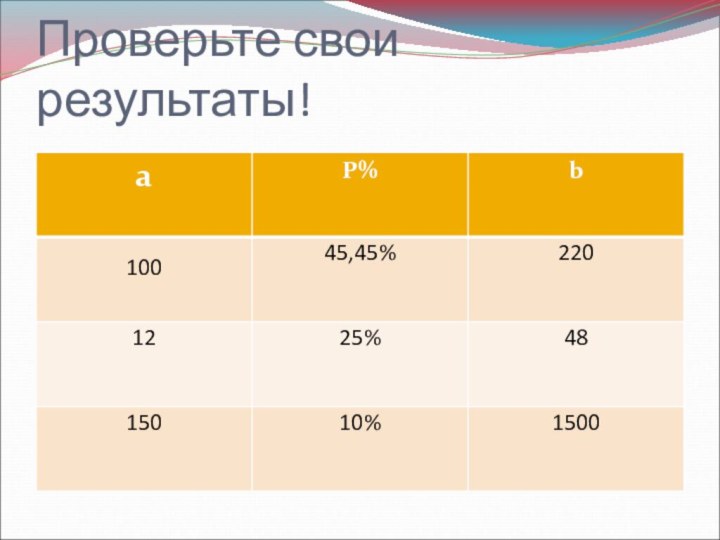
- 8. Проверьте свои результаты!
- 9. Изучение нового материала. Демонстрационный эксперимент. Чем отличаются эти растворы?Масса растворенного вещества в растворах различна
- 10. Роль растворов в природе. 1) 97
- 11. Тело медузы состоит на 99.9% изводы
- 12. 70% - массовая доля воды в организме млекопитающих.
- 13. Первичный океан содержал, по мнению ученых 1% солей.
- 14. Массовая доля солей в крови человека 0,9%.
- 15. Природные воды, живые организмы, бытовые и промышленные жидкости – это растворы.
- 16. Компоненты раствораРаствор = растворенное вещество +
- 17. Выполните задание № 2 «Заполните таблицу»
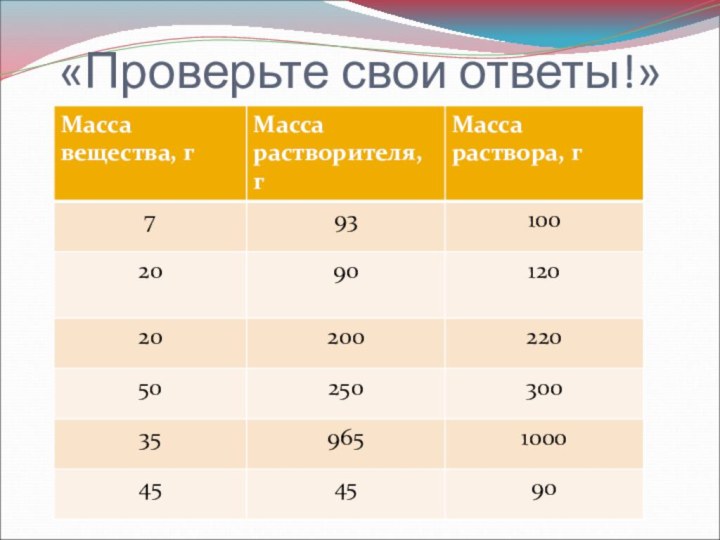
- 18. «Проверьте свои ответы!»
- 19. Формула для расчета массовой доли растворенного веществаω=
- 20. Как найти массу раствора?m раствора = m
- 21. Как найти массу растворенного вещества?m растворенного вещества = ω * m раствора 100%
- 22. Физкультпауза . «Глядя на слова произнесите вслух цвета, которыми эти слова написаны, как можно быстрее! Удачи!!!»
- 23. Решите задачу:Задача №1 Рассчитайте массовую долю
- 24. Объясните, что означает запись? 100г 36%
- 25. Проверьте свои результаты:36 г соли растворено в
- 26. Демонстрационный эксперимент. Перед вами два новых
- 27. Решите задачу №2:Рассчитайте массу растворенного вещества в
- 28. Демонстрационный эксперимент Дольем воды в исходные растворы.
- 29. Решите задачу № 3.Масса первого раствора стала
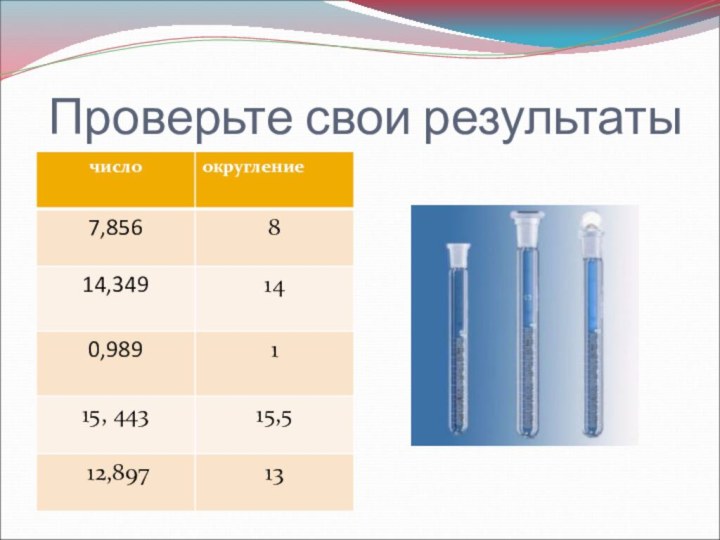
- 30. Заполните таблицу 3. Выполните округление данных чисел до разряда десятых.
- 31. Проверьте свои результаты
- 32. Для чего нужны знания о массовой доле?
- 33. Зарядка для глаз «Посмотрите внимательно в центр картинки»
- 34. Самостоятельная работа. Контроль знаний. Задачи первого уровня1
- 35. Задачи второго уровня1 вариант Определите массу
- 36. Задачи третьего уровня 1 вариантК 150 г
- 37. Итог урока. Рефлексия знаний. Вопросы к учащимся
- 38. Скачать презентацию
- 39. Похожие презентации
ДЕВИЗ УРОКА: «Только из союза двух работающих вместе и при помощи друг друга рождаются великие вещи» Антуан































Слайд 3
ЦЕЛИ УРОКА:
Объединить знания по химии и математике
в теме «Доля» при решении расчетных задач.
Выяснить, для чего
нужны знания о массовой доле в повседневной жизни человека.
Слайд 6
Актуализация знаний и умений
Что такое доля?
Чем
она может быть выражена?
Какое еще понятие тоже дает
нам представление о части от числа? Что такое процент?
Как найти число, если известно, сколько процентов оно составляет от целого?
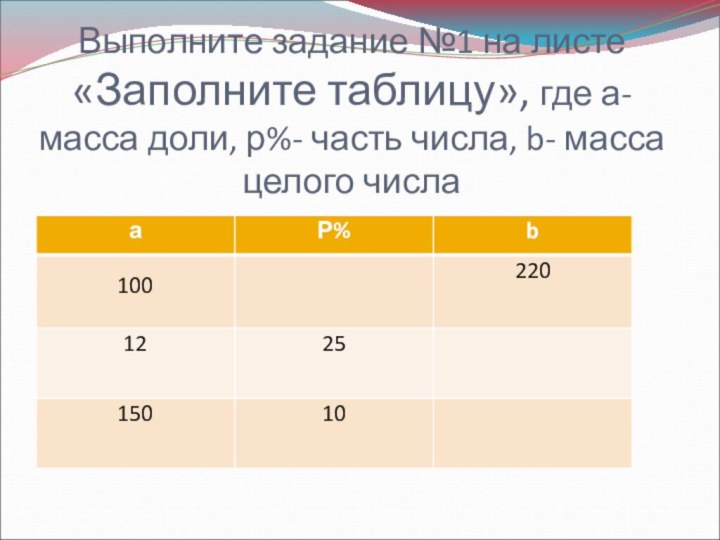
Слайд 7 Выполните задание №1 на листе «Заполните таблицу», где
а- масса доли, р%- часть числа, b- масса целого
числа
Слайд 9
Изучение нового материала.
Демонстрационный эксперимент.
Чем отличаются эти растворы?
Масса
растворенного вещества в растворах различна
Слайд 10 Роль растворов в природе. 1) 97 % поверхности земного
шара занимают океаны и моря, 3% - озера,
реки, подземные воды. Роль растворов в природе. 90% воды содержат плоды огурца, арбуза
Слайд 16
Компоненты раствора
Раствор =
растворенное вещество + растворитель
m
раствора=
m растворенного вещества+ m растворителя
Что чаще всего используется
в качестве растворителя?Приведите несколько примеров водных, спиртовых растворов, которые использует человек.
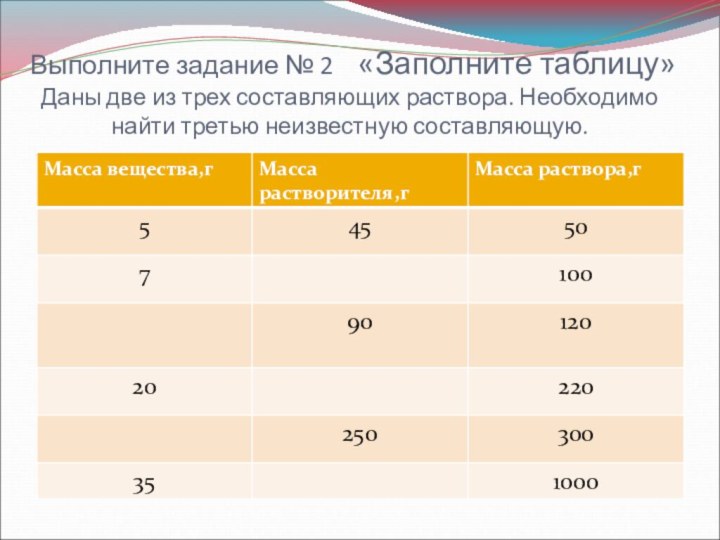
Слайд 17 Выполните задание № 2 «Заполните таблицу» Даны две
из трех составляющих раствора. Необходимо найти третью неизвестную составляющую.
Слайд 19
Формула для расчета массовой доли растворенного вещества
ω= m
растворенного вещества *100%
m раствораСлайд 22 Физкультпауза . «Глядя на слова произнесите вслух цвета,
которыми эти слова написаны, как можно быстрее! Удачи!!!»
Слайд 23
Решите задачу:
Задача №1
Рассчитайте массовую долю медного
купороса в двух растворах, если масса растворов - 100
г , причем в первом из них растворено 10 г соли, а во втором – 2 г.Ответ: 10%, 2%.
Слайд 24
Объясните, что означает запись?
100г 36% раствора
100г 12%
раствора
50 г 7% раствора
20 г 10% раствора
56г 12 %
раствора смешали с 56 г 24% раствора. Какова массовая доля в полученном растворе?45 г 17% раствора смешали с 70 г 26% раствора. Какова массовая доля в полученном растворе?
Слайд 25
Проверьте свои результаты:
36 г соли растворено в 64
г воды
12 г соли растворено в 88 г воды
3,5
г соли растворено в 46,5 г воды2 г соли растворено в 18 г воды
ω = 56*0,12+56*0,24/ 112= 0,18 или 18%
ω= 45*0,17+70*0,26/ 115 = 0,22 или 22%
Слайд 26
Демонстрационный эксперимент.
Перед вами два новых раствора.
В чем
отличия этих растворов?
Интенсивность окраски одинакова, значит концентрация одинакова, но
различна масса растворов.)
Слайд 27
Решите задачу №2:
Рассчитайте массу растворенного вещества в двух
растворах, если масса первого - 80 г, второго
- 50 г, массовая доля растворенной соли равна 15 % в каждом растворе.Ответ: 12г, 7,5г
Слайд 28
Демонстрационный эксперимент
Дольем воды в исходные растворы.
В первый - 100 мл, а во второй –
50мл. Как изменились растворы внешне? Что произошло с концентрацией растворов?
Слайд 29
Решите задачу № 3.
Масса первого раствора стала равна
180 г, а второго 100 г. А масса растворенного
вещества при этом не изменилась. Рассчитаем массовую долю в полученных растворах.ω 1 =12/ 180 *100% = 6,67%
ω 2 = 7,5/ 100 * 100% = 7,5%
Слайд 34
Самостоятельная работа. Контроль знаний.
Задачи первого уровня
1 вариант
Определите
массовую долю соли в растворе, если для его приготовления
взяли 80 г воды и 20 г соли.Ответ: а) 20%; б) 25%; в) 30%; г) 10%.
2 вариант
Определите массовую долю сахара в растворе, если для его приготовления взяли 120 г воды и 30 г сахара.
Ответ: а) 15%; б) 25%; в) 10%; г) 20%.
Слайд 35
Задачи второго уровня
1 вариант
Определите массу сахара, который
нужно растворить в 1000 г воды, чтобы получился раствор
с массовой долей сахара 20%.Ответ: а) 8 г; б) 80 г; в) 0,8 г; г) 18 г.
2 вариант
Определите массу сухой соли, которая образуется в чашке после выпаривания 150 г раствора с массовой долей этой соли 15%.
Ответ: а) 22,5 г; б) 20 г; в) 100 г; г) 2,25 г.
Слайд 36
Задачи третьего уровня
1 вариант
К 150 г 20
%-ого раствора соляной кислоты прилили 200 мл воды. Каково
процентное содержание соляной кислоты во вновь полученном растворе?Ответ: а) 5%; б) 8,57%; в) 7%; г) 0,85%.
2 вариант
К 200 г 40 %-ого раствора серной кислоты прилили 80 мл воды. Каково процентное содержание серной кислоты во вновь полученном растворе?
Ответ: а) 2,86%; б) 28,6%; в) 35%; г) 23%.
Слайд 37
Итог урока. Рефлексия знаний.
Вопросы к учащимся :
-
Пригодятся ли эти знания в жизни?
- Все ли было
понятно?- Какие трудности возникли?
- Понравилось ли вам работать на уроке?
Оценки за урок.





























