- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему по химии на тему Алюминий(9класс)
Содержание
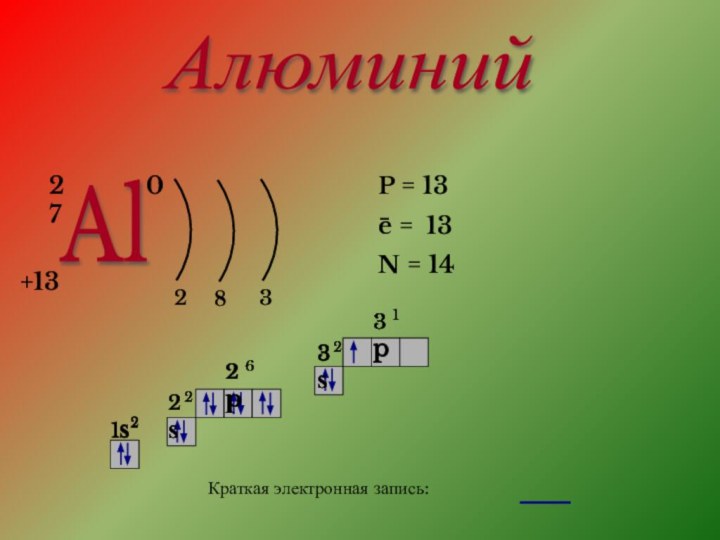
- 2. Алюминий Al 27+130283P = 13e = 13N = 14−Краткая электронная запись:
- 3. Физические свойстваплавления 660°С. Пластичен, легко Чистый алюминий
- 4. Химические свойства 2Al+3O2Al2O3+3Cl22AlCl3+3SAl2S3+6HCl2AlCl3 + 3H2+3CuSO4Al2(SO4)3 + 3Cu
- 5. Химические свойства Является амфотерным элементом: взаимодействует с
- 6. ПОЛУЧЕНИЕВпервые алюминий был получен в 1821 г. в Германии
- 7. ПРИМЕНЕНИЕОсновным преимуществом использования алюминиевых сплавов является их
- 8. Скачать презентацию
- 9. Похожие презентации
Алюминий Al 27+130283P = 13e = 13N = 14−Краткая электронная запись:







Слайд 3
Физические свойства
плавления 660°С. Пластичен, легко Чистый алюминий —
серебристо-белый легкий металл,вытягивается в проволоку и раскатывается в листы
и фольгу. Является хорошим проводником электричества и тепла (после серебра и меди). Сплавы алюминия с различными металлами обладают высокой прочностью и легкостью.
Слайд 5
Химические свойства
Является амфотерным элементом: взаимодействует с кислотами
и со щелочами.
2Al + 6HCl = 2AlCl3 + 3H2
2Al
+ 2NaOH + 2H2O = 2NaAlO2 + 3H2Оксид и гидроксид алюминия также обладают амфотерными свойствами:
Al2O3 + 6HCl = 2AlCl3 + 3H2O
Al2O3 + 2NaOH = 2NaAlO2 + H2O
2Al(OH)3 + 6HCl = 2AlCl3 + 6H2O
Al(OH)3 + NaOH = NaAlO2 + 2H2O





























