свет По числу семи планет: Медь, железо, серебро… Дал нам Космос на
добро. Злато, олово, свинец… Сын мой, сера – их отец. А еще ты должен знать: Всем им ртуть – родная мать.Самородная медь
Самородок серебра
Железный метеорит
Самородок золота
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть








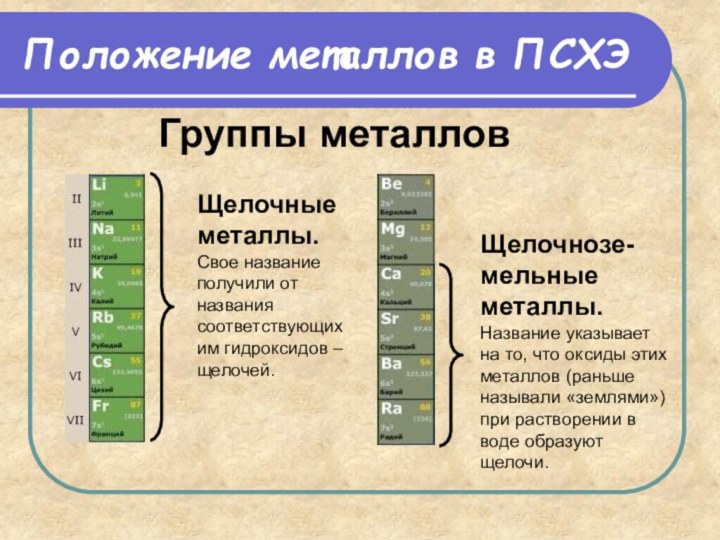






























Самородная медь
Самородок серебра
Железный метеорит
Самородок золота
Украшение из меди
?
Самородок меди
понижение
Au Ag Cu Sn Pb Zn… Bi Mn
понижение
В-ль ок-ль
Смешанный оксид железа II - III
В-ль ок-ль
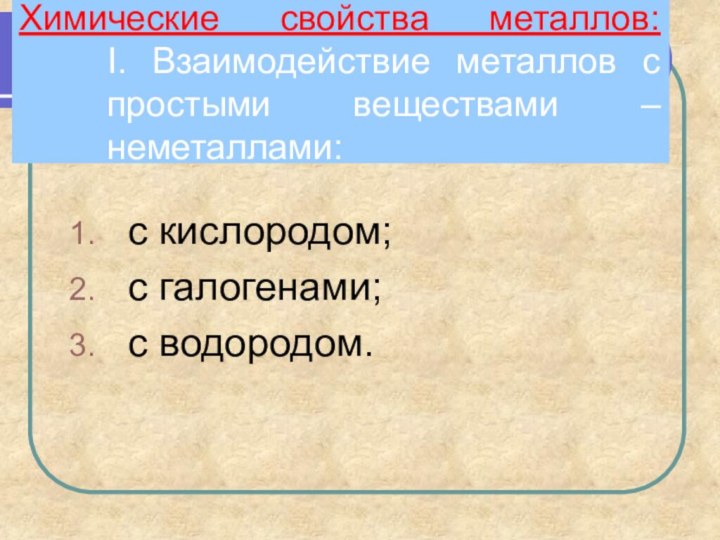
с кислородом не взаимодействуют, т.е. не окисляются