Слайд 2
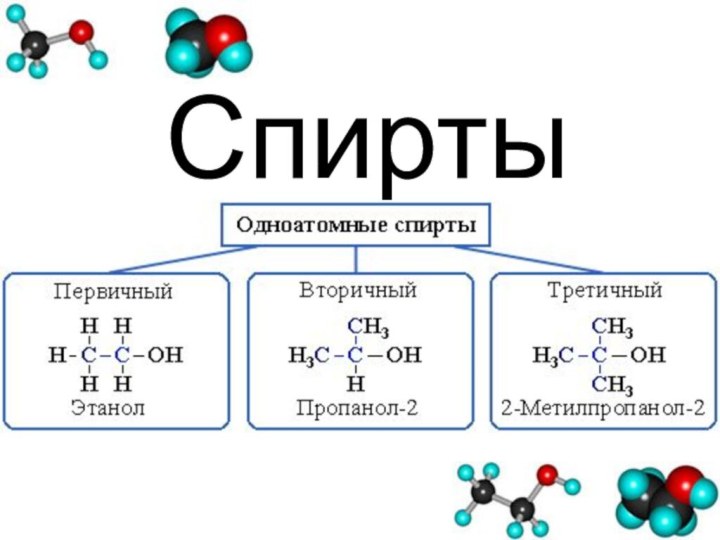
Предельные одноатомные спирты (алканолы)
CnH2n+1OH
или R – OH
Номенклатура:
название углеводорода + ол:
этан + ол = этанол
Изомерия:
1) углеродного скелета;
2) положения функциональной
гидроксильной группы;
3) межклассовая изомерия – простые эфиры:
C2H5OH этанол – спирт, а диметиловый эфир
–межклассовый изомер CH3 – O – CH3
Слайд 3
Физ. свойства:
Даже первый спирт – жидкость;
C1-C11
- жидкости, хорошо растворимы в воде, летучи, имеют запах,
с C12 – твердые, без запаха,
не растворимы в воде,
между молекулами возможно образование
водородных связей.
Слайд 4
Химические свойства:
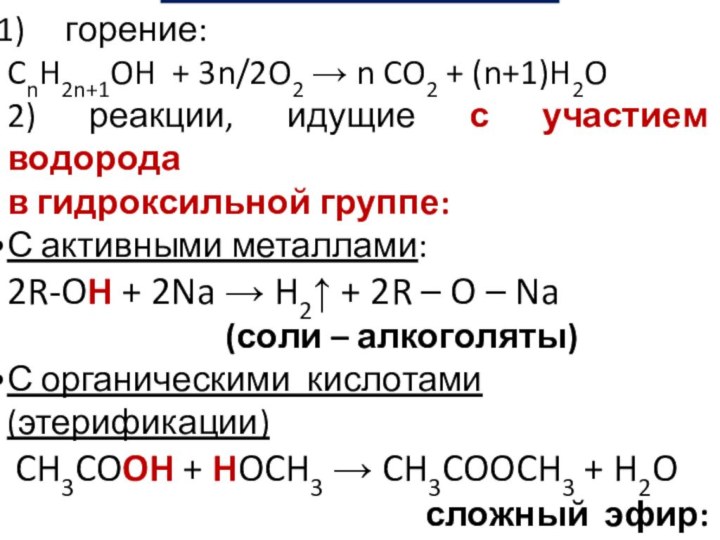
горение:
CnH2n+1OH + 3n/2O2 n CO2
+ (n+1)H2O
2) реакции, идущие с участием водорода
в гидроксильной
группе:
С активными металлами:
2R-OH + 2Na H2 + 2R – O – Na (соли – алкоголяты)
С органическими кислотами (этерификации)
CH3COOH + HOCH3 CH3COOCH3 + H2O
сложный эфир: метилацетат)
Слайд 5
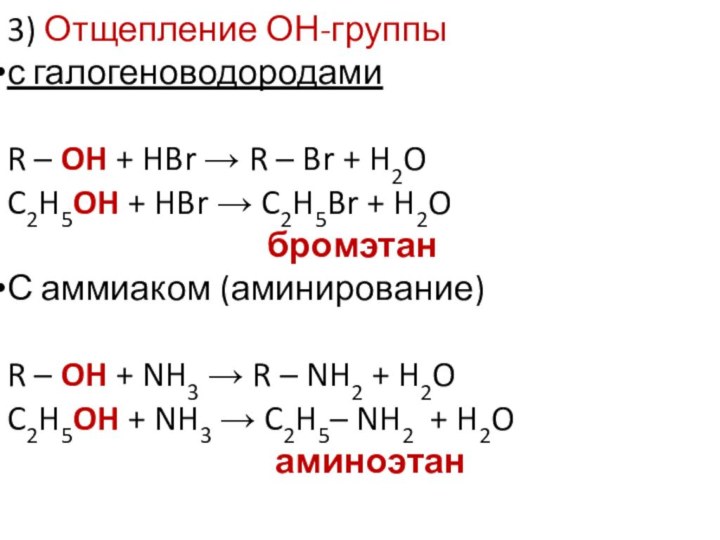
3) Отщепление ОН-группы
с галогеноводородами
R – OH +
HBr R – Br + H2O
C2H5OH + HBr
C2H5Br + H2O
бромэтан
С аммиаком (аминирование)
R – OH + NH3 R – NH2 + H2O
C2H5OH + NH3 C2H5– NH2 + H2O
аминоэтан
Слайд 6
4) реакции с участием группы «ОН»
Окисление:
Первичные спирты
окисляются в альдегиды:
O
//
C2H5OH + CuO CH3 – C + Cu + H2O
\
H этаналь
Вторичные спирты окисляются в кетоны
CH3 – CH– CH3 + CuO CH3–C–CH3 + Cu + H2O
| ||
OH O пропанон
Слайд 7
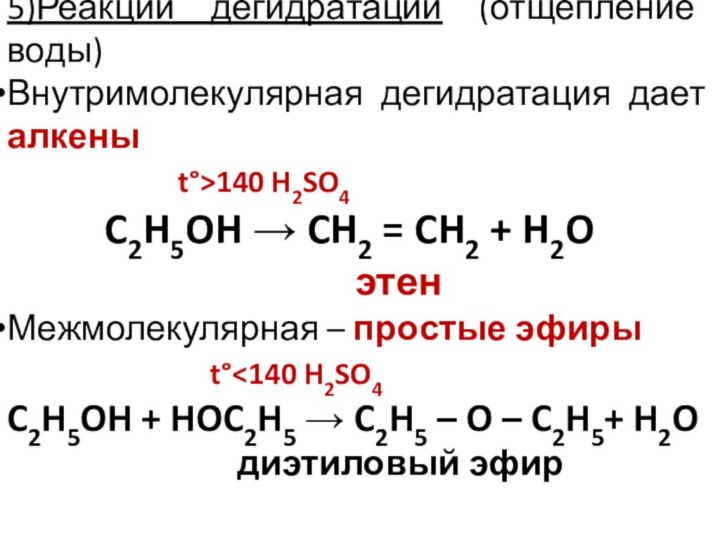
5)Реакции дегидратации (отщепление воды)
Внутримолекулярная дегидратация дает алкены
t°>140 H2SO4
C2H5OH CH2 = CH2 + H2O
этен
Межмолекулярная – простые эфиры
t°140 H2SO4
C2H5OH + HOC2H5 C2H5 – O – C2H5+ H2O
диэтиловый эфир
Слайд 8
Получение спиртов:
Гидратация алкенов:
CH2=CH2 +HOH CH3 –CH2OH
2)
щелочной гидролиз галогеналканов
C2H5Cl + KOH (водный) C2H5OH + KCl
3)
восстановление альдегидов:
CH3COH + H2 C2H5OH
4) брожение глюкозы:
C6H12O6 2CO2 + 2C2H5OH
5) Из синтез-газа для метанола:
CO + 2H2 CH3OH
Слайд 9
Бутанол-1 образует сложный эфир при взаимодействии с
1) пропанолом
2)
метаналем
3) муравьиной кислотой
4) соляной кислотой
Слайд 10
При окислении метанола образуется:
метан
метаналь
3) уксусная кислота
4) хлорметан
Слайд 11
Одноатомные предельные спирты
не вступают в реакцию:
1) этерификации
2)
гидрирования
3) дегидратации
4) замещения
Слайд 12
При нагревании метанола с концентрированной серной кислотой образуется
1)
диметиловый эфир
2) метановая кислота
3) формальдегид
4) метан
Слайд 13
Сложный эфир образуется при взаимодействии этанола с
1) CH3COOH
2)
CH3OH
3) HBr
4) KMnO4
Слайд 14
Гидроксильная группа имеется в молекулах:
1) спиртов и карбоновых
кислот
2) альдегидов и простых эфиров
3) аминокислот и сложных эфиров
4)
жиров и спиртов
Слайд 15
Многоатомные спирты, в отличие от одноатомных спиртов, могут
реагировать с:
1) гидроксидом меди (II)
2) щелочными металлами
3) карбоновыми кислотами
4)
кислородом
Слайд 16
В отличие от пропанола-1, глицерин вступает в реакцию
с
1) уксусной кислотой
2) бромоводородом
3) кальцием
4) гидроксидом меди (II)
Слайд 17
Свежеприготовленный осадок Си(ОН)2
растворится, если к нему добавить:
пропандиол-1,2
2) Пропен
3) пропанол-1
4) пропанол-2
Слайд 18
С каждым из двух веществ: Cu(OH)2 и HCl
будет взаимодействовать
1) этиленгликоль
2) этанол
3) формальдегид
4) метанол
Слайд 19
Верны ли следующие суждения о свойствах спиртов?
А. Многоатомные
спирты вступают в реакции с гидроксидом меди (II).
Б. Среда
водного раствора глицерина нейтральная.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
Слайд 20
При взаимодействии фенола с натрием образуются:
1) фенолят натрия
и вода
2) фенолят натрия и водород
3) бензол и гидроксид
натрия
4) бензоат натрия и водород
Слайд 21
Атом кислорода в молекуле фенола
образует:
одну σ-связь
одну σ- и одну π-связи
две σ-связи
две π-связи
Слайд 22
Верны ли следующие суждения о феноле?
А. В отличие
от бензола фенол взаимодействует с бромной водой.
Б. Для фенола
характерны основные свойства.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны