- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Атмосфера. Химия стратосферы
Содержание
- 3. Механизм образования озона.Молекула кислорода может распадаться с
- 4. В реакцию синтеза озона способен вступать только
- 5. Распад молекулы озонаРаспад молекулы озона по реакции
- 6. Основная реакция разложения – это реакция с
- 7. Нулевой цикл озонаО2 + О(3P)+ М → О3 + М*,О3 + hν → О2 + О(3P)
- 8. Цепные процессы разрушения озона водородный цикл (реакции
- 9. Водородный циклПроисходит с участием гидроксидных радикалов ОН.Н2О
- 10. Азотный циклNО + О3 → N О2
- 11. Азотный цикл (продолжение)Опасность для озона представляют только
- 12. Озоновый слой «достает» только гемиоксид азота (N2О).
- 13. Хлорный цикл.Cl + О3 → ClO +
- 14. Взаимосвязь между количеством хлора и озона
- 15. Фреоны - фторхлоруглеводородыАтомарный хлор появляется в стратосфере
- 16. Фреоны- это нетоксичные, пожаровзрывобезопасные соединения, обладающие низкой реакционной способностью
- 17. Попадая в стратосферу, эти соединения могут взаимодействовать
- 18. Бромный цикл.Атом брома, подобно атому хлора, способен
- 19. Бромный цикл ( продолжение).Бром потенциально наиболее опасен
- 20. Основными источниками брома в стратосфере являются бромсодержащие соединения, используемые для тушения пожаров .
- 21. Галоны (хладоны). Эти вещества состоят из углерода
- 22. Обрыв цепи в реакциях распада озона В
- 23. Однако поскольку озон все-таки существует, значит есть
- 24. ОН + NO → HNО2.Протекание этой реакции
- 25. Окончательный обрыв цепи превращений азотного цикла наступает в результате вывода этих временных резервуаров (HNО2) в тропосферу.
- 26. Особое значение для обрыва цепи имеет реакция
- 27. Серебристые облака –устойчивые аэрозольные образования.Кристаллы льда + капли переохлажденной жидкости, содержащей ClONO2 (ClO)2 HNO3, HNO 2
- 28. Весенние процессы ClONO2 + H2O→HNO3+HOClClONO2 + HCl→
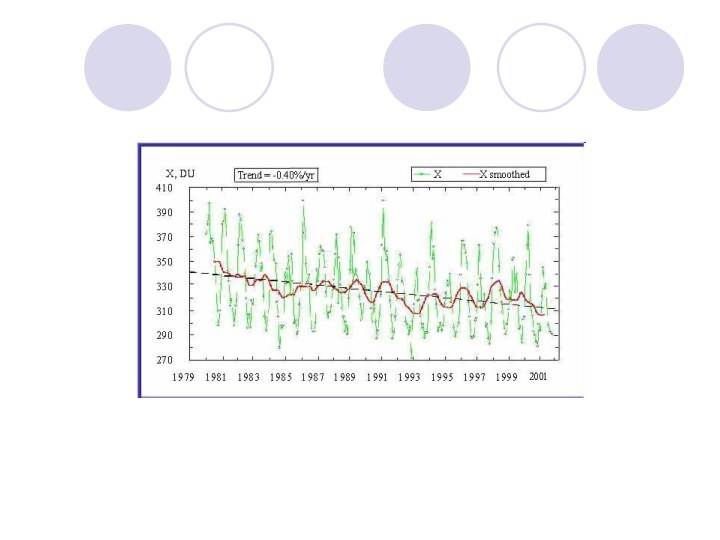
- 29. Химия озонаКоличество стратосферного озона над станцией Халли-Бей в Антарктиде.
- 30. Свойства озонаЖидкий озон – темно-синяя жидкость. Твердый озон – темно-фиолетовые призматические кристаллы.
- 31. Химические свойства озона характеризуются двумя основными чертами: нестойкостью (высокой реакционной способностью) сильным окислительным действием
- 32. При высоких концентрациях разлагается со взрывом. Озон
- 33. Распределение озона в атмосфере.Максимум концентрации озона располагается
- 34. В мезосфере озона мало, но он играет
- 35. Количества озона в атмосфереПрибор Добсона. Слой озона
- 36. Общее количества озона в атмосфере меняется от
- 37. Распределение озона В атмосфере принято выделять три
- 38. тропическая зона – минимальное содержание (265 е.Д.),
- 39. Причины образования озоновой дыры над Антарктидойувеличение поступления хлорфторуглеводородов в атмосферу (антропогенный фактор).
- 40. специфика движения воздушных масс в стратосфере высоких
- 41. прекращение обмена воздухом с другими областями стратосферы;сток озона в тропосферу;
- 42. снижение температуры воздуха внутри вихря до –70…–80
- 44. Скачать презентацию
- 45. Похожие презентации
Механизм образования озона.Молекула кислорода может распадаться с образованием триплетного О(3P) и синглетного О(1D) кислородаО2 + hν → О(1D) + О(3P) ν < 240 нм










































Слайд 3
Механизм образования озона.
Молекула кислорода может распадаться с образованием
триплетного О(3P) и синглетного О(1D) кислорода
О(1D) + О(3P) ν < 240 нм
Слайд 4
В реакцию синтеза озона способен вступать только триплетный
атом О(3P)
О2 + О(3P)+ М → О3 + М*,
где
М* – так называемое «третье тело».
Слайд 5
Распад молекулы озона
Распад молекулы озона по реакции с
участием «нечетного кислорода.
О3 + О → 2О2.
приводит к
стоку (выводу) озона из стратосферы. Однако скорость этой реакции невелика.
Слайд 6
Основная реакция разложения – это реакция с излучениями
с ν до 1130 нм:
О3 + hν →
О2 + О(1D) ; при 320нм макс. ск.О3 + hν → О2 + О(3P).
Слайд 8
Цепные процессы разрушения озона
водородный цикл (реакции с
участием ОН );
азотный цикл (с участием оксидов азота);
хлорный
и бромный циклы ( с участием соединений хлора и брома).
Слайд 9
Водородный цикл
Происходит с участием гидроксидных радикалов ОН.
Н2О +
hν → ОН + Н. длина волны менее 240 нм
Н2О + О(1D) → 2ОН;
СН4 + О(1D) → СН3 + ОН.
Водородный цикл
ОН + О3 → НО2 + О2
НО2 + О(3P) → ОН + О2
____________________________________________
О3 + О(3P) → 2О2
Слайд 10
Азотный цикл
NО + О3 → N О2 +
О2
N О2 + О(3P) → NО + О2
______________О3 + О(3P) → 2 О2
Существование азотного цикла нарушает нулевой цикл озона:
Слайд 11
Азотный цикл (продолжение)
Опасность для озона представляют только NО
и NО2 образующиеся непосредственно в стратосфере. Тропосферные оксиды азота
не «долетают» до озонового слоя.
Слайд 12
Озоновый слой «достает» только гемиоксид азота (N2О).
В
стратосфере из гемиоксида азота образуется NО, который инициирует азотный
путь (цикл) гибели озона:N2О + О(1D) → 2NО
Слайд 13
Хлорный цикл.
Cl + О3 → ClO + О2
ClO + О(3P) → Cl + О2 ______________________________
О3 +
О(3P) → 2 О2
Слайд 15
Фреоны - фторхлоруглеводороды
Атомарный хлор появляется в стратосфере при
фотохимическом разложении ряда хлорфторуглеводородов, которые благодаря малой химической активности
успевают достигнуть озонового слоя.
Слайд 16
Фреоны- это нетоксичные, пожаровзрывобезопасные соединения, обладающие низкой реакционной
способностью
Слайд 17
Попадая в стратосферу, эти соединения могут взаимодействовать с
излучением с длиной волны менее 240 нм с образованием
Сl :СFСl3 + hν → СFСl2 + Сl.
(СFСl3) - Ф-11
Слайд 18
Бромный цикл.
Атом брома, подобно атому хлора, способен при
взаимодействии с озоном образовывать оксид брома и молекулу кислорода.
:Br + О3 → BrO + О2;
BrO + BrO → 2Br + О2
ClO + BrO → Cl + Br + О2.
Слайд 19
Бромный цикл ( продолжение).
Бром потенциально наиболее опасен для
озонового слоя.
Однако влияние его меньше, чем влияние других
циклов, поскольку концентрация брома в стратосфере очень низкая.
Слайд 20
Основными источниками брома в стратосфере являются бромсодержащие соединения,
используемые для тушения пожаров .
Слайд 21
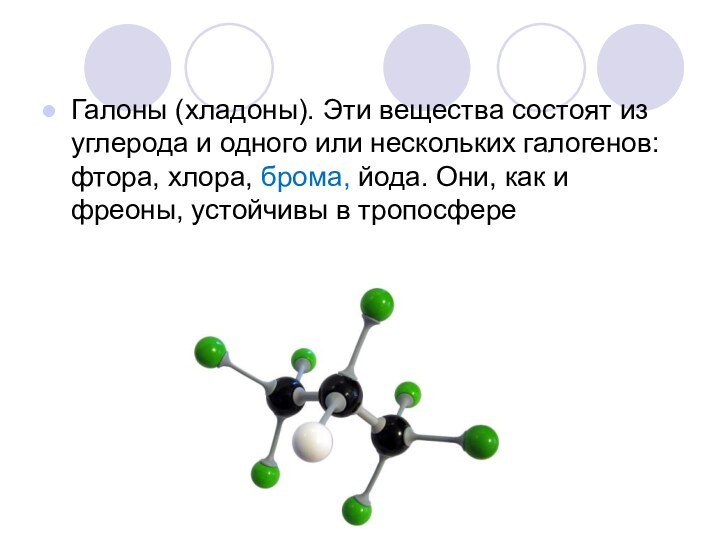
Галоны (хладоны). Эти вещества состоят из углерода и
одного или нескольких галогенов: фтора, хлора, брома, йода. Они,
как и фреоны, устойчивы в тропосфере
Слайд 22
Обрыв цепи в реакциях распада озона
В рассмотренных выше
циклах «активные» частицы практически не расходуются. Каждая из «активных»
частиц может многократно (до 10 млн раз) инициировать цикл разрушения озона.
Слайд 23
Однако поскольку озон все-таки существует, значит есть реакции,
которые обрывают эти циклы.
Наиболее важные реакции:
СН4 + ОН →
СН3 + Н2О;ОН + НО2 → Н2О + О2.
Слайд 24
ОН + NO → HNО2.
Протекание этой реакции приводит
к образованию временного резервуара для «активных» частиц водородного и
азотного циклов, поскольку азотистая кислота разлагается с образованием исходных «активных» частиц.
Слайд 25
Окончательный обрыв цепи превращений азотного цикла наступает в
результате вывода этих временных резервуаров (HNО2) в тропосферу.
Слайд 26
Особое значение для обрыва цепи имеет реакция взаимодействия
оксида хлора и диоксида азота.
ClO + NО2 → ClONO2.
ClONO2-хлористый
нитрозил
Слайд 27
Серебристые облака –устойчивые аэрозольные образования.
Кристаллы льда + капли
переохлажденной жидкости, содержащей ClONO2 (ClO)2 HNO3,
HNO 2
Слайд 28
Весенние процессы
ClONO2 + H2O→HNO3+HOCl
ClONO2 + HCl→ Cl2
+ HNO3
Cl2 + hν → 2Cl
HOCl + hν →
Cl+ OH
Слайд 30
Свойства озона
Жидкий озон – темно-синяя жидкость.
Твердый озон
– темно-фиолетовые призматические кристаллы.
Слайд 31
Химические свойства озона характеризуются двумя основными чертами:
нестойкостью
(высокой реакционной способностью)
сильным окислительным действием
Слайд 32
При высоких концентрациях разлагается со взрывом. Озон очень
токсичен. ПДК 1 мг/м3.
До земной поверхности доходит только
УФ с длинами волн больше 290 нм. Озон выполняет защитную функцию для биосферы.
Слайд 33
Распределение озона в атмосфере.
Максимум концентрации озона располагается на
высотах от 15 до 35 км, т. е. в
стратосфере.В тропосфере – от 0 до 0,1 мг/м3.
Слайд 34
В мезосфере озона мало, но он играет важную
роль в поддержании теплового баланса планеты и формировании нижнего
слоя ионосферы.
Слайд 35
Количества озона в атмосфере
Прибор Добсона. Слой озона высотой
10–5 м (0,01 мм) принимается равным одной единице Добсона
(е. Д.).
Слайд 36
Общее количества озона в атмосфере меняется от 120
до 760 е.Д. при среднем для всего земного шара
значении 290 е. Д.
Слайд 37
Распределение озона
В атмосфере принято выделять три зоны:
полярная зона – характеризуется максимальным содержанием (около 400
е. Д.) и наибольшими сезонными колебаниями (около 50 %); зона максимальной концентрации озона расположена наиболее близко к поверхности – на высотах 13–15 км;.
Слайд 38
тропическая зона – минимальное содержание (265 е.Д.), сезонные
колебания не превышают 10–15 %; зона максимальной концентрации озона
находится на высотах 24–27 км;средние широты – занимают промежуточное положение