электропроводности растворов – ионы
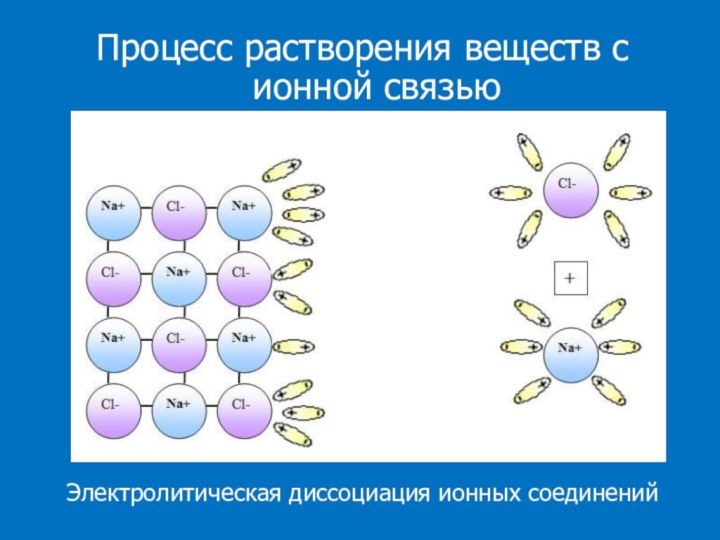
Процесс распада электролита на ионы-электролитическая диссоциация
И.А.Каблуков
В процессе диссоциации участвуют молекулы воды. Их взаимодействие с ионами называется гидратацией
В растворе находятся гидратированные ионы