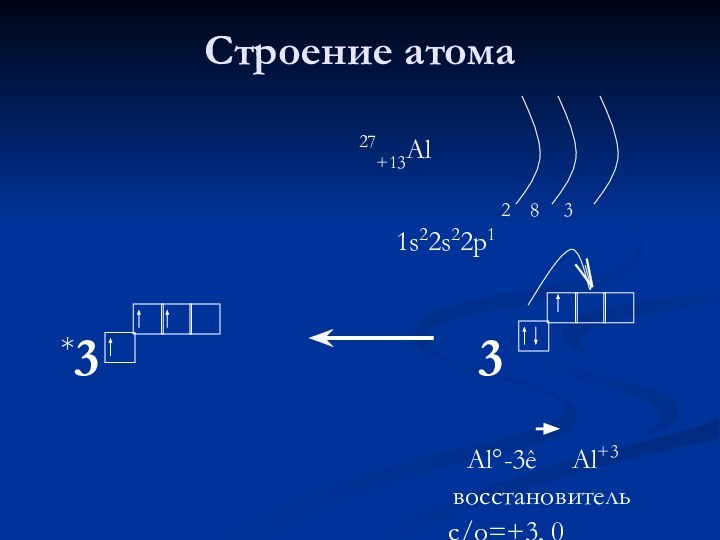
27+13Al
2 8 31s22s22p1
*3 3
Al°-3ê Al+3
восстановитель
с/о=+3, 0
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть











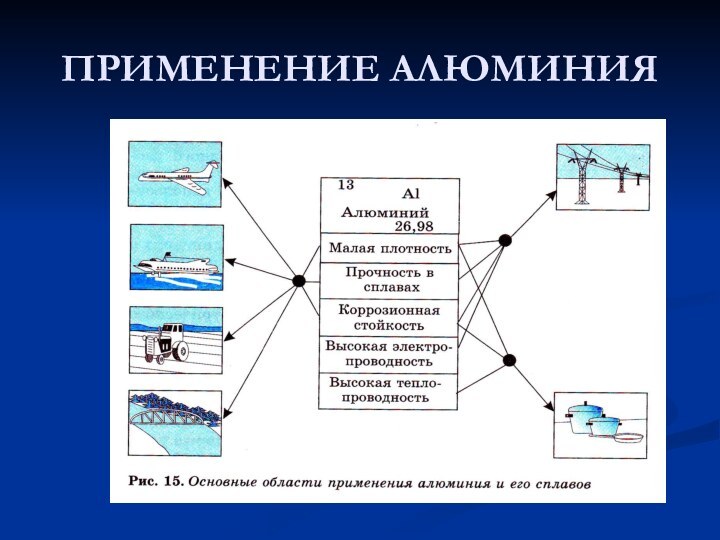

![АЛЮМИНИЙ Ссылки на источники используемого материала: http://s019.radikal.ru/i606/1204/27/74062dfcc275.jpg [URL=http://www.radikal.ru][IMG]http://s019.radikal.ru/i606/1204/27/74062dfcc275.jpg[/IMG][/URL] [URL=http://radikal.ru/F/s019.radikal.ru/i606/1204/27/74062dfcc275.jpg.html][IMG]http://s019.radikal.ru/i606/1204/27/74062dfcc275t.jpg[/IMG][/URL]](/img/tmb/12/1191557/e7a9c6038487d705f9b252bdadfeb0b2-720x.jpg)