кислород как атом и молекула;
изучить физические и химические свойства
кислорода, нахождение его в природе; рассмотреть способы получения кислорода в лаборатории и промышленности;
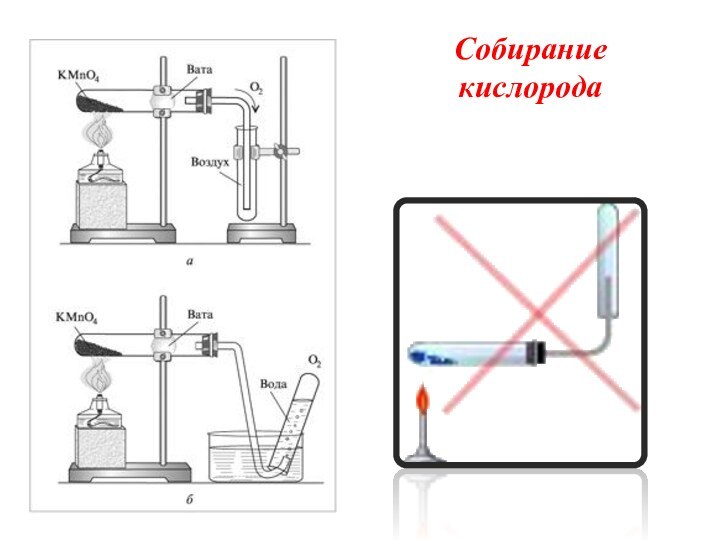
способах собирания кислорода;
способствовать закреплению умения составлять уравнения реакций.