- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Мембранное материаловедение. Топливные элементы
Содержание
- 2. 8ТОПЛИВНЫЕ ЭЛЕМЕНТЫ
- 3. СХЕМА ТОПЛИВНОГО ЭЛЕМЕНТА
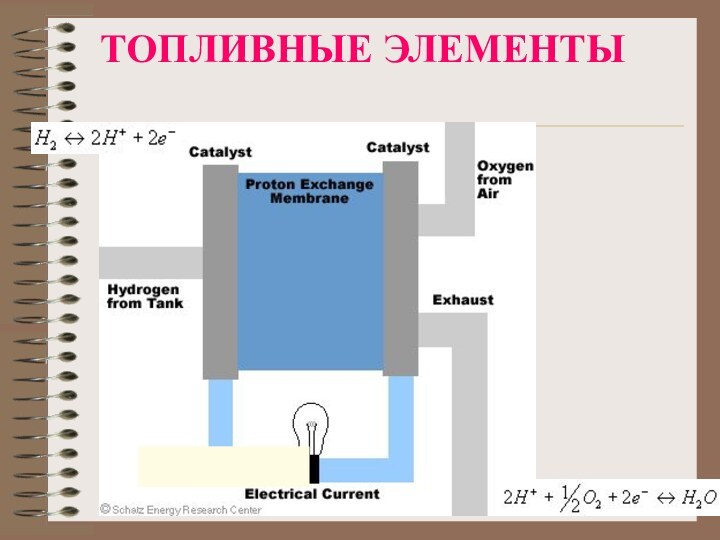
- 4. ТОПЛИВНЫЕ ЭЛЕМЕНТЫ
- 5. Топливные элементы – междисциплинарная проблема ЭлектрохимияМембранный транспортКатализМатериаловедениеИнжениринг и проблемы энергетики
- 6. КПД различных машин
- 7. Причины высоких КПД в ТЭ
- 8. Различные типы топливных элементов
- 9. Щелочные топливные элементы
- 10. Водородные ТЭ с Н+ проводящей мембраной
- 11. Метанольные ТЭ с Н+ проводящей мембраной
- 12. ТЭ на фосфорной кислоте
- 13. ТЭ на расплавах карбонатов
- 14. ТЭ на твердых оксидах
- 15. Требования к мембранамНизкая стоимость (120-150oC, >10000 час Механическая стабильностьЭлектроизолирующие свойства
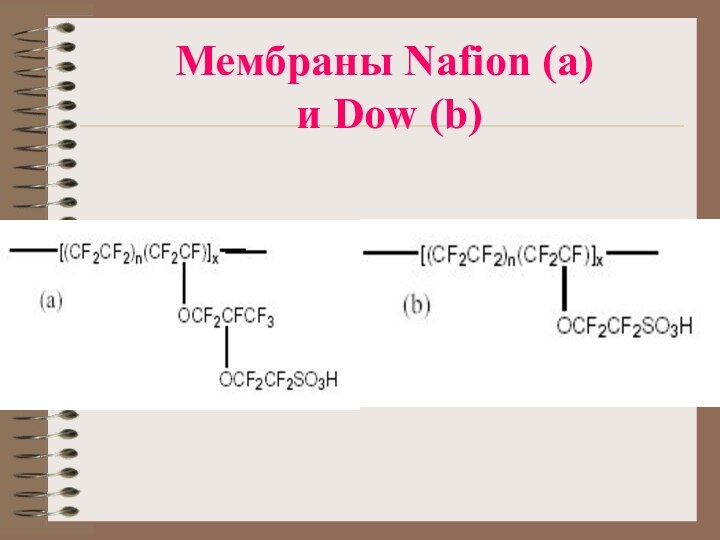
- 16. Мембраны Nafion (a) и Dow (b)
- 17. Мембрана сулфонилимида (более проводящая чем Nafion)
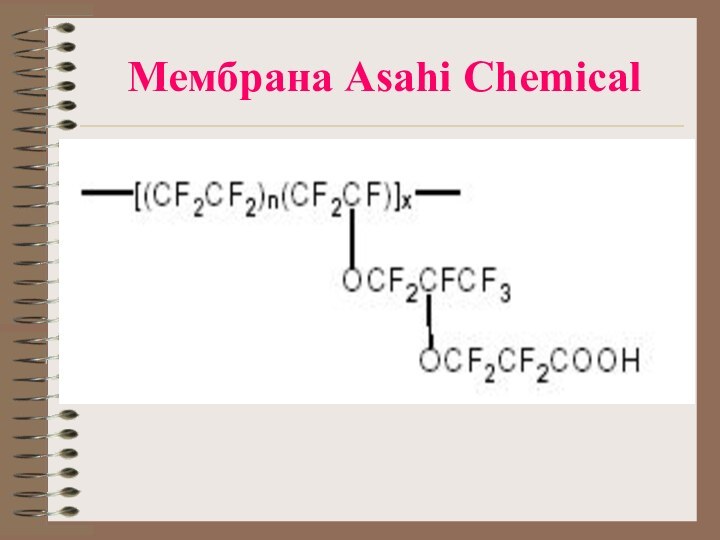
- 18. Мембрана Asahi Chemical
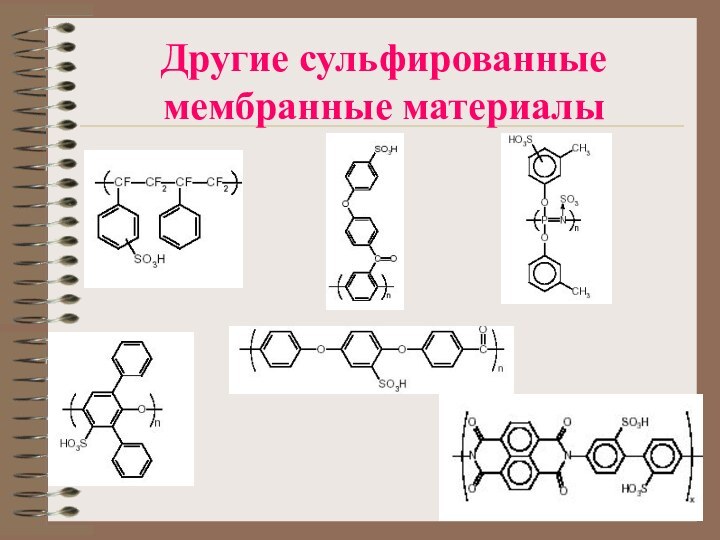
- 19. Другие сульфированные мембранные материалы
- 20. Материалы с остатками фосфорной кислоты
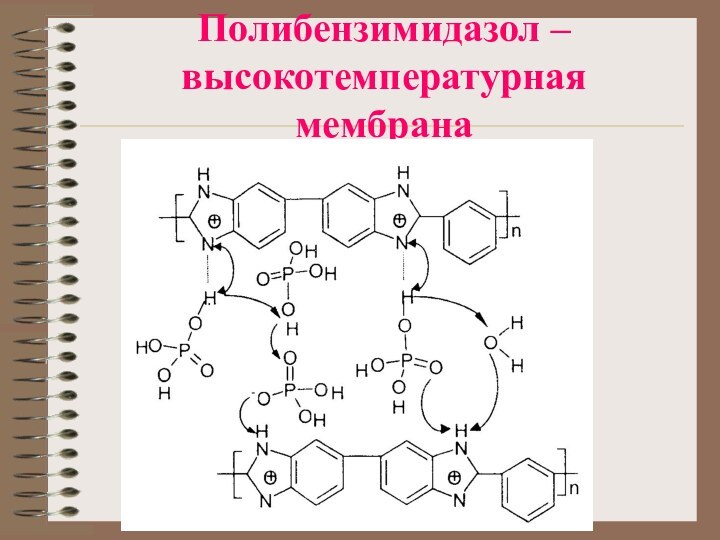
- 21. Полибензимидазол – высокотемпературная мембрана
- 22. Полимерная цепь Nafion
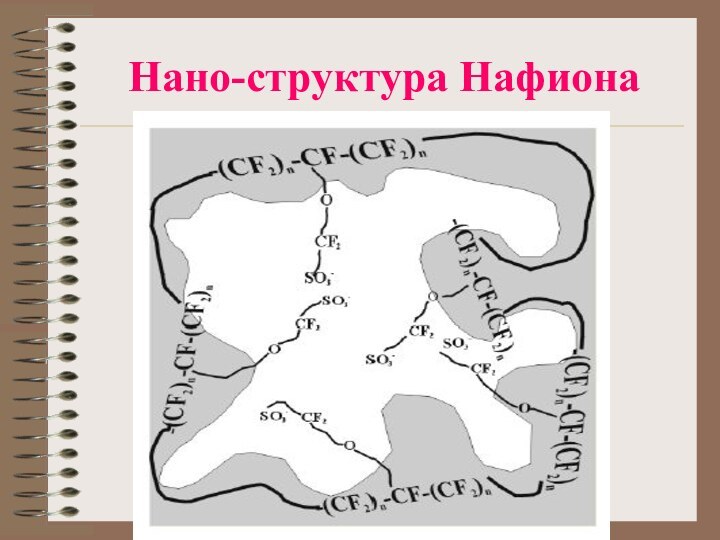
- 23. Нано-структура Нафиона
- 24. Влияние влажности на проводимость Нафиона
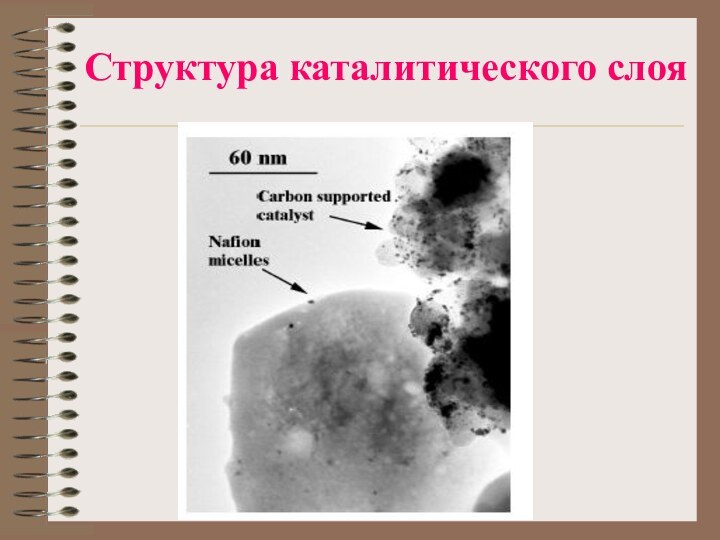
- 25. Структура каталитического слоя
- 26. Структура каталитического слоя
- 27. Водные проблемы (water management)Состояние воды в мембране: сольватация –SO3H групп сольватация Н+ «объемная» водыДегидратация: “асимметрия” образования воды; температурный режим (
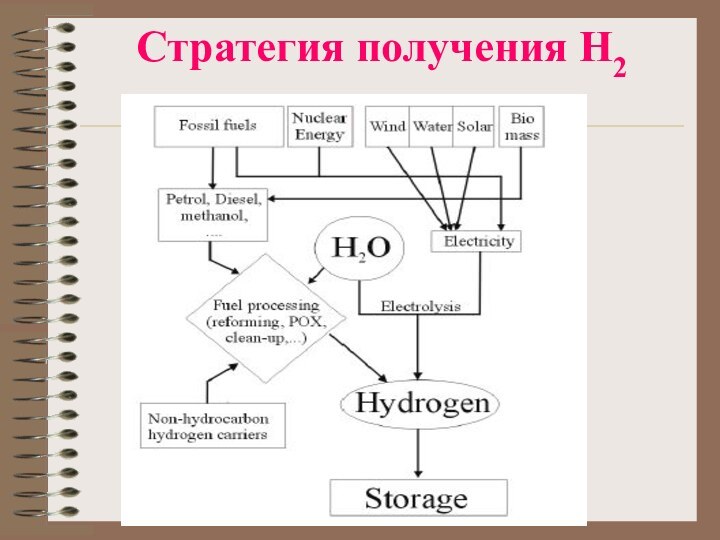
- 28. Стратегия получения Н2
- 29. Методы получения водорода (ископаемые топлива)Паровая конверсия природного
- 30. Альтернативные методы получения водородаЭлектролизФотолиз водыВысокотемпературные ядерные (Не) реактора
- 31. Термохимический цикл в Не ядерном реактореИсточник энергии
- 32. Фотохимическая генерация Н2
- 33. Методы очистки водородаМембраны: Pd полимерные мембраныХимические:дожигание: СО + 1/2O2
- 34. Хранение водородаГазовые баллоны (0,5 кг Н2)Жидкий водород
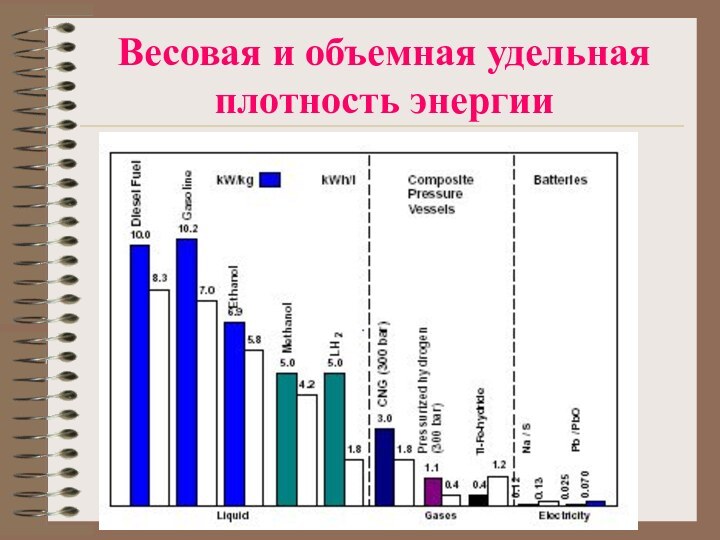
- 35. Весовая и объемная удельная плотность энергии
- 36. Скачать презентацию
- 37. Похожие презентации
8ТОПЛИВНЫЕ ЭЛЕМЕНТЫ



























Слайд 5
Топливные элементы – междисциплинарная проблема
Электрохимия
Мембранный транспорт
Катализ
Материаловедение
Инжениринг и
проблемы энергетики
Слайд 15
Требования к мембранам
Низкая стоимость (
барьерные свойства (Н2,О2, МеОН)
Термическая и химическая стабильность: >120-150oC, >10000
час Механическая стабильность
Электроизолирующие свойства
Слайд 27
Водные проблемы
(water management)
Состояние воды в мембране:
сольватация –SO3H групп
сольватация
Н+
«объемная» воды
Дегидратация:
“асимметрия” образования воды;
температурный режим (
стабильностьУвлажнение:
роль кроссовера;
“заливание” пор в электроде.
Слайд 29
Методы получения водорода
(ископаемые топлива)
Паровая конверсия природного газа:
CH4 +
H2O ? CO + 3H2
CO + H2O = CO2
+ H2Каталитический риформинг
C6H14 ? C6H6 + 4H2
Пиролиз
CnHm ? C2H4 + H2
Слайд 30
Альтернативные методы получения водорода
Электролиз
Фотолиз воды
Высокотемпературные ядерные (Не) реактора
Слайд 31
Термохимический цикл в Не ядерном реакторе
Источник энергии –
Не (~1000оС)
2H2О + SO2 + J2 ? H2SO4 +
2HJ (при 900о)2HJ ? J2 + H2 (при 450оС)
H2SO4 + SO2 + H2O + 1/2O2 (при 850oC)
Слайд 33
Методы очистки водорода
Мембраны:
Pd
полимерные мембраны
Химические:
дожигание: СО + 1/2O2 ?
CO2
реакция водяного пара: CO + H2O = CO2 +
H2метанирование: СO + 3H2 ? CH4 + H2O
Адсорбционные