огромная пасть все еще светилась голубоватым пламенем, глубоко сидящие
дикие глаза обведены огненными кругами. Я дотронулся до этой светящейся головы и, подняв руку, увидел, что мои пальцы тоже засветились в темноте.- Фосфор, – сказал я».
ФОСФОР
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть






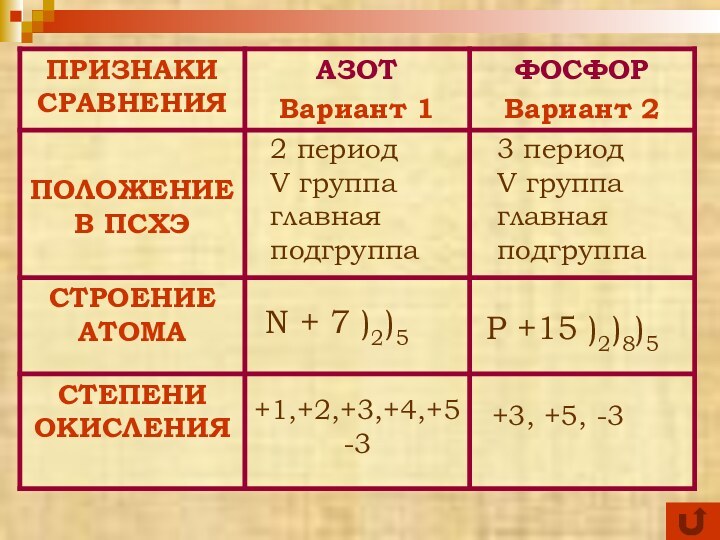
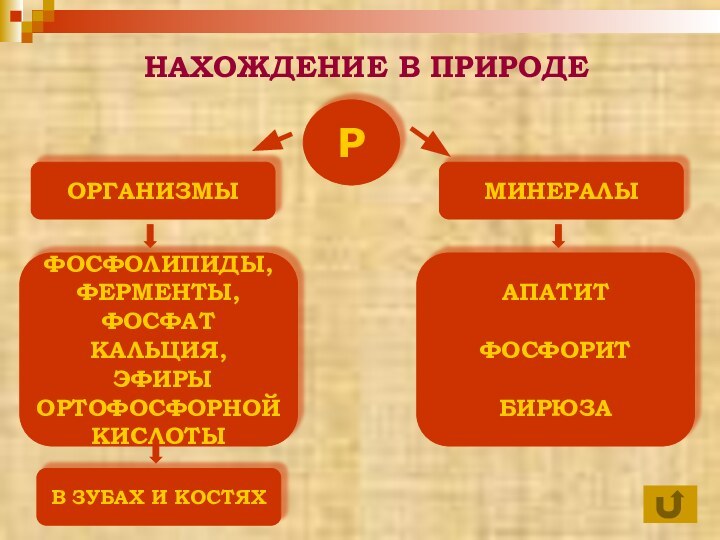











ФОСФОР
ПЛАН УРОКА:
4P0 + 5O02 = 2P+52O-25
3Ca0 + 2P0 = Ca+23P-32
ХИМИЧЕСКИЕ СВОЙСТВА
2P0 + 3O0 = 2P+32S-23
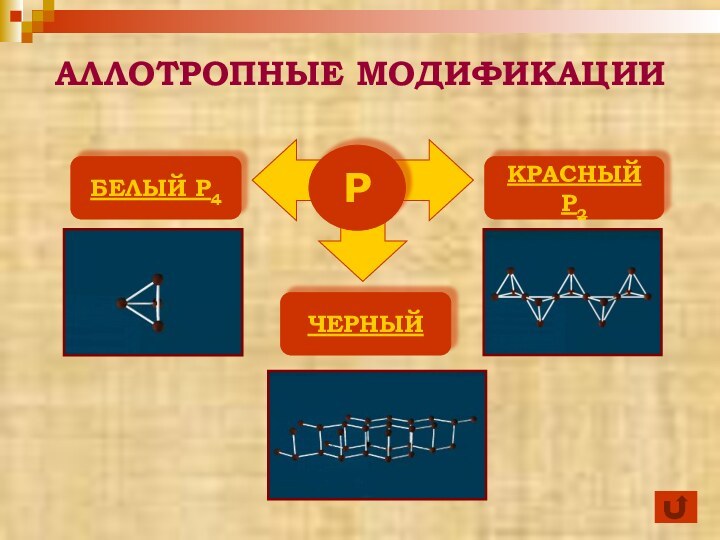
БЕЛЫЙ ФОСФОР
КРАСНЫЙ ФОСФОР
ЧЕРНЫЙ ФОСФОР
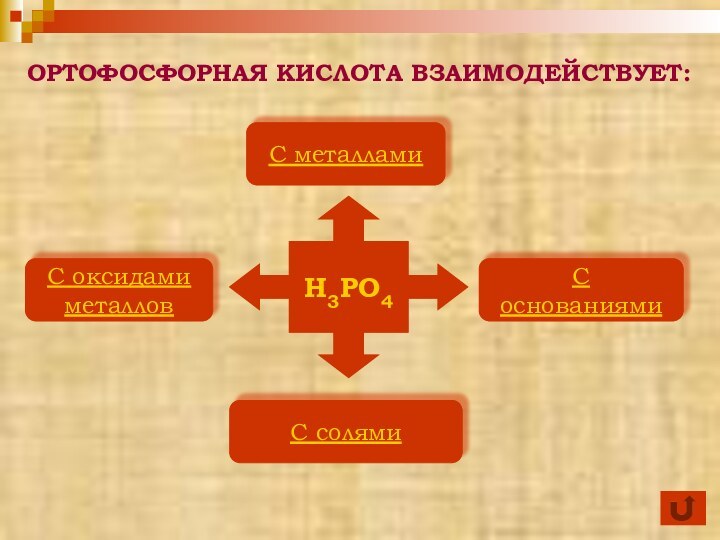
H3PO4+ NaOH=NaH2PO4+ H2O
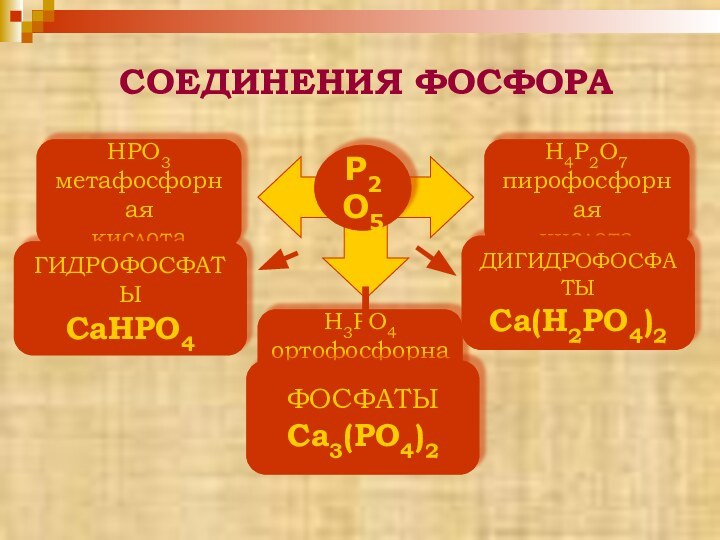
H3PO4
С основаниями
H3PO4+2NaOH=Na2HPO4+2H2O
2H3PO4+3Na2СO3=2Na3PO4+3СО2+3H2O
H3PO4
С солями
H3PO4+3AgNO3=Ag3PO4↓+3HNO3