дефицита пресной воды.
Противоречие
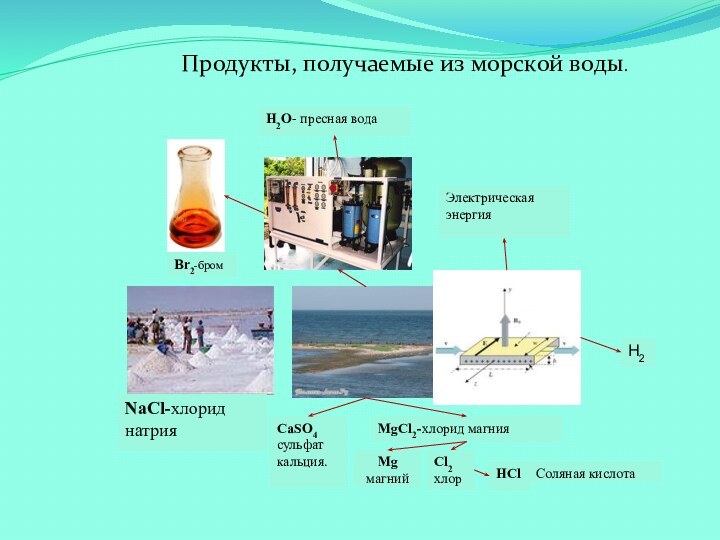
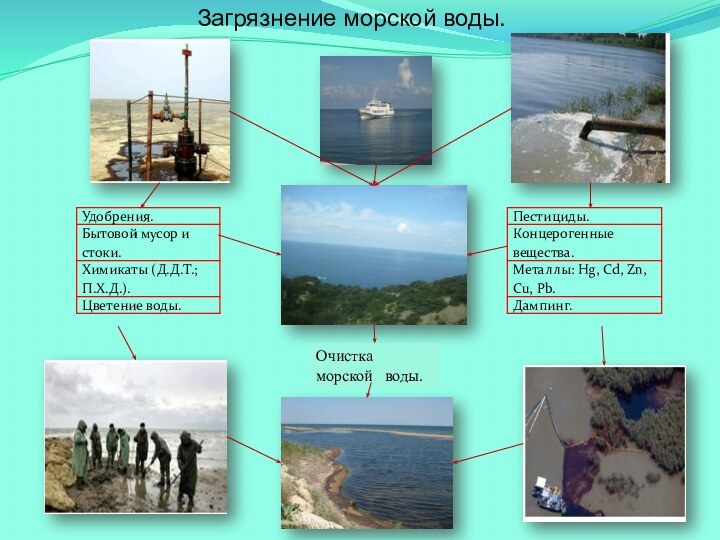
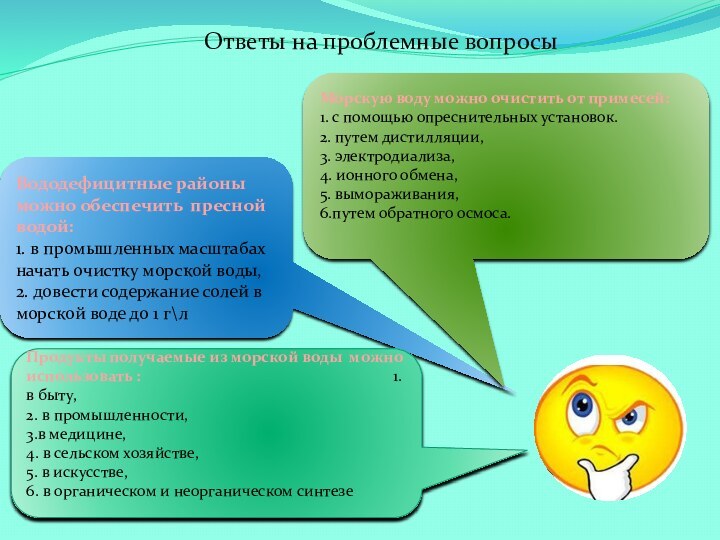
1. Какими способами можно очистить морскую
воду от примесей?2. Куда использовать продукты очистки?
3.Как решить обеспечение пресной водой вододефицитные районы?
?
Проблемные вопросы: