Слайд 2
ТОКСИЧНОСТЬ АММИАКА
Аммиак - NH3 является клеточным ядом. При
высоких концентрациях он повреждает главным образом нервные клетки (гепатаргическая
кома).
В норме распад 70 г АК в сутки ведет к концентрации NH3 в крови 60 мкмоль/л, что в 100 раз меньше концентрации глюкозы в крови.
Аммиак настолько токсичен, что должен быть немедленно удален посредством того или иного экскреторного механизма, либо путем включения в какое-то другое азотсодержащее соединение, не обладающее подобной токсичностью.
Слайд 3
Обезвреживание аммиака
В организмах автотрофов большая часть образующегося аммиака
может вновь использоваться для синтеза новых клеточных структур. Гетеротрофы
же обычно получают с пищей значительное количество белка, усвоение которого легко может привести к накоплению большого количества конечных продуктов азотистого обмена. Удаление этих отходов требует создания соответствующего аппарата.
Слайд 4
Обезвреживание аммиака
Организм, живущий в водной среде, может выделять
аммиак непосредственно, поскольку он будет немедленно разбавлен водой, не
оказывая никакого или почти никакого вредного влияния на клетки. Экскреция аммиака у животных, обитающих в засушливых областях, потребовала бы для его разведения использования собственных водных ресурсов.
Поэтому у многих видов аммиак превращается в организме в некоторые другие соединения, обладающие меньшей токсичностью.
Слайд 5
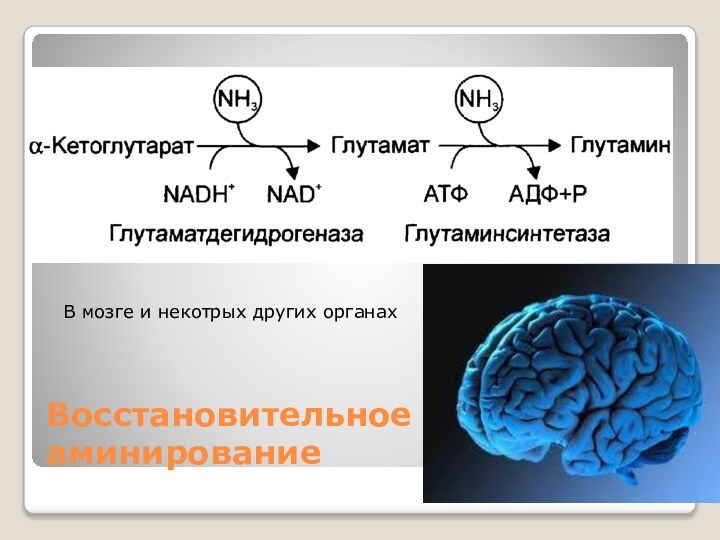
Восстановительное аминирование
Большинство организмов обладает способностью реутилизировать аммиак за
счет реакции, катализируемой глутаматдегидрогеназой.
А-Кетоглутарат + NH3 + НАДФН.Н+
Глутамат
+ НАДФ+.
Это восстановительное аминирование.
Однако все же некоторая часть образовавшегося аммиака остается неиспользованной и в конце концов выводится из организма беспозвоночных и позвоночных либо в свободном виде, либо в форме мочевой кислоты, либо в форме мочевины.
Слайд 6
Восстановительное аминирование
В мозге и некотрых других органах
Слайд 8
Глутаминаза
В клетках кишечника под действием фермента глутаминазы происходит
гидролитическое освобождение амидного азота в виде аммиака:
Слайд 9
Высокий уровень глутамина в крови и лёгкость его
поступления в клетки обусловливают использование глутамина во многих анаболических
процессах. Глутамин - основной донор азота в организме. Амидный азот глутамина используется для синтеза пуриновых и пиримидиновых нуклеотидов, аспарагина, аминосахаров и других соединений
Слайд 10
Глутамин
Белки
Пурины
Пиримидины
Аспарагин
Аминосахара
Глюкоза
Слайд 11
Синтез аспарагина
Существуют 2 изоформы этого фермента - глутаминзависимая
и аммиакзависимая, которые используют разные доноры амидных групп. Первая
функционирует в животных клетках, вторая преобладает в бактериальных клетках, но присутствует и у животных. Однако такой путь обезвреживания аммиака в клетках человека используется редко и к тому же требует больших энергетических, чем синтез глутамина.
Слайд 12
МОЧЕВИНА
У человека инактивация аммиака осуществляется прежде всего за
счет синтеза мочевины, часть NH3 выводится непосредственно почками.
Слайд 13
АММОНИОТЕЛИЧЕСКИЕ ОРГАНИЗМЫ
У разных видов позвоночных инактивация и выведение
аммиака производятся различными способами. Живущие в воде животные выделяют
аммиак непосредственно а воду; например, у рыб он выводится через жабры (аммониотелические организмы).
Слайд 14
УРЕОТЕЛИЧЕСКИЕ ОРГАНИЗМЫ
Наземные позвоночные, в том числе человек, выделяют
лишь небольшое количество аммиака, а основная его часть превращается
в мочевину (уреотелические организмы).
Слайд 15
УРИКОТЕЛИЧЕСКИЕ ОРГАНИЗМЫ
Птицы и рептилии, напротив, образуют мочевую кислоту,
которая в связи с экономией воды выделяется преимущественно в
твердом виде (урикотелические организмы).
Слайд 16
Синтез мочевины
Мочевина в противоположность аммиаку это нейтральное и
нетоксичное соединение. Небольшая молекула мочевины может проходить через мембраны,
а также из-за ее хорошей растворимости в воде мочевина легко переносится кровью и выводится с мочой.
Слайд 17
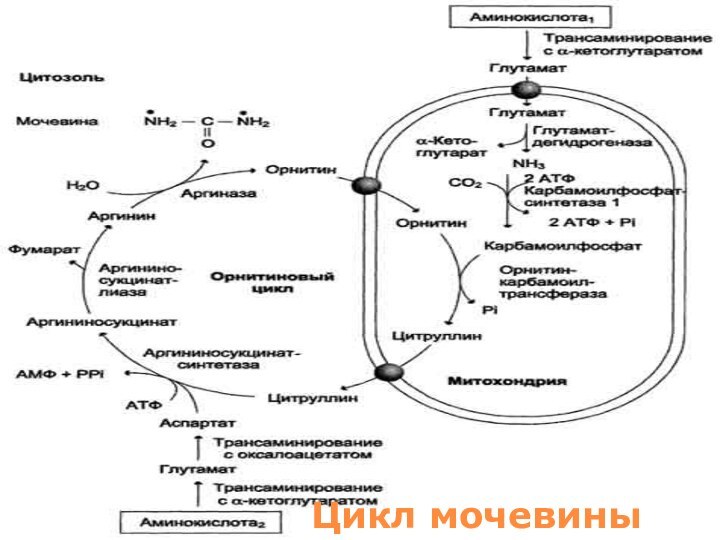
СТАДИИ СИНТЕЗА МОЧЕВИНЫ
Мочевина образуется в результате циклической последовательности
реакций, протекающих в печени.
Оба атома азота берутся из
свободного аммиака и за счет дезаминирования аспартата, карбонильная группа — из гидрокарбоната.
Слайд 19
Первая реакция
На первой стадии, реакция [1], из гидрокарбоната
(НСО3-) и аммиака с потреблением 2 молекул АТФ образуется
карбамоилфосфат.
Слайд 20
Вторая стадия
На следующей стадии, реакция [2], карбамоильный
остаток переносится на орнитин с образованием цитруллина. Для этой
реакции вновь необходима энергия в форме АТФ, который при этом расщепляется на АМФ и дифосфат.
Слайд 21
Третья стадия
Вторая аминогруппа молекулы мочевины поставляется за счет
реакции аспартата с цитруллином [3].
Слайд 22
Четвертая стадия
Для обеспечения необратимости реакции дифосфат гидролизуется полностью.
Отщепление фумарата от аргининосукцината приводит к аргинину [4],
















![Обезвреживание аммиака (связывание) Первая реакцияНа первой стадии, реакция [1], из гидрокарбоната (НСО3-) и аммиака с](/img/tmb/13/1232918/69a976a285128a499fef31a372887fbe-720x.jpg)
![Обезвреживание аммиака (связывание) Вторая стадияНа следующей стадии, реакция [2], карбамоильный остаток переносится на орнитин](/img/tmb/13/1232918/368ba96ac5ce409674a6637443223f76-720x.jpg)
![Обезвреживание аммиака (связывание) Третья стадияВторая аминогруппа молекулы мочевины поставляется за счет реакции аспартата с цитруллином [3].](/img/tmb/13/1232918/2fad2348c9eab81939d091c4d1c7fb7b-720x.jpg)

![Обезвреживание аммиака (связывание) Пятая стадия из которого в результате гидролиза образуется мочевина [5]. Остающийся орнитин](/img/tmb/13/1232918/1ca4d0bce1b946b93cdc40c7bc679123-720x.jpg)