- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Оксиды, их классификация и свойства
Содержание
- 2. Что такое оксиды?Оксиды – это сложные вещества,
- 3. Классификация оксидовПо агрегатному состоянию ТВЕРДЫЕ Fe2O3, SiO2ЖИДКИЕ Н2О, SO3ГАЗООБРАЗНЫЕ SO2, CO2
- 4. Пример твердого оксидаПесок – диоксид кремния SiO2 с небольшим количеством примесей.
- 5. Пример жидкого оксидаВода – оксид водорода Н2O.
- 6. Классификация оксидовПо химическим свойствам Солеобразующие Несолеобразующие
- 7. Классификация оксидов Несолеобразующие оксиды –
- 8. Классификация оксидов Солеобразующие оксиды –
- 9. Основные оксиды Основные оксиды –
- 10. Кислотные оксиды Кислотные оксиды –
- 11. Типичные реакции основных оксидов1) Основной оксид +
- 12. Типичные реакции основных оксидов1) Основной оксид +
- 13. Типичные реакции основных оксидов2) Основной оксид +
- 14. Типичные реакции основных оксидов3) Основной оксид +
- 15. Типичные реакции кислотных оксидов1) Кислотный оксид +
- 16. Типичные реакции кислотных оксидов1) Кислотный оксид +
- 17. Типичные реакции кислотных оксидов1) Кислотный оксид +
- 18. Типичные реакции кислотных оксидов1) Кислотный оксид +
- 19. Обобщение темы:Вопрос-ответ:Что такое оксиды?Какие оксиды называются основными?В каком случае кислотный оксид взаимодействует с водой?
- 20. Обобщение темы:Тест: «Правильный ответ»1) Какой из оксидов
- 21. Правильно.
- 22. Неправильно.
- 23. Ответы на вопросы:1) Оксиды – это сложные
- 24. Домашнее задание:§ 40 Упр. 1, 2, 3.
- 25. Скачать презентацию
- 26. Похожие презентации
Что такое оксиды?Оксиды – это сложные вещества, состоящие из двух химических элементов, один из которых кислород в степени окисления -2.





















Слайд 3
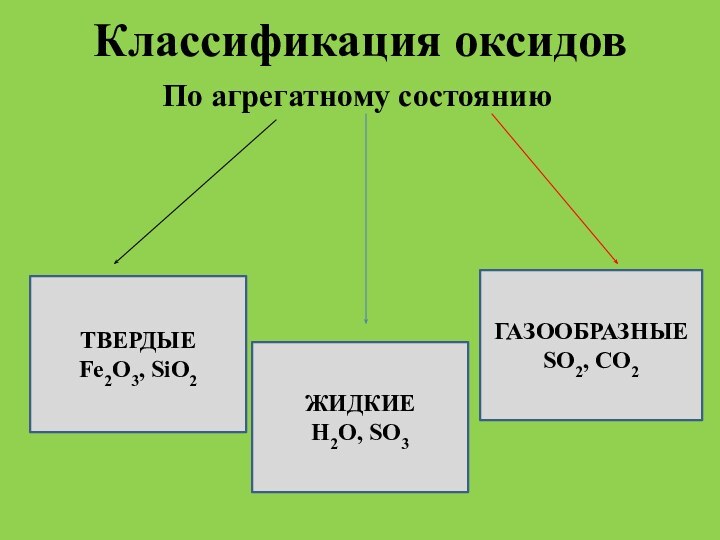
Классификация оксидов
По агрегатному состоянию
ТВЕРДЫЕ
Fe2O3,
SiO2
ЖИДКИЕ
Н2О, SO3
ГАЗООБРАЗНЫЕ
SO2, CO2
Слайд 7
Классификация оксидов
Несолеобразующие оксиды – такие
оксиды, которые не взаимодействуют ни с кислотами, ни с
щелочами и не образуют солей.Например:
oксиды азота (I), (II) и (IV) - N2O, NO, NO2
oксид углерода (II) – СО
oксид кремния (II) - SiO
Слайд 8
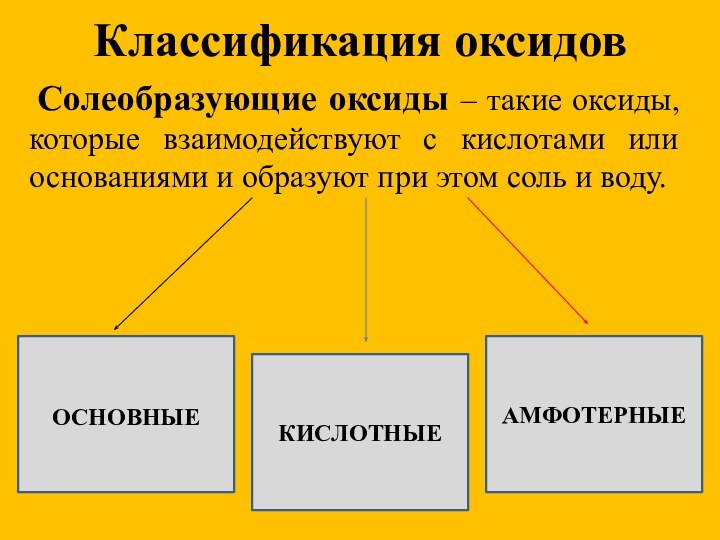
Классификация оксидов
Солеобразующие оксиды – такие
оксиды, которые взаимодействуют с кислотами или основаниями и образуют
при этом соль и воду.
ОСНОВНЫЕ
КИСЛОТНЫЕ
АМФОТЕРНЫЕ
Слайд 9
Основные оксиды
Основные оксиды – это
такие оксиды, которым соответствуют основания.
Например:
MgO соответствует Mg(OH)2
Na2O соответствует
NaOHBaO соответствует Ba(OH)2
Слайд 10
Кислотные оксиды
Кислотные оксиды – это
такие оксиды, которым соответствуют кислоты.
Например:
SO3 соответствует H2SO4
CO2 соответствует
H2CO3P2O5 соответствует H3PO4
Слайд 11
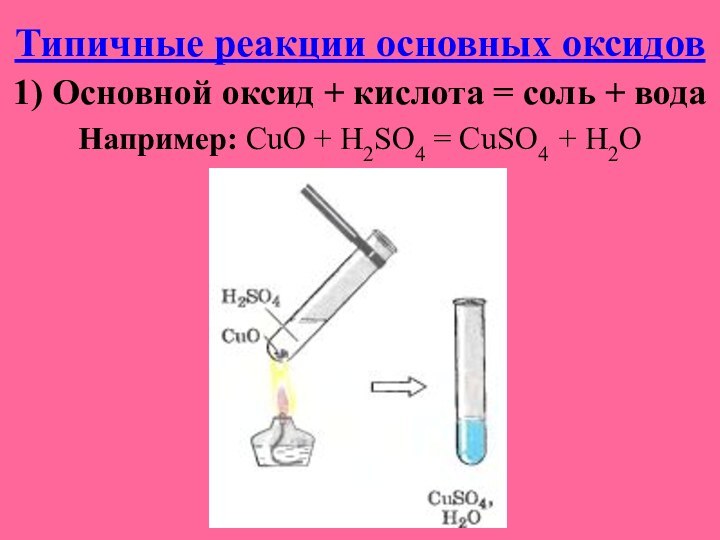
Типичные реакции основных оксидов
1) Основной оксид + кислота
= соль + вода
2) Основной оксид + кислотный оксид
= соль3) Основной оксид + вода = щелочь
Слайд 12
Типичные реакции основных оксидов
1) Основной оксид + кислота
= соль + вода
Например: CuO + H2SO4 = CuSO4
+ H2O
Слайд 13
Типичные реакции основных оксидов
2) Основной оксид + кислотный
оксид = соль
Например:
СaO + N2O5 = Ca(NO3)
MgO + SiO2 = MgSiO3
Слайд 14
Типичные реакции основных оксидов
3) Основной оксид + вода
= щелочь
Например: K2O + H2O = 2KOH
Эта реакция
протекает только в том случае, если образуется растворимое основание – щелочь.
Слайд 15
Типичные реакции кислотных оксидов
1) Кислотный оксид + основание
= соль + вода
2) Кислотный оксид + основной оксид
= соль3) Кислотный оксид + вода = кислота
Слайд 16
Типичные реакции кислотных оксидов
1) Кислотный оксид + основание
= соль + вода
Например:SO2 + 2KOH = K2SO3 +
H2O
Слайд 17
Типичные реакции кислотных оксидов
1) Кислотный оксид + основной
оксид = соль
Например:
SO3 + K2O = K2SO4
CO2 + CaO = CaCO3
Слайд 18
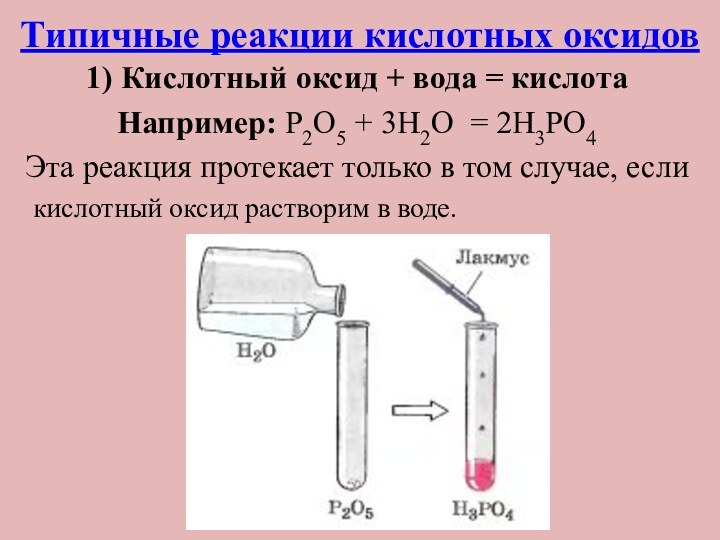
Типичные реакции кислотных оксидов
1) Кислотный оксид + вода
= кислота
Например: P2O5 + 3H2O = 2H3PO4
Эта реакция протекает
только в том случае, если кислотный оксид растворим в воде.
Слайд 19
Обобщение темы:
Вопрос-ответ:
Что такое оксиды?
Какие оксиды называются основными?
В каком
случае кислотный оксид взаимодействует с водой?
Слайд 20
Обобщение темы:
Тест: «Правильный ответ»
1) Какой из оксидов несолеобразующий:
а) P2O5 б) NO
в)
SO3 г) CaO 2) Какой из предложенных оксидов кислотный:
а) K2O б) MgO
в) CO2 г) Na2O
3) Какой класс соединений образуется при взаимодействии кислотного оксида с водой:
а) кислота б) основание
в) соль г) соль и основание
Слайд 23
Ответы на вопросы:
1) Оксиды – это сложные вещества,
состоящие из двух химических элементов, один из которых кислород
в степени окисления -2.2) Основные оксиды – это такие оксиды, которым соответствуют основания.
3) Кислотный оксид взаимодействует с водой только в том случае, если кислотный оксид растворим в воде.





























