Слайд 2
УГЛЕВОДЫ
Углеводы входят в состав клеток и тканей всех растительных
и животных организмов и по массе составляют основную часть
органического вещества на Земле. На долю углеводов приходится около 80% сухого вещества растений и около 20% животных. Растения синтезируют углеводы из неорганических соединений - углекислого газа и воды (СО2 и Н2О) в процессе фотосинтеза:
6СО2 + 6Н2О свет, хлорофилл→ C6H12O6 + 6O2
Слайд 3
Углеводы имеют общую формулу Cn(H2O)m, откуда и возникло
название этих природных соединений. Углеводы делятся на: моносахариды (важнейшие
представители – глюкоза и фруктоза); дисахариды (сахароза); полисахариды (важнейшие представители – крахмал и целлюлоза).
Слайд 4
Моносахариды - твердые вещества, способные кристаллизоваться. Они гидроскопичны,
очень легко растворимы в воде, легко образуют сиропы, из
которых выделить их в кристаллическом виде бывает очень трудно.
Самые распространённые моносахариды – глюкоза и фруктоза, имеющие формулу (CH2O)6. Все моносахариды имеют сладкий вкус, кристаллизуются и легко растворяются в воде.
Слайд 5
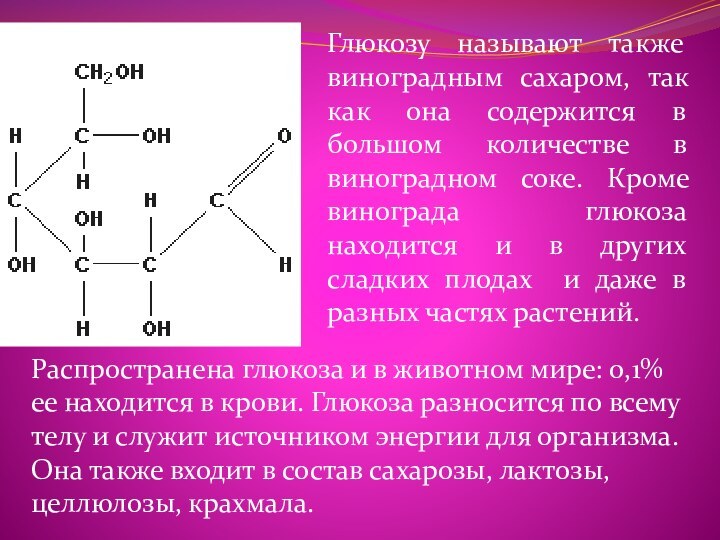
Строение и изомерия
Глюкоза является альдегидоспиртом
Слайд 6
Химические свойства глюкозы
Качественная реакция глюкозы с гидроксидом меди
(II)
Глюкоза содержит в своем составе пять гидроксильных групп и
одну альдегидную группу. Поэтому она относиться к альдегидоспиртам. Ее химические свойства похожи на свойства многоатомных спиртов и альдегидов. Реакция с гидроксидом меди (II) демонстрирует восстановительные свойства глюкозы. Прильем к раствору глюкозы несколько капель раствора сульфата меди (II) и раствор щелочи. Осадка гидроксида меди не образуется. Раствор окрашивается в ярко-синий цвет. В данном случае глюкоза растворяет гидроксид меди (II) и ведет себя как многоатомный спирт. Нагреем раствор. Цвет раствора начинает изменяться. Сначала образуется желтый осадок Cu2O, который с течением времени образует более крупные кристаллы CuO красного цвета. Глюкоза при этом окисляется до глюконовой кислоты.
СН2ОН – (СНОН)4 – СОН + Сu(ОН)2 → СН2ОН – (СНОН)4 – СООН + Сu2О↓+ Н2О
Слайд 7
Специфические свойства
Важнейшим свойством моносахаридов является их ферментативное брожение,
т.е. распад молекул на осколки под действием различных ферментов.
Брожение происходит в присутствии ферментов, выделяемых дрожжевыми грибками, бактериями или плесневыми грибками. В зависимости от природы действующего фермента различают реакции следующих видов:
Слайд 8
1.Спиртовое брожение:
C6H12O6 → 2C2H5-OH + 2CO2↑
2. Молочнокислое брожение:
C6H12O6
→ 2СH3-CH-COOH
│
OH
молочная кислота
3. Маслянокислое брожение:
C6H12O6 → C3H7COOH + 2H2 ↑+ 2CO2↑
Слайд 9
Свойства альдегидов:
1. Реакция серебряного зеркала:
СH2OH(CHOH)4-COH + Ag2O
t.NH3→ СH2OH(CHOH)4-COOH + 2Ag↓
глюконовая кислота
2. Окисление гидроксидом меди (II):
СH2OH(CHOH)4-COH + 2Cu(OH)2 t → СH2OH(CHOH)4-COOH + Cu2O + 2H2O
голубой красный
3. Восстановление:
СH2OH(CHOH)4-COH + H2 t,Ni → СH2OH(CHOH)4-CH2OH
сорбит – шестиатомный спирт
Слайд 10
Применение
Глюкоза является ценным питательным продуктом. В организме она
подвергается сложным биохимическим превращениям в результате которых образуется диоксид
углерода и вода, при это выделяется энергия согласно итоговому уравнению:
C6H12O6 + 6O2 → 6H2O + 6CO2 + 2800 кДж
Слайд 11
Так как глюкоза легко усваивается организмом, её используют
в медицине в качестве укрепляющего лечебного средства при явлениях
сердечной слабости, шоке, она входит в состав кровозаменяющих и противошоковых жидкостей. Широко применяют глюкозу в кондитерском деле (изготовление мармелада, карамели, пряников и т. д.), в текстильной промышленности в качестве восстановителя, в качестве исходного продукта при производстве аскорбиновых и глюконовых кислот, для синтеза ряда производных сахаров и т.д. Большое значение имеют процессы брожения глюкозы. Так, например, при квашении капусты, огурцов, молока происходит молочнокислое брожение глюкозы, так же как и при силосовании кормов. Если подвергаемая силосованию масса недостаточно уплотнена, то под влиянием проникшего воздуха происходит маслянокислое брожение и корм становится непригоден к применению. На практике используется также спиртовое брожение глюкозы, например при производстве пива.
Слайд 12
Глюкозу называют также виноградным сахаром, так как она
содержится в большом количестве в виноградном соке. Кроме винограда
глюкоза находится и в других сладких плодах и даже в разных частях растений.
Распространена глюкоза и в животном мире: 0,1% ее находится в крови. Глюкоза разносится по всему телу и служит источником энергии для организма. Она также входит в состав сахарозы, лактозы, целлюлозы, крахмала.
Слайд 13
Химические и физические свойства сахарозы
Молекулярная масса 342,3 а.

е. м. Вкус сладковатый. Растворимость: в воде 179 (0°C)
и 487 (100 °C), в этаноле 0,9 (20 °C). Малорастворима в метаноле. Не растворима в диэтиловом эфире. Плотность 1,5879 г/см3 (15 °C). Удельное вращение для D-линии натрия: 66,53 (вода; 35 г/100г; 20 °C). При охлаждении жидким воздухом, после освещения ярким светом кристаллы сахарозы фосфоресцируют. Не проявляет восстанавливающих свойств — не реагирует с реактивом Толленса и реактивом Фелинга. Не образует открытую форму, поэтому не проявляет свойств альдегидов и кетонов. Наличие гидроксильных групп в молекуле сахарозы легко подтверждается реакцией с гидроксидами металлов. Если раствор сахарозы прилить к гидроксиду меди (II), образуется ярко-синий раствор сахарата меди. Альдегидной группы в сахарозе нет: при нагревании с аммиачным раствором оксида серебра (I) она не дает «серебряного зеркала», при нагревании с гидроксидом меди (II) не образует красного оксида меди (I). Из числа изомеров сахарозы, имеющих молекулярную формулу С12Н22О11, можно выделить мальтозу и лактозу.
Слайд 14
Реакция сахарозы с водой
Если прокипятить раствор сахарозы с
несколькими каплями соляной или серной кислоты и нейтрализовать кислоту
щелочью, а после этого нагреть раствор, то появляются молекулы с альдегидными группами, которые и восстанавливают гидроксид меди (II) до оксида меди (I). Эта реакция показывает, что сахароза при каталитическом действии кислоты подвергается гидролизу, в результате чего образуются глюкоза и фруктоза:
Слайд 15
В молекуле сахарозы имеется несколько гидроксильных групп. Поэтому
соединение взаимодействует с гидроксидом меди (II) аналогично глицерину и
глюкозе. При добавлении раствора сахарозы к осадку гидроксида меди (II) он растворяется; жидкость окрашивается в синий цвет. Но, в отличие от глюкозы, сахароза не восстанавливает гидроксид меди (II) до оксида меди (I).
Реакция с гидроксидом меди (II)