- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
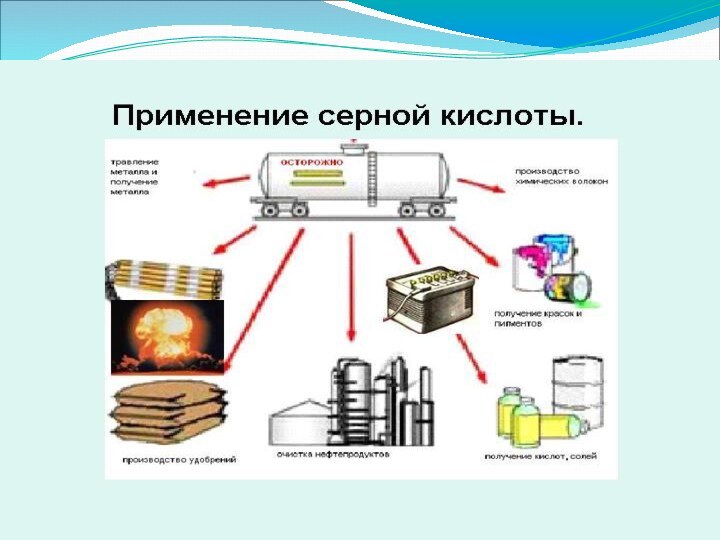
Презентация на тему Производство серной кислоты (польза и вред)
Содержание
- 2. Цель работы:
- 3. Серная кислота H2SO4 В технике серной
- 4. Серная кислота H2SO4 При обычных условиях
- 6. Сырьё, используемое для производства серной кислоты:Самородная сера
- 7. Сырьё, используемое для производства серной кислоты:Сульфиды цветных металловКристаллы сульфида цинка http://basik.ru/forum/index.php?showtopic=88Кристаллы сульфида медиhttp://www.terramarina.okis.ru/P_3.html
- 8. Производство серной кислоты.Серную кислоту в промышленности производят двумя способами: контактным и нитрозным. http://www.newchemistry.ru/letter.php?n_id=950
- 9. Производство серной кислоты.Основные стадии получения серной кислоты:Обжиг
- 10. Контактный способПодготовка сырья.Измельчение пирита.
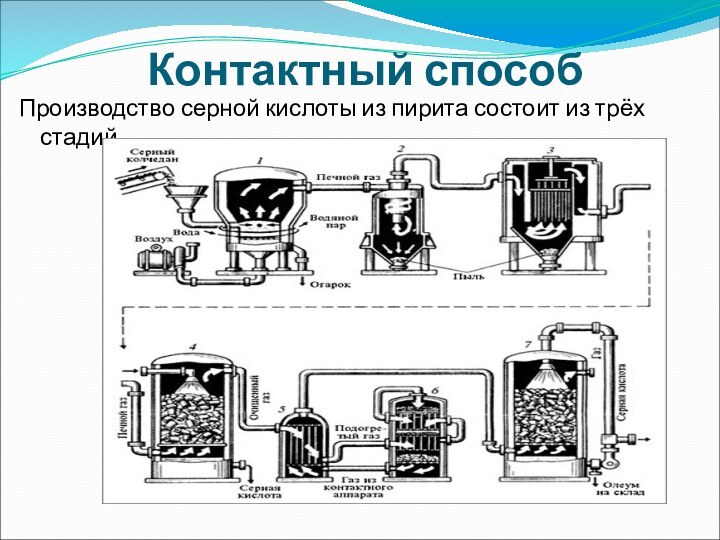
- 11. Контактный способПроизводство серной кислоты из пирита состоит из трёх стадий.
- 12. Контактный способПирит сверху засыпают в печь.
- 13. Контактный способ Очистку печного газа от
- 14. Контактный способВТОРАЯ СТАДИЯ - окисление SO2 в
- 15. Контактный способТРЕТЬЯ СТАДИЯ - поглощение SO3 серной
- 16. Нитрозный способСо стадии окисления SO2 до
- 17. Нитрозный способНедостаток нитрозного метода :серная кислота
- 18. Вред производства серной кислоты. В
- 19. Вред производства серной кислоты.Серная кислота и сульфаты
- 20. Скачать презентацию
- 21. Похожие презентации
Цель работы: Узнать:из чего получают серную кислоту;как получают серную кислоту;для чего получают серную кислоту;вредно ли производство серной кислоты?


















Слайд 3
Серная кислота H2SO4
В технике серной кислотой
называют её смеси как с водой, так и с
серным ангидридом.Если молярное отношение SO3 : H2O < 1, то это водный раствор серной кислоты, если > 1, — раствор SO3 в серной кислоте.
Раствор серного ангидрида в
серной кислоте называют
олеумом.
Слайд 4
Серная кислота H2SO4
При обычных условиях концентрированная
серная кислота — тяжёлая маслянистая жидкость без цвета и
запахаЭто сильная двухосновная
кислота, отвечающая высшей
степени окисления серы (+6).
Слайд 6
Сырьё, используемое для производства серной кислоты:
Самородная сера S
Пирит (серный колчедан)
FeS2http://www.catalogmineralov.ru/article/98.html
http://www.24open.ru/csucatudacha/blog/589875/
Сероводород H2S
http://www.manbw.ru/analitycs/hidrogen_sulfide_h2s.html
Слайд 7
Сырьё, используемое для производства серной кислоты:
Сульфиды цветных металлов
Кристаллы сульфида цинка
http://basik.ru/forum/index.php?showtopic=88
Кристаллы
сульфида меди
http://www.terramarina.okis.ru/P_3.html
Слайд 8
Производство серной кислоты.
Серную кислоту в
промышленности
производят двумя
способами: контактным
и нитрозным.
http://www.newchemistry.ru/letter.php?n_id=950
Слайд 9
Производство серной кислоты.
Основные стадии получения серной кислоты:
Обжиг сырья
с получением SO2
Окисление SO2 в SO3
АбсорбцияSO3
В промышленности применяют
два метода окисления SO2 :
контактный
— с использованием твердых катализаторов(контактов)
и нитрозный — с оксидами азота.
http://www.karabash-info.ru/?pg=wall&wall=5
Слайд 10
Контактный способ
Подготовка сырья.
Измельчение пирита.
Перед использованием большие куски пирита измельчают
в дробильных машинах.
Очистка пирита.
После измельчения пирита, его очищают методом флотации. Для этого измельчённый пирит опускают в огромные чаны с водой, перемешивают, пустая порода всплывает наверх, затем пустую породу удаляют.
Слайд 12
Контактный способ
Пирит сверху засыпают в печь. Снизу
пропускают воздух,
обогащённый кислородом. Температура в печи -800°С
4FeS2 + 11O2 → 2Fe2O3 + 8SO2 + Q
Выделяющейся теплотой :поддерживается температура в
печи, а избытком отапливают рядом стоящие
помещения.
Оксид железа Fe2O3 (огарок) используют
для получения железа и его сплавов на
металлургических заводах .
Принципы химического производства :
безотходность производства., принцип противотока,
принцип теплообмена
ПЕРВАЯ СТАДИЯ - обжиг пирита в печи для обжига в "кипящем слое".
Слайд 13
Контактный способ
Очистку печного газа от
твёрдых
частичек огарка
проводят в циклоне и в
электрофильтрах .
Очистка
печного газа Для осушки печного газа
используют серную
концентрированную кислоту,
(хорошо поглощает воду).
Слайд 14
Контактный способ
ВТОРАЯ СТАДИЯ - окисление SO2 в SO3 кислородом.
2SO2 +
O2 2SO3 + Q
Оптимальные
условия реакции:температура 400-500°С (температура в
контактном аппарате поддерживается за счёт
теплоты в реакции превращения SO2 в SO3. ) Нагрев
смеси начинается в теплообменнике, который
установлен перед контактным аппаратом.
катализатор- оксид ванадия V2O5;
повышенное давление.
Контактный
аппарат
Слайд 15
Контактный способ
ТРЕТЬЯ СТАДИЯ - поглощение SO3 серной кислотой.
nSO3 +
H2SO4 H2SO4·nSO3Для того, чтобы не образовывалось
сернокислотного тумана, используют
98%- ную концентрированную
серную кислоту.
Оксид серы очень хорошо растворяется в
такой кислоте, образуя олеум: H2SO4·nSO3,
который и перевозят по назначению по ж/д
Поглотительная башня
Слайд 16
Нитрозный способ
Со стадии окисления SO2 до H2SO4,.оба
метода отличаются друг от друга.
В специальной окислительной башне смешивают
окись азота NO и NO2 своздухом
2NO + O2 → 2NO2
Смесь подаётся в башни орошаемые 75% - ной серной кислотой; здесь смесь окислов азота поглощается с образованием нитрозиллерной кислоты:
NO + NO2 + 2H2SO4 →2NO(HSO4) + H2O
Раствор нитрозиллерной кислоты в серной кислоте, называемый нитрозой, орошает башни , куда противотоком поступает SO2 ,и добавляется вода.
В результате гидролиза нитрозиллерной кислоты образуется азотная кислота:
NO(HSO4) + H2O→H2SO4 + HNO2
Она - то и окисляет SO2 по уравнению:
SO2 + 2HNO2→H2SO4 + 2NO
Слайд 17
Нитрозный способ
Недостаток нитрозного метода :
серная кислота имеет
концентрацию лишь 75% (при большей концентрации плохо идёт гидролиз
нитрозиллерной кислоты).;башенная серная кислота бывает недостаточно чистой, что ограничивает её применение.
Преимущество нитрозного метода :
примеси ,содержащиеся в SO2, не влияют на ход процесса, так что исходный SO2 достаточно очистить от пыли.
Слайд 18
Вред производства серной кислоты.
В зоне
до 300 км от источника загрязнения (SO2) опасность представляет
серная кислота,
в зоне до 600 км. -
сульфаты.
http://www.mobus.com/kharkov/235677.html
Слайд 19
Вред производства серной кислоты.
Серная кислота и сульфаты приводят:
к
замедлению роста с/х культур;
к закислению водоемов (влечёт гибель икр и
молоди рыб);к разрушению конструкций из известняка и мрамора;
повышение коррозионного износа металлов;
увеличение количества случаев респираторных заболеваний человека и животных;
громадные суммы каждый год теряются при раскислении почв.