общего найдет математик и физик
между молекулой метана
и пакетом молока?
Что
делать химику с алканами?Экологи и технологи спорят: алканы – зло или благо?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Email: Нажмите что бы посмотреть





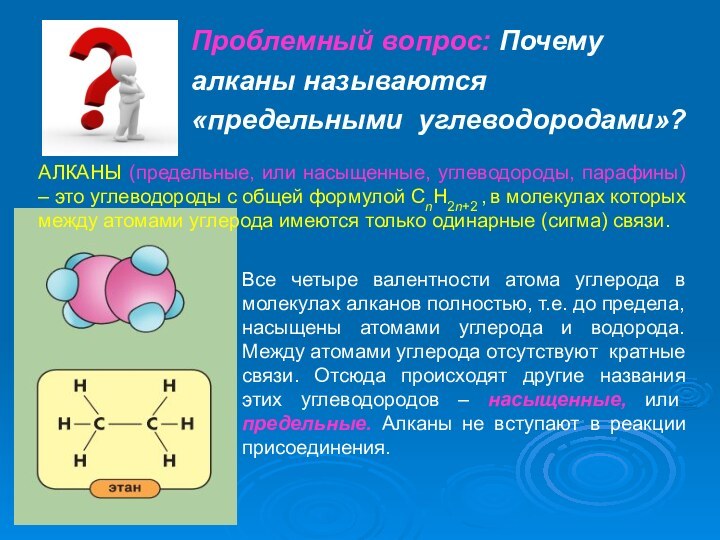



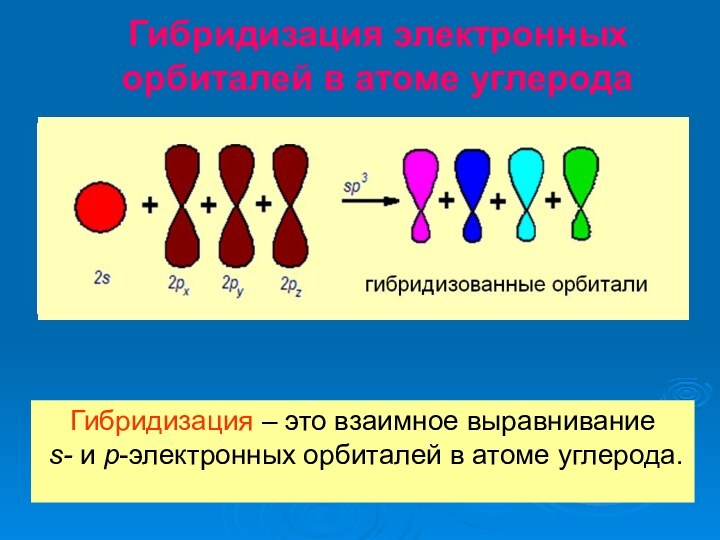




























Все четыре валентности атома углерода в молекулах алканов полностью, т.е. до предела, насыщены атомами углерода и водорода. Между атомами углерода отсутствуют кратные связи. Отсюда происходят другие названия этих углеводородов – насыщенные, или предельные. Алканы не вступают в реакции присоединения.
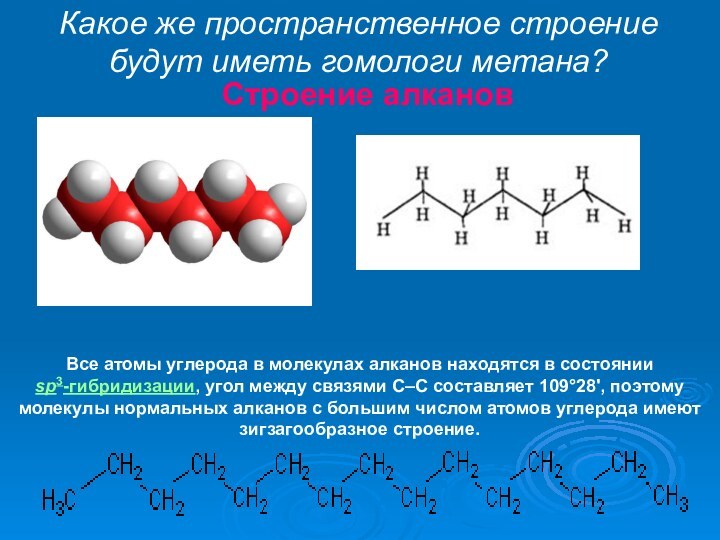
Какое же пространственное строение
будут иметь гомологи метана?
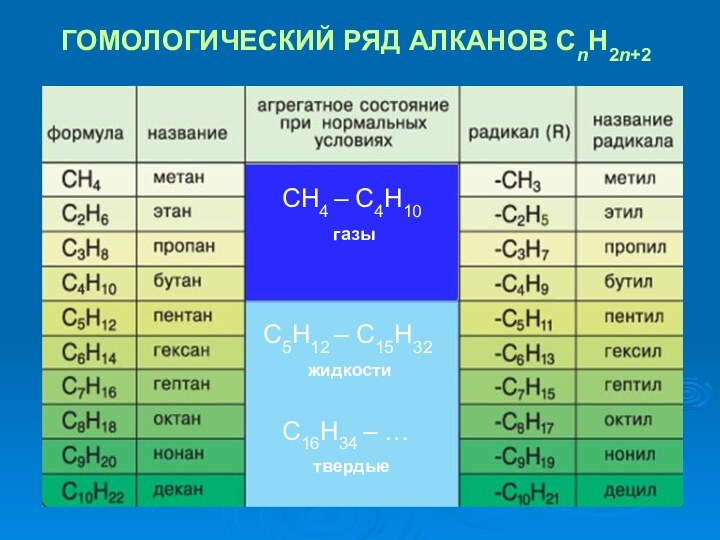
CH4…C4H10
Газы (без запаха)
C16H34…
Твердые вещества
(без запаха)
Физические свойства алканов
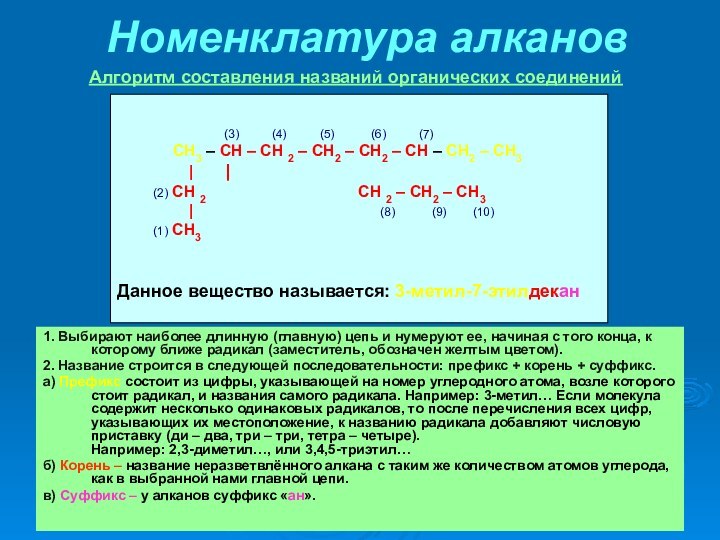
(3) (4) (5) (6) (7)
СН3 – СН – СН 2 – СН2 – СН2 – СН – СН2 – СН3
| |
(2) СН 2 СН 2 – СН2 – СН3
| (8) (9) (10)
(1) СН3
Данное вещество называется: 3-метил-7-этилдекан
Алгоритм составления названий органических соединений
CH3 CH CH3 + HNO3 CH3 C CH3 + H2O.
CH3 CH3
СН3–СН3 + Сl2 CH2Cl–CH3 + HCl.
Реакции замещения у алканов
1) Галогенирование (действие галогенов):
ЗАПОМНИ! Реакция начинается при освещении и носит радикально-цепной
характер.
2) Нитрование (реакция Коновалова):
ЗАПОМНИ! Реакция нитрования происходит при нагревании и приводит
к образованию нитросоединений.
2) Каталитическое окисление алканов.
2. Крекинг – разложение больших молекул
на молекулы с меньшим количеством
атомов углерода:
1. Пиролиз
C16H34
t
C8H18
+
C8H16.
t
гексадекан октан октен
Запуск видео
Ni, 300 °C
t
Группа «Экологи и технологи»
Утечка нефти приводит
к экологическим катастрофам.
Какие птицы
помогали шахтёрам?
Канарейки очень чувствительны к содержанию в воздухе метана. Эту особенность использовали в своё время шахтёры, которые, спускаясь под землю, брали с собой клетку с канарейкой. Если пения давно не было слышно, значит, следовало
подниматься наверх
как можно
быстрее.
Удивительное
рядом!
t
Ответ:
C2H2.