- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентации по Химии

Введение Вся жизнь человека неразрывно связана с атмосферным воздухом. Причем для нормальной жизнедеятельности он должен удовлетворять многим параметрам. Температура, влажность, давление, процентное содержание углекислого газа, степень загрязненности – это лишь малая часть параметров, от которых зависит жизнедеятельность. При их отклонении от нормы

Дмитрий Иванович Менделеев(1834-1907) - русский ученый-энциклопедист, талантливый химик, открывший Периодический закон и разработавший Периодическую систему химических элементов. Создана вырезка экрана: 01.10.2008; 17:01 8 февраля 1834 – 2 февраля 1907 года Автор фундаментальных исследований по химии, химической технологии, физике, метрологии, воздухоплаванию, метеорологии, сельскому

Цель урока:1. Рассмотрение свойств разбавленной серной кислоты с точки зрения электролитической диссоциации.2. Продолжить формирование умений и навыков , сравнивать и обобщать, отработать умения составлять уравнения реакций в молекулярном и ионном виде.. Тип урока:1. Урок усвоения новых знаний учащимися.Формы обучения:1. Коллективные2.

Алке́ны (олефины, этиленовые углеводороды) — ациклические непредельные углеводороды, содержащие одну двойную связь между атомами углерода, образующие гомологический ряд с общей формулой CnH2n. Атомы углерода при двойной связи находятся в состоянии sp² гибридизации, и имеют валентный угол 120°. Простейшим алкеном является этилен (C2H4).

Пример:2Cu0 + O2 =2 Cu2+O2-2H+CL- + Zn0 = Zn2+CL2- + H20Реакции, протекающие с изменением степеней окисления атомов всех или некоторых элементов, входящих в состав реагирующих веществ, называют окислительно-восстановительными. Восстановитель-это вещество , в состав которого входит элемент, отдающий электроныMg0 – 2e- =

Состав и строениеЖиры - органические соединения, полные сложные эфиры глицерина (триглицериды) и одноосновных жирных кислот; входят в класс липидов. Наряду с углеводами и белками Ж. — один из главных компонентов клеток животных, растений и микроорганизмов. Пищевые жиры – необходимая составная часть

Общие сведения о химии Химия - одна из важнейших и обширных областей естествознания, наука о веществах, их свойствах, строении и превращениях, происходящих в результате химических реакций, а также фундаментальных законах, которым эти превращения подчиняются.Современная химия является одной из самых обширных

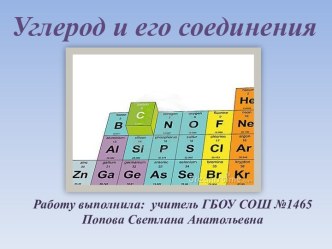
Шведский химик Й.Берцелиус Символы химических элементов - начальные буквы латинских названий химических элементов Например,Водород (латинское название – Hydrogenium (гидрогениум)) – обозначение «Н» (читается «аш»)Кислород (латинское название – Oxygenium (оксигениум)) – обозначение «О» (читается «о»)Углерод (латинское название – Carboneum (карбонеум))
Презентации из раздела Химия. Для просмотра учебных материалов воспользуйтесь проигрывателем. Любую презентацию на заданную тему можно скачать внизу страницы, поделившись ссылкой в социальных сетях. Не забудьте добавить наш сайт презентаций в закладки!