- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Физические и химические свойства оснований
Содержание
- 2. Цель урока:Рассмотреть физические и химические свойства оснований
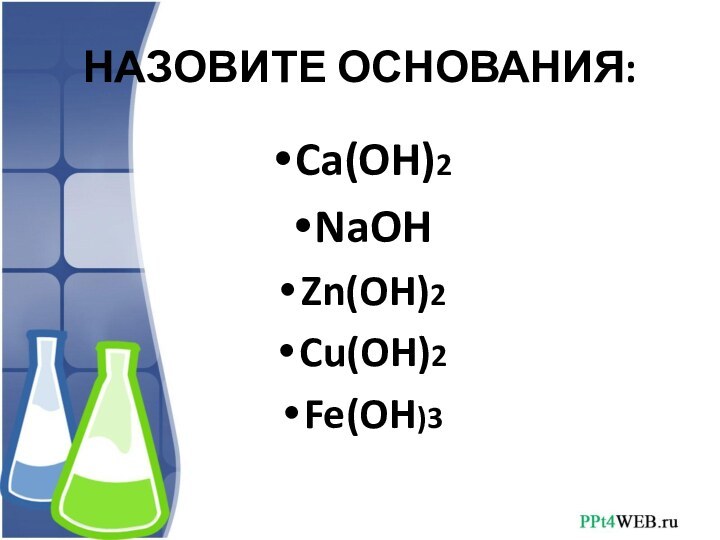
- 3. НАЗОВИТЕ ОСНОВАНИЯ:Ca(OH)2NaOHZn(OH)2 Cu(OH)2 Fe(OH)3
- 4. СОСТАВЬТЕ ФОРМУЛЫ ОСНОВАНИЙ: литиябария железа (II) меди(I) алюминияКАКИЕ ИЗ НИХ ОТНОСЯТСЯ К ЩЕЛОЧАМ?
- 5. ФИЗИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙГидроксид калияГидроксид натрияГидроксид алюминияГидроксид железа (III)Гидроксид свинца (II)Гидроксид никеля(II)
- 6. Действие щелочей на индикаторы
- 7. ХИМИЧЕСКИЕ СВОЙСТВА1. Реакция нейтрализации:NaOH + HCl =
- 8. ХИМИЧЕСКИЕ СВОЙСТВАРеакция нейтрализации: Cu(OH)2 ↓ + 2HCl
- 9. Взаимодействие щелочи с раствором соли:
- 10. 2.Щелочи взаимодействуют с растворами солей:2NaOH + CuSO4
- 11. 3.Щелочи взаимодействуют С КИСЛОТНЫМИ ОКСИДАМИ, ОБРАЗУЯ СОЛЬ
- 12. 4.НЕРАСТВОРИМЫЕ ОСНОВАНИЯпри нагревании разлагаются:Cu(OH)2 = CuO +
- 13. Домашнее задание:§ 31, упр. № 5 (п) стр.99
- 14. Скачать презентацию
- 15. Похожие презентации
Цель урока:Рассмотреть физические и химические свойства оснований












Слайд 5
ФИЗИЧЕСКИЕ СВОЙСТВА ОСНОВАНИЙ
Гидроксид
калия
Гидроксид
натрия
Гидроксид алюминия
Гидроксид
железа (III)
Гидроксид
свинца (II)
Гидроксид никеля(II)
Слайд 7
ХИМИЧЕСКИЕ СВОЙСТВА
1. Реакция нейтрализации:
NaOH + HCl = NaCl
+ H2O
гидроксид соляная хлорид
воданатрия кислота натрия
(соль)
Реакция нейтрализации относится к реакциям обмена
Слайд 8
ХИМИЧЕСКИЕ СВОЙСТВА
Реакция нейтрализации:
Cu(OH)2 ↓ + 2HCl =
CuCl2 +2 H2O
гидроксид
соляная хлорид водамеди (II) кислота меди(II)
(соль)
тип реакции: обмен
Слайд 10
2.Щелочи взаимодействуют с растворами солей:
2NaOH + CuSO4 =Cu(OH)2↓+Na2SO4
гидроксид
сульфат гидроксид сульфат
натрия
меди(II) меди(II) натрия(щелочь) (соль) (основание) (соль)
Слайд 11
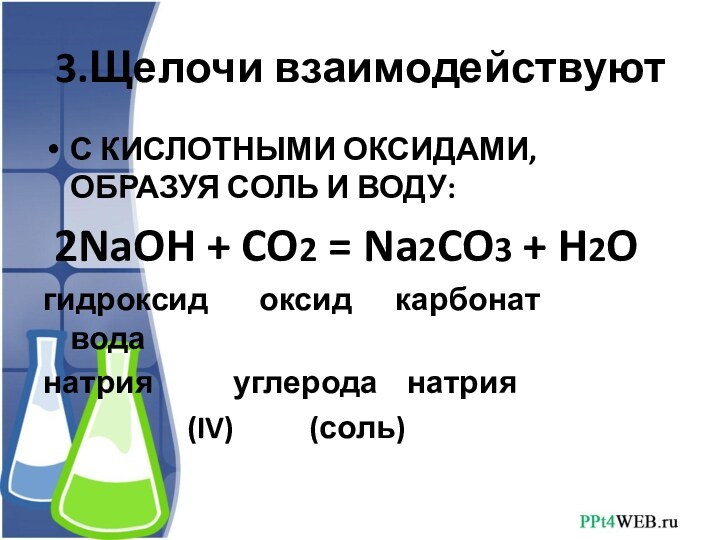
3.Щелочи взаимодействуют
С КИСЛОТНЫМИ ОКСИДАМИ, ОБРАЗУЯ СОЛЬ И
ВОДУ:
2NaOH + CO2 = Na2CO3 + H2O
гидроксид
оксид карбонат воданатрия углерода натрия
(IV) (соль)