- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему БОЛЕЗНЬ ИЦЕНКО
Содержание
- 2. Гипофиз- небольшая железа внутренней секреции, расположенная в
- 3. Гистологически в передней доле гипофиза различают 3
- 4. Промежуточная доля – МСГ, некоторые авторы ее
- 5. Гормоны гипофизасоматотропный гормон (СТГ)стимулирует синтез белка в
- 6. Гормоны гипофизаЛТГ (пролактин) – гонадотропный гормон, т.к.
- 7. Гормоны гипофизаАДГ (антидиуретический гормон, вазопрессин) и окситоцин
- 8. Гипоталамус и гипофиз представляют собой единую взаимосвязанную
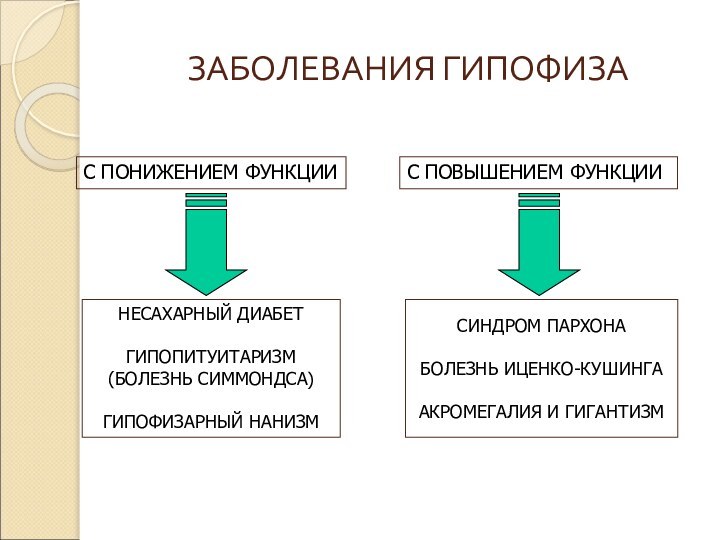
- 9. ЗАБОЛЕВАНИЯ ГИПОФИЗА
- 10. Болезнь Иценко-Кушинга Заболевание, проявляющееся двусторонней гиперплазией надпочечников,
- 11. Болезнь Иценко-КушингаЭтиология: - черепно-мозговая травма; -
- 12. Болезнь Иценко-КушингаПатогенез Под влиянием избыточной продукции
- 13. Болезнь Иценко-КушингаЗаболевание в 4-5 раз чаще встречается
- 14. нарушение менструального цикла проявляется в виде опсо-,
- 15. Болезнь Иценко-Кушинга
- 16. Болезнь Иценко-Кушинга полицитемии, лимфоцитопения, эозинопения и нейтрофильный
- 17. Болезнь Иценко-Кушингапарлодел (бромкриптин) в дозе 2,5-7,0 мг
- 18. Болезнь Иценко-КушингаБольная Е.: А – до лечения, Б – через 3 года после субтотальной адреналэктомии.
- 19. Надпочечники – парная эндокринная железа, располагающаяся над
- 20. Корковое вещество надпочечника состоит из трех зон:
- 21. НАДПОЧЕЧНИКИ
- 22. МИНЕРАЛОКОРТИКОИДЫ (альдостерон, дезоксикортикостерон) регулируют водно-минеральный обмен;способствуют
- 23. РЕГУЛЯЦИЯ СЕКРЕЦИИ АЛЬДОСТЕРОНАактивностью ренин-ангиотензиновой системы;концентрацией ионов калия
- 24. Роль альдостерона в регуляции давления крови и уровня натрия
- 25. ГЛЮКОКОРТИКОИДЫ (КОРТИЗОЛ, КОРТИЗОН, КОРТИКОСТЕРОН)усиливают глюконеогенез из
- 26. ПОЛОВЫЕ КОРТИКОСТЕРОИДЫ (ТЕСТРОСТЕРОН, ЭСТРАДИОЛ)участвуют в формировании половых
- 27. КАТЕХОЛАМИНЫ. Адреналинусиливает сердечные сокращения;ускоряет пульс;повышает АД,
- 28. КАТЕХОЛАМИНЫ. Норадреналинне оказывает влияния на углеводный
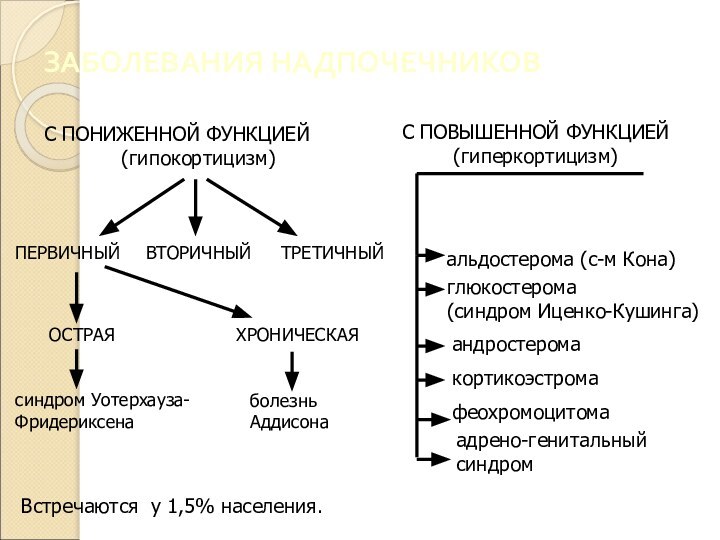
- 29. ЗАБОЛЕВАНИЯ НАДПОЧЕЧНИКОВ
- 30. ХРОНИЧЕСКАЯ НЕДОСТАТОЧНОСТЬ КОРЫ НАДПОЧЕЧНИКОВ (Аддисонова болезнь, гипокортицизм,
- 31. Этиологиятуберкулез;идиопатическая атрофия коры надпочечников (антигены к митохондриям и микросомальной фракции);кровоизлияния в надпочечники;амилоидоз;сифилис.
- 32. ПатогенезДефицит глюкокортикоидов приводит к адинамии, сердечно-сосудистым и
- 33. Патогенез и развитие клинических симптомов при болезни Аддисона
- 34. КЛАССИФИКАЦИЯПо клиническому течению:типичная форма;атипичная форма (гипоальдостеронизм, беспигментная
- 35. КЛИНИКА
- 36. КЛИНИКАгиперпигментации кожи и слизистых, пигментация послеоперационных рубцов,
- 37. ЛАБОРАТОРНАЯ ДИАГНОСТИКАВ анализе крови: лимфоцитоз, эозинофилия, СОЭ
- 38. ДИАГНОСТИЧЕСКИЕ ПРОБЫ:Проба с АКТГ (синактеном): в/в вводят
- 39. ДИАГНОСТИЧЕСКИЕ ПРОБЫ (продолжение)Водная проба Робинсона-Пауэра-Кеплера основана на
- 40. ДИАГНОСТИЧЕСКИЕ ПРОБЫ (продолжение)Для дифференциальной диагностики первичной и
- 41. ЛЕЧЕНИЕлегкая форма (диета бедная солями калия и
- 42. ОСТРАЯ НЕДОСТАТОЧНОСТЬ КОРЫ НАДПОЧЕЧНИКОВ (Аддисонический криз)Этиология: инфекция,
- 43. ОСТРАЯ НЕДОСТАТОЧНОСТЬ КОРЫ НАДПОЧЕЧНИКОВКлиника:снижение АД (коллапс или
- 44. ОСТРАЯ НЕДОСТАТОЧНОСТЬ КОРЫ НАДПОЧЕЧНИКОВЛабораторная диагностика:в крови: снижение
- 45. ОСТРАЯ НЕДОСТАТОЧНОСТЬ КОРЫ НАДПОЧЕЧНИКОВЛечение:глюкокортикоиды: преднизолон 150-200мг или
- 46. Скачать презентацию
- 47. Похожие презентации

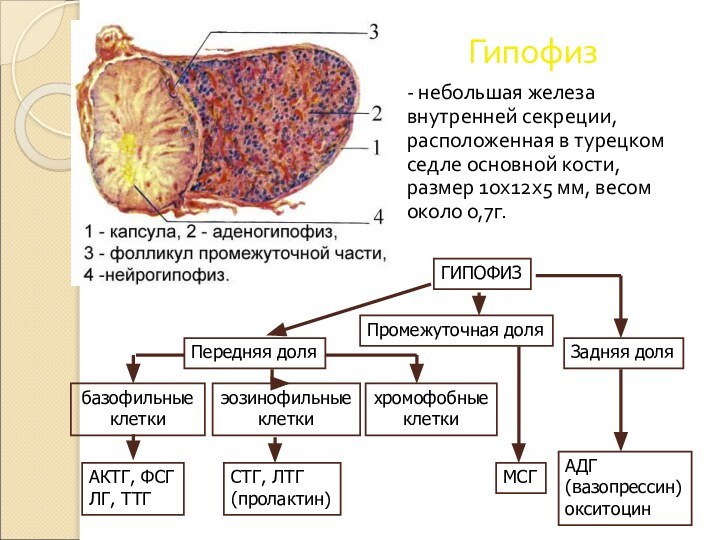




































Слайд 3 Гистологически в передней доле гипофиза различают 3 группы
клеток:
базофильные клетки составляют 4-10% клеточного состава аденогипофиза, которые подразделяются
на 3 подтипа клеток, секретирующих АКТГ, ТТГ, ФСГ и ЛГ;эозинофильные клетки, составляют 30-35% клеточного состава и подразделяются на 2 подтипа клеток, секретирующих соответственно СТГ и пролактин;
хромофобные клетки (50-60%) не принимают участия в гормонообразовании, они являются лишь источником для образования эозино- и базофилов.
Слайд 4 Промежуточная доля – МСГ, некоторые авторы ее относят
к передней доле или аденогипофизу.
Задняя доля гипофиза (нейрогипофиз) служит
резервуаром для хранения нейрогормонов – вазопрессина и окситоцина, которые поступают сюда по аксонам клеток, расположенных в гипоталамических ядрах, где осуществляется их синтез. Нейрогипофиз – место не только депонирования, но и своеобразной активации поступающих сюда нейрогормонов, после чего они высвобождаются в кровь.
Слайд 5
Гормоны гипофиза
соматотропный гормон (СТГ)
стимулирует синтез белка в костях,
печени и других внутренних органах;
на жировой обмен оказывает
преходящее (в течение 30-40мин) липогенетическое действие, затем усиливает процессы липолиза;на углеводный обмен оказывает кратковременно (в течение 30-40 мин) инсулиноподобное действие, затем активируется глюконеогенез в печени;
стимулирует функцию α-клеток, повышает содержание глюкогона, который в свою очередь активирует ферменты, разрушающие инсулин, что приводит со временем к абсолютной инсулиновой недостаточности и развитию СД;
под влиянием СТГ растут тканевые структуры организма, включая соединительную ткань, мышцы и внутренние органы (сердце, легкие, печень). Механизм этого действия заключается в стимуляции образования и высвобождения соматомединов, инсулиноподобного фактора роста І и ІІ, которые являются посредниками анаболического и ростового влияния СТГ;
уровень СТГ в сыворотке крови – 1-4.5 нг/мл
Слайд 6
Гормоны гипофиза
ЛТГ (пролактин) – гонадотропный гормон, т.к. стимулирует
функцию желтого тела. Однако основное физиологическое действие пролактина –
стимуляция секреции молочных желез;АКТГ (адренокортикотропный гормон) – стимулирует через кору надпочечников синтез глюкокортикоидов, а также частично – минералортикоидов;
ТТГ (тиреотропный гормон) – стимулирует биосинтез тиреоидных гормонов (Т3, Т4), их поступление в кровь, способствует гиперпластическим процессам в железистой ткани щитовидной железы;
ФСГ (фолликулостимулирующий гормон) – гонадотропный гормон (стимулирует деятельность половых желез), у женщин активирует рост фолликулов яичников, у мужчин – рост эпителия семенных канальцев;
ЛГ (лютеинизирующий гормон) - гонадотропный гормон (стимулирует деятельность половых желез), у женщин способствует овуляции и развитию желтого тела в яичниках, у мужчин – стимулирует рост и функцию интерстициальных клеток (клетки Лейдига) в семенниках.
Слайд 7
Гормоны гипофиза
АДГ (антидиуретический гормон, вазопрессин) и окситоцин вырабатываются
в супраоптических и паравентрикулярных ядрах гипоталамуса и по ножке
спускаются в нейрогипофиз, где накапливаются в тельцах ГерингаАДГ – усиливает реабсорбцию воды в дистальных отделах почечных канальцев, что ведет к уменьшению диуреза
Окситоцин – стимулирует сокращение матки, усиливает лактацию
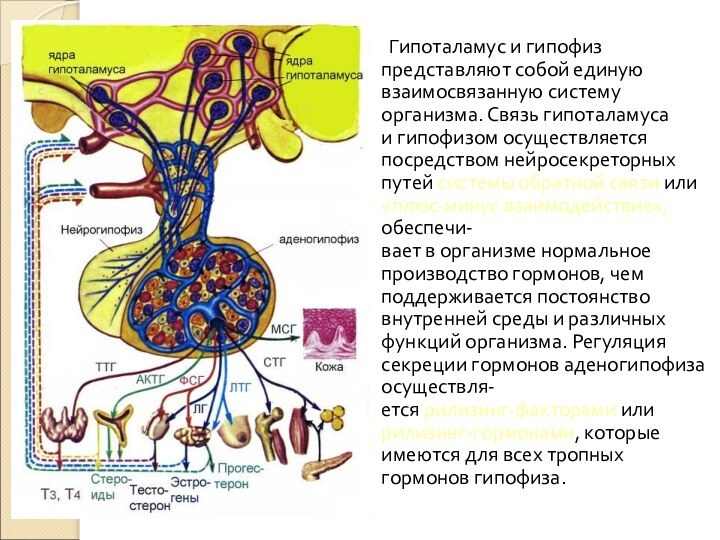
Слайд 8 Гипоталамус и гипофиз представляют собой единую взаимосвязанную систему
организма. Связь гипоталамуса и гипофизом осуществляется посредством нейросекреторных путей
системы обратной связи или «плюс-минус взаимодействие», обеспечи- вает в организме нормальное производство гормонов, чем поддерживается постоянство внутренней среды и различных функций организма. Регуляция секреции гормонов аденогипофиза осуществля- ется рилизинг-факторами или рилизинг-гормонами, которые имеются для всех тропных гормонов гипофиза.
Слайд 10
Болезнь Иценко-Кушинга
Заболевание, проявляющееся двусторонней гиперплазией надпочечников, повышенной
секрецией АКТГ и гормонов коры надпочечников.
Впервые заболевание описал
в 1924 г русский невропатолог Н.М.Иценко, в 1932 г. аналогичный симптомокомплекс был описан американским нейрохирургом Кушингом .
Слайд 11
Болезнь Иценко-Кушинга
Этиология:
- черепно-мозговая травма;
- нейроинфекция;
- гормональная перестройка
в период климакса, беременности и др.
Слайд 12
Болезнь Иценко-Кушинга
Патогенез
Под влиянием избыточной продукции кортиколиберина, секреция
которого стимулируется серотонин- и ацетилхолинэргическими нейронами, происходит гиперплазия клеток
аденогипофиза, вырабатывающих АКТГ. При длительной продукции кортиколиберина такая гиперплазия, развиваясь, превращается в микроаденому, затем в аденому со способностью к автономной продукции АКТГ. Это приводит к двусторонней гиперплазии коры надпочечников, увеличению синтеза и секреции кортикостероидов, которые, влияя на обмен веществ, обусловливают клиническую симптоматику болезни Иценко-Кушинга.
Слайд 13
Болезнь Иценко-Кушинга
Заболевание в 4-5 раз чаще встречается у
женщин, и наиболее часто начало его приходится на возраст
25-45 лет.ожирение (наблюдается отложение жира в области плечевого пояса, живота, надключичных пространств, лица, молочных желез и спины. Лицо становится лунообразным, круглым, щеки – красными. Все это создает характерный вид лица - «матронизм». Ожирение наблюдается у 95% больных. );
розово-пурпурные стрии, которые связаны с нарушением белкового обмена (катаболизм белка), располагаются на коже живота, подмышечной области, плечевого пояса, бедер и ягодиц;
избыточное оволосение, гирсутизм;
артериальная гипертония, обычно умеренная, но иногда 220-225 на 130-145 мм рт.ст.(задержка натрия приводит к повышению объема циркулирующей крови);
Клиника
Слайд 14 нарушение менструального цикла проявляется в виде опсо-, олиго-
или аменореи, которая встречается у 70-80% больных;
мышечная слабость, связана
с гипокалиемией. Иногда бывает настолько выраженной, что больные без посторонней помощи не могут встать со стула.;остеопороз и даже патологические переломы позвоночника и конечностей выявляется у 90% больных. Катаболическое действие глюкокортикоидов приводит к уменьшению белковой матрицы кости, снижается содержание в кости органического вещества и его компонентов, что приводит к повышенной резобции кальция из кости. Наряду с этим уменьшается всасывание кальция в кишечнике и увеличивается его потеря с мочой.
Болезнь Иценко-Кушинга
Клиника
Слайд 16
Болезнь Иценко-Кушинга
полицитемии, лимфоцитопения, эозинопения и нейтрофильный лейкоцитоз;
снижение калия;
ренгенологически
остеопороз костей скелета;
повышение уровня АКТГ и кортикостероидов на протяжении
всех 24 часов (отмечается нарушение их суточного ритма).Лабораторные данные:
Слайд 17
Болезнь Иценко-Кушинга
парлодел (бромкриптин) в дозе 2,5-7,0 мг в
день;
лучевая терапия проводится по дробно-интенсивной методике возрастающими дозами по
75-100-150-200-250 рад сначала через день, а затем ежедневно с таким расчетом, чтобы больной в течение недели получал 900-1000 рад (курсовая доза 4500-5000 рад). Более стойкая ремиссия достигается повторением через 7-9 мес курса облучения. Удовлетворительтные результаты наблюдаются у 50-60% больных;гипофизэктомия;
одно- или двусторонняя адреналэктомия ( проводят в 2 этапа, после удаления второго надпочечника кортизол 250-300 мг, в последующие дни (8-9 дню) дозу снижают до 100 мг, затем переводят на преднизолон в суточной дозе 5-15 мг, причем 2/3 дозы утром, 1/3 дозы – в вечернее время);
комбинированная терапия (односторонняя адреналэктомия с последующей рентгено- или медикаментозной терапией).
Лечение:
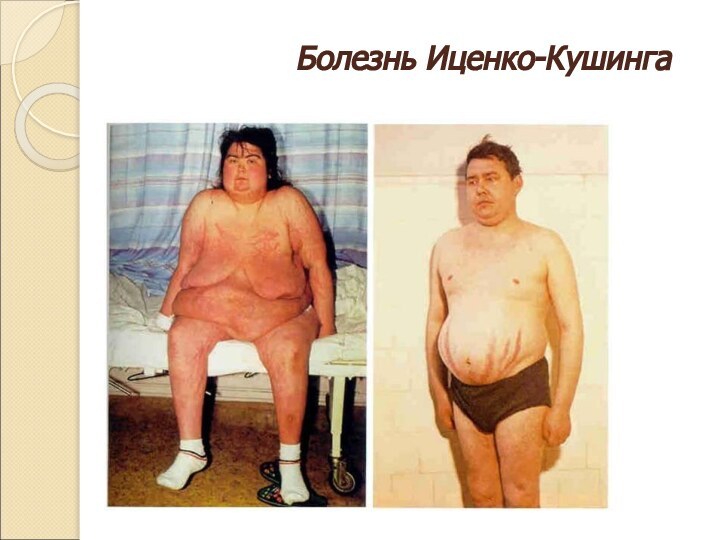
Слайд 18
Болезнь Иценко-Кушинга
Больная Е.: А – до лечения, Б
– через 3 года после субтотальной адреналэктомии.
Слайд 19 Надпочечники – парная эндокринная железа, располагающаяся над верхними
полюсами почек на уровне между I поясничным и XI
грудным позвонком, треугольные по форме.Масса обоих надпочечников колеблется от 6 до 12 г, длина достигает 4-6 см, ширина – 2-3 см, толщина до 1 см.
Снаружи надпочечник окружен соединительнотканной капсулой.
Надпочечник состоит из наружного коркового и внутреннего мозгового вещества.
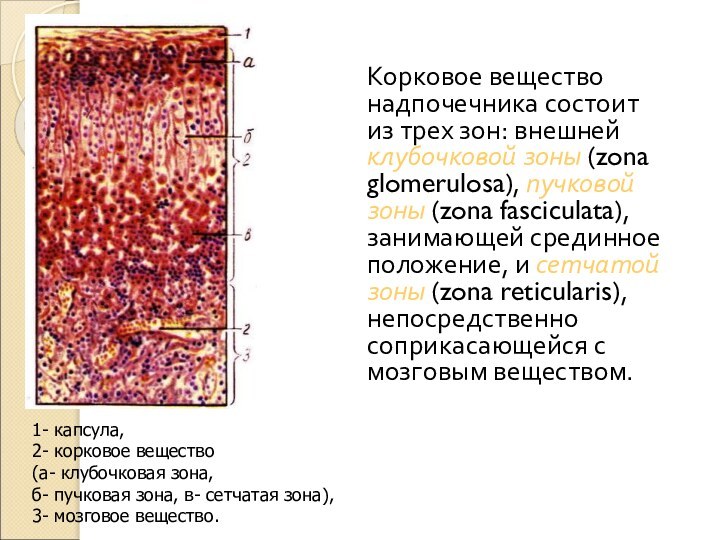
Слайд 20 Корковое вещество надпочечника состоит из трех зон: внешней
клубочковой зоны (zona glomerulosa), пучковой зоны (zona fasciculata), занимающей
срединное положение, и сетчатой зоны (zona reticularis), непосредственно соприкасающейся с мозговым веществом.1- капсула,
2- корковое вещество
(а- клубочковая зона,
б- пучковая зона, в- сетчатая зона),
3- мозговое вещество.
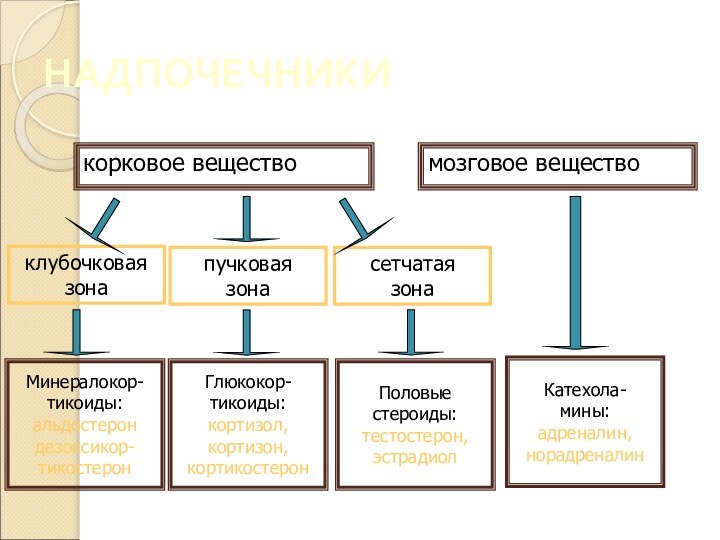
Слайд 22
МИНЕРАЛОКОРТИКОИДЫ
(альдостерон, дезоксикортикостерон)
регулируют водно-минеральный обмен;
способствуют реабсорбции ионов
натрия в почечных канальцах;
понижают выделение натрия с мочой;
усиливают выделение
ионов калияУвеличение гидрофильности тканей,
объема плазмы,
повышение артериального давления
Слайд 23
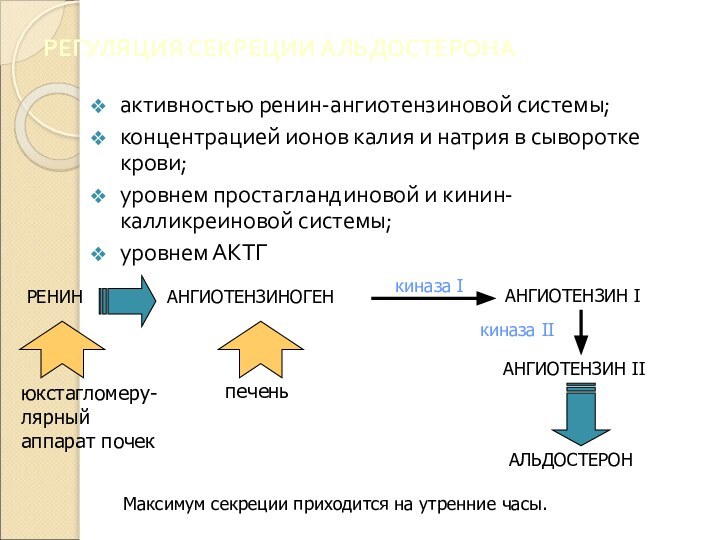
РЕГУЛЯЦИЯ СЕКРЕЦИИ АЛЬДОСТЕРОНА
активностью ренин-ангиотензиновой системы;
концентрацией ионов калия и
натрия в сыворотке крови;
уровнем простагландиновой и кинин-калликреиновой системы;
уровнем АКТГ
Максимум
секреции приходится на утренние часы.
Слайд 25
ГЛЮКОКОРТИКОИДЫ
(КОРТИЗОЛ, КОРТИЗОН, КОРТИКОСТЕРОН)
усиливают глюконеогенез из белка и
жира;
участвуют в транспорте глюкозы в скелетных мышцах;
участвуют в адаптации
организма к действию стресс-факторов (оказывают сильное противовоспалительное и антиаллергическое действие - уменьшают проницаемость капилляров, уменьшают образование антител);обладают слабыми минералокортикоидными свойствами.
Секреция кортизола имеет характерный суточный ритм: максимум приходится на утренние часы – 6-8 ч утра.
Секреция глюкокортикоидов находится под контролем АКТГ и кортиколиберина (по принципу обратной связи).
Участвуют в регуляции углеводного, белкового и липидного обменов.
Слайд 26
ПОЛОВЫЕ КОРТИКОСТЕРОИДЫ
(ТЕСТРОСТЕРОН, ЭСТРАДИОЛ)
участвуют в формировании половых гормонов и
развитии вторичных половых признаков;
участвуют в регуляции либидо.
Концентрация половых кортикостероидов
изменяется на протяжении суток: максимум в 7-9 часов; минимум в 3 часа утра.
Слайд 27
КАТЕХОЛАМИНЫ.
Адреналин
усиливает сердечные сокращения;
ускоряет пульс;
повышает АД, в основном
за счет систолического;
способствует повышению пульсового давления;
расслабляет гладкую мускулатуру бронхов,
кишечника;расширяет сосуды мышц и сердца и суживает сосуды слизистых оболочек и органов брюшной полости;
способствует сокращению мышц матки и селезенки;
участвует в пигментном обмене;
повышает чувствительность ЩЗ к действию ТТГ;
стимулирует продукцию АКТГ;
усиливает распад гликогена в печени, активирует липолиз
Слайд 28
КАТЕХОЛАМИНЫ.
Норадреналин
не оказывает влияния на углеводный обмен и
гладкую мускулатуру;
повышает АД, в основном, за счет диастолического,
что обусловлено, главным образом, его способностью сужать артериолы мышц.Влияние катехоламинов на клеточном уровне опосредуется через адренергические рецепторы (α1-, α2- и β1-, β2-рецепторы).
Высвобождение катехоламинов как из мозгового вещества надпочечников, так и из окончаний симпатической нервной системы происходит под влиянием таких физиологических стимуляторов, как стресс, физическая и психическая нагрузка, повышение уровня инсулина в крови, гипотония.
Высвобождение катехоламинов происходит при участии ионов кальция.
РЕГУЛЯЦИЯ СЕКРЕЦИИ КАТЕХОЛАМИНОВ
Слайд 30
ХРОНИЧЕСКАЯ НЕДОСТАТОЧНОСТЬ КОРЫ НАДПОЧЕЧНИКОВ
(Аддисонова болезнь, гипокортицизм, бронзовая болезнь)
Аддисонова
болезнь – тяжелое хронически протекающее заболевание, обусловленное частичным или
полным выпадением гормональной функции коры обоих надпочечников вследствие ее двустороннего поражения.Развивается в возрасте 20-40 лет.
Впервые описана Томасом Аддисоном в 1855 г.
Слайд 31
Этиология
туберкулез;
идиопатическая атрофия коры надпочечников (антигены к митохондриям и
микросомальной фракции);
кровоизлияния в надпочечники;
амилоидоз;
сифилис.
Слайд 32
Патогенез
Дефицит глюкокортикоидов приводит к адинамии, сердечно-сосудистым и желудочно-кишечным
растройствам:
падает уровень сахара в крови;
развиваются эозинофилия, лейкоцитоз и нейтропения;
гипонатриемия,
гипохлоремия, гиперкалиемия, что приводит к дегидратации и гипотонии;понижение продукции половых гормонов приводит у мужчин к импотенции, у женщин – к нарушению менструального цикла;
бронзовый цвет кожи обусловлен отложением пигмента меланина в сосочковом слое дермы и слизистых оболочек.
Слайд 34
КЛАССИФИКАЦИЯ
По клиническому течению:
типичная форма;
атипичная форма (гипоальдостеронизм, беспигментная форма
и др).
По степени тяжести:
легкая (клинический эффект достигается диетой);
средняя (диета
+ заместительная гормональная терапия: кортизон, гидрокортизон, преднизолон);тяжелая - склонность к развитию аддисонического криза (заместительная терапия: глюкокортикоиды + минералокортикоиды + диета).
Слайд 36
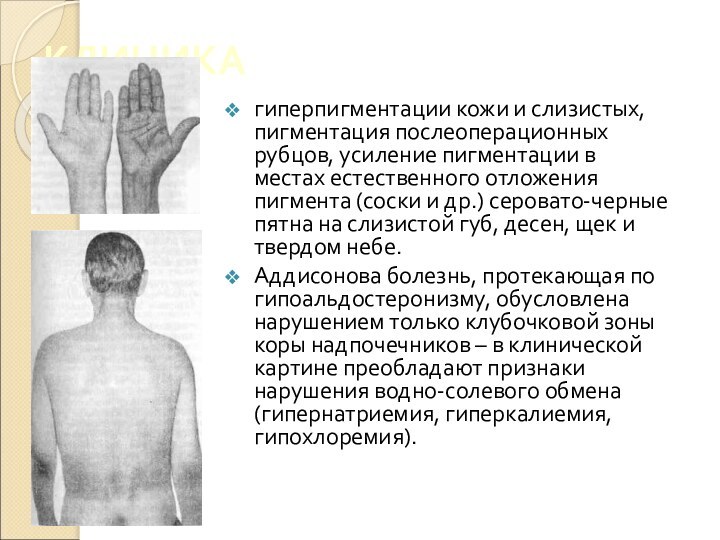
КЛИНИКА
гиперпигментации кожи и слизистых, пигментация послеоперационных рубцов, усиление
пигментации в местах естественного отложения пигмента (соски и др.)
серовато-черные пятна на слизистой губ, десен, щек и твердом небе.Аддисонова болезнь, протекающая по гипоальдостеронизму, обусловлена нарушением только клубочковой зоны коры надпочечников – в клинической картине преобладают признаки нарушения водно-солевого обмена (гипернатриемия, гиперкалиемия, гипохлоремия).
Слайд 37
ЛАБОРАТОРНАЯ ДИАГНОСТИКА
В анализе крови: лимфоцитоз, эозинофилия, СОЭ снижена,
при наличии активного туберкулеза – повышена;
Электролиты: гипонатриемия, гипохлоремия, гиперкалиемия;
Содержание
АКТГ – повышено;Содержание кортизола – снижено;
Концентрация глюкозы в крови – снижена;
тест толерантности к глюкозе – плоский с выраженной гипогликемической фазой к 3-му часу;
концентрация 17-ОКС в моче снижена;
выделение калия с мочой снижено, натрия и хлора - повышено
Слайд 38
ДИАГНОСТИЧЕСКИЕ ПРОБЫ:
Проба с АКТГ (синактеном): в/в вводят капельно
25 ЕД АКТГ в изотоническом растворе NaCl в течении
8 часов или 0,25 мг синактена (синтет. аналог АКТГ). Уровент 17-ОКС в крови определяют до и через 30 и 60 мин после введения препарата.У здоровых и у больных гипопитуитаризмом после введения АКТГ али синактена содержание 17-ОКС в крови и моче повышается, а у больных с хронической недостаточностью надпочечников остается сниженным.
Слайд 39
ДИАГНОСТИЧЕСКИЕ ПРОБЫ (продолжение)
Водная проба Робинсона-Пауэра-Кеплера основана на задержании
воды у больных аддисоновой болезнью при усиленном выведении хлоридов
и относительной задержке мочевины.Пробу начинают в 18 ч., когда больному запрещают есть и пить. С 22 ч. после опорожнения мочевого пузыря собирают мочу до 8ч следующего утра. Измеряют объем, после чего больному дают выпить в течении 45 мин определенное количество воды из расчета 20 мл на 1 кг массы тела. Затем ежечасно в течение 4 ч. определяют объем выделенной мочи.
У здоровых людей наибольший объем часовой порции мочи больше объема ночной мочи. У лиц с адиссоновой болезнью соотношение обратное. У больных индекс водной пробы < 25, а у здоровых – более 30.
Слайд 40
ДИАГНОСТИЧЕСКИЕ ПРОБЫ (продолжение)
Для дифференциальной диагностики первичной и вторичной
недостаточности надпочечников определяют потенциальные возможности или резервы коры надпочечников
(проба Лабхарта и уровень АКТГ в крови)Содержание АКТГ в плазме крови при первичной недостаточности – повышено. при вторичной – понижено.
Проба Лабхарта – в течении 2-х дней в/м вводят 40 ЕД АКТГ с пролонгированным 24-часовым действием или однократно 1 мг синактена-депо. В первый день проведения пробы 17-ОКС в крови определяют в 16ч, на 2-ой день – в 8ч. Одновременно определяют 17-ОКС и в суточной моче.
У здоровых людей – выделение с мочой 17-ОКС в первые сутки увеличивается на 100% по сравнению с исходными наличными резервами, а в последующие вторые и третьи сутки достигает 300% (потенциальные резервы).
При первичной недостаточности коры надпочечников – наличные и потенциальные резервы снижены или отсутствуют, а при вторичных – наличные резервы снижены, резервы потенциальные могут быть снижены.
Слайд 41
ЛЕЧЕНИЕ
легкая форма (диета бедная солями калия и повышенном
содержании до 10 г NaCl, аскорбиновой кислоты 0,5-1,0г.
средняя и
тяжелая форма – заместительная гормональная терапия глюко- и минералокортикоидами.кортизон, гидрокортизон по 12,5 – 50 мг;
преднизолон, преднизон 5-20 мг;
дексаметазон 1 – 2 мг;
ДОКСА (дезоксикортикостерона-ацетат) в/м в виде 0,5% масляного раствора по 5 мг ежедневно, через день или 2 раза в неделю (!контроль АД);
дезоксикортикостерона триметилацетат назначают в/м в виде водной 2,5% суспензии по 1 мл 1 раз в 2-3 недели.
Примечание: критерий оптимальной дозы глюкокортикоидов – появление сахара в моче,
критерий кратности введения ДОКСА – снижение АД.
стрептомицин 0,5-1 г, рифампицин 150-300 мг, тубазид, фтивазид, ПАСК или другие противотуберкулезные препараты.
Слайд 42
ОСТРАЯ НЕДОСТАТОЧНОСТЬ КОРЫ НАДПОЧЕЧНИКОВ
(Аддисонический криз)
Этиология:
инфекция, стресс, травма,
операция, ишемия или кровоизлияния в надпочечники, отмена глюкортикоидов (при
заместительной терапии), гипопитуитаризм.Патогенез:
снижение продукции гормонов корой надпочечников приводит к декомпенсации обмена веществ и процессов адаптации.
Слайд 43
ОСТРАЯ НЕДОСТАТОЧНОСТЬ КОРЫ НАДПОЧЕЧНИКОВ
Клиника:
снижение АД (коллапс или шок);
пульс
слабый, тоны сердца глухие, акроцианоз;
тошнота, рвота, понос, боль в
животе («острый живот»), обезвоживание;заторможенность, судороги, менингеальные симптомы, галлюцинации, кома.
Клинические варианты:
сердечно-сосудистая недостаточность;
желудочно-кишечный (абдоминальный);
нервно-психический (церебральный).
Слайд 44
ОСТРАЯ НЕДОСТАТОЧНОСТЬ КОРЫ НАДПОЧЕЧНИКОВ
Лабораторная диагностика:
в крови: снижение уровня
кортизола, альдостерона, глюкозы, натрия (>130 ммоль/л), хлора (>90 ммоль/л),
повышение уровня калия (<5ммоль/л), лейкоцитоз, лимфоцитоз, эозинофилия, эритремия.в моче: ацетон, белок, цилиндры, олигоурия, снижение выделение 17-КС, 17-ОКС. Проба с кортикотропином (синактеном) – отрицательная.
Дифференциальная диагностика:
аддисонический криз;
инфаркт миокарда, сосудистый коллапс, шок;
пищевая токсикоинфекция,
гипогликемическая кома;
гипопитуитарная кома.
Слайд 45
ОСТРАЯ НЕДОСТАТОЧНОСТЬ КОРЫ НАДПОЧЕЧНИКОВ
Лечение:
глюкокортикоиды: преднизолон 150-200мг или гидрокортизон
150-200 мг в/в струйно, затем капельно до 1000 мг
в сутки;минеракортикоиды: ДОКСА 5-10 мг (1-2 мл) в/м через 6 часов;
регидратация: изотонический раствор натрия хлорида, 5% раствор глюкозы – 2-3 л.
аскорбиновая кислота 5% раствор до 50 мл, кокарбоксилаза 200-300 мг;
при коллапсе: норадреналин – 1мл (на 500 мл изотонического раствора натрия хлорида), дофамин – 5 мл 4% расвора или 1 мл 1% раствора мезатона;
симптоматическая терапия: антибиотики, сердечные гликозиды.