Слайд 3
I Прибайкальская межрегиональная
научно-практическая конференция (2006 год)
Слайд 4
Кроветворение
Кроветворение (синоним гематопоэз) — процесс, заключающийся в серии клеточных
дифференцировок, в результате которых образуются зрелые клетки крови
Кроветворная
ткань – одна из интенсивно пролиферирующих тканей организма.
Для клеточного деления клеток крови необходима сумма сигналов.
Слайд 6
Биология сигнальных систем клетки
Кроветворные клетки имеют рецепторы к
экзогенным сигнальным молекулам: факторам роста, цитокинам, гормонам(стероидным и пептидным)
В
ответ на специфический сигнал клетка запускает каскадный механизм, реализующий интегративный путь биохимического ответа
Способы передачи сигналов одинаковы для многих типов клеток клеток
Специфичность клеточного ответа определяется типом экспрессируемого рецептора
Слайд 7
Киназы и фосфатазы
Фосфорилирование и дефосфорилирование - основные
механизмы внутриклеточной передачи сигнала
В этих профессах участвуют два типа
ферментов: киназы и фосфатазы
Фосфорилирование вызывает:
волновую активацию белков
создает в молекулах белков стыковочные участки и формирует временные внутриклеточные передатчики
Слайд 8
Рецепторы факторов роста
Рецепторы факторов роста обычно стимулируют клеточный
рост, однако при определенных условиях они могут подавлять клеточный
рост или регулировать основные функции клеток.
Большинство рецепторов факторов роста являются рецепторными тирозинкиназами (receptor protein-tyrosin kinases)
Pецепторные тирозинкиназы являются рецепторами клеточной мембраны, активирующими тримерные G-белки, которые затем активируют эффекторные молекулы (аденилатциклазу, фосфолипазу С, протеинкиназу С и др.)
Слайд 9
Вторичные мессенджеры
Циклический аденозинмонофосфат ( cAMP)
протеинкиназа А
Циклический
аденозинмонофосфат (cGMP)
Диацилглицерол ( DA) связывается с протеинкиназой С
Инозитолтрифосфат (IP3)
связывается с белками кальциевых каналов
Кальций (Ca) – обратная регуляция кальмодулином
Ca2+ response in stably transfected (VR1 receptor) NIH 3T3 cells after stimulation with an agonist
Слайд 10
Способы доставки сигнальных молекул к клеткам
Эндокринный механизм
Паракринный механизм
– клетка секретирует сигнальные молекулы и активирует соседние клетки.
Гигнальные молекулы не поступают в кровоток.
Аутокринный механизм – клетка отвечает на свой собственный сигнал
Юкстакринный механизм (прикреплениек клеток крови друг к другу или к эндотелию при гемостазе или воспалении, сигнал передается через межклеточные адгезионные молекулы)
Слайд 11
Рецепторы клеток
Группа 1 Семейство липофильных рецепторов:
Стероиды: ГК, МК,
половые стероиды
Тиреоидные гормоны, тироксин
Ретиноиды, молекулы структурно сходные с
витамином А и Д
Группа 2 Семейство гидрофильных рецепторов
Рецепторы, сопряженные с G-белками
Рецепторы как ионные каналы. Pro BNP –мозговой натрийуретический пептид – выход Na
Рецепторы, имеющие киназные домены
Рецепторы с фосфатазной активностью
Рецепторы цитокинов имеют сигналпередающие субьединицы.
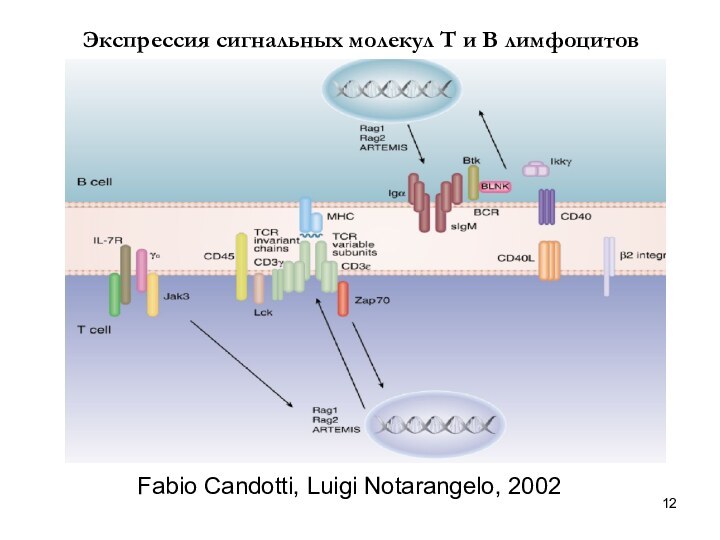
Слайд 12
Fabio Candotti, Luigi Notarangelo, 2002
Экспрессия сигнальных молекул Т
и В лимфоцитов
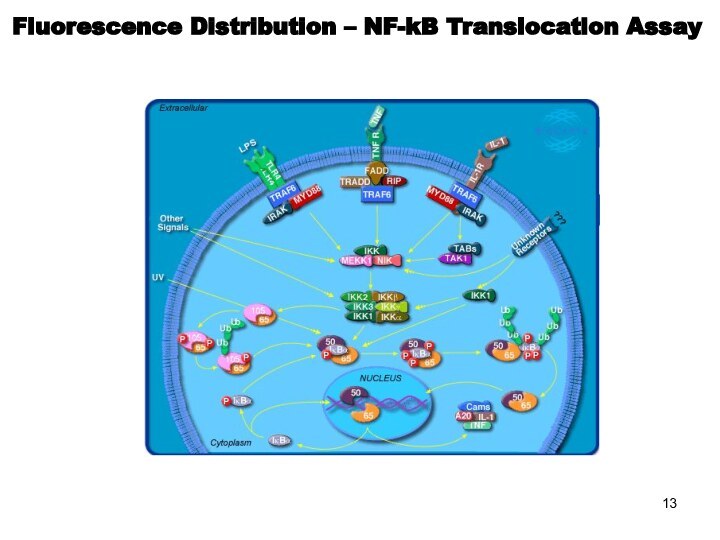
Слайд 13
Fluorescence Distribution – NF-kB Translocation Assay
Слайд 14
Связывание с bcr/abl-тирозинкиназой: сравнение иматиниба и нилотиниба
Слайд 15
Внутриклеточные сигнальные пути
Кроме активации ras-пути , в клетках
существуют еще по крайней мере два пути, активируюшиеся рецепторами
факторов роста .
Один из них - фосфатидилинозитольный путь, приводящий к активации протеинкиназы С
Другой - фосфатидилинозитол-3-киназный путь (PI3K) - использует сходные молекулы в качестве вторичных мессенджеров, однако является самостоятельным путем, клеточная функция которого еще не вполне ясна
Слайд 16
Свойства факторов роста
Факторами роста называют группу белковых молекул,
индуцирующих синтез ДНК в клетке ( Goustin A.S. ea,1986
).
Позднее было обнаружено, что спектр воздействий на клетки этих компонентов гораздо шире, чем предполагалось вначале. Так, некоторые белки этой группы в зависимости от типа клеток- респондентов могут индуцировать дифференцировку и подавлять пролиферацию .
Кроме того, к ним относят регуляторные полипептиды, модулирующие подвижность клеток , хемокины, но не обязательно влияющие на деление клеток ( Stoker M. and Gherardi E., 1987 ).
Главное отличие факторов роста от белковых гормонов - аутокринный механизм действия или паракринный механизм действия ( холокринный механизм действия для гормонов ; Deuel T.F., 1987 ).
Ростовые факторы предотвращают апоптоз клеток крови
Ц И К Л
Основные термины:
Интерфаза
Митотический цикл,
Фаза G
1
Фаза G 0
Фаза S
Фаза G 2
фактор, стимулирующий созревание
Циклины
Опухолевый супрессор
Белок p 53
Ретинобластома
Апоптоз
Хроматин
Слайд 18
Трубочки, колечки и висюльки
Первым, как отмечают историки, клетку увидел
Роберт Гук в 1663 году. Но его приспособление из пары линз давало 30−кратное
увеличение, поэтому он мог видеть в изучаемых срезах пробки лишь нечто похожее на соты, которые он назвал клетками.
Прибор Левенгука увеличивал уже в 300 раз — и голландец видел клетки крови, сперматозоиды и бактерии, названные им маленькими зверьками. Он вполне мог первым наблюдать и за тем, как делится клетка. В первой половине XIX века М. Шлейден и Т. Шванн, обобщив накопленные к тому времени знания, создали клеточную теорию, гласившую, что клетки — это структурная и функциональная основа всех живых организмов.
Слайд 19
Митотический цикл
Митотический цикл - совокупность последовательных и взаимосвязанных
процессов в период подготовки клетки к делению, а также
на протяжении самого деления.
Митоз греч "митос" - нить
Слайд 20
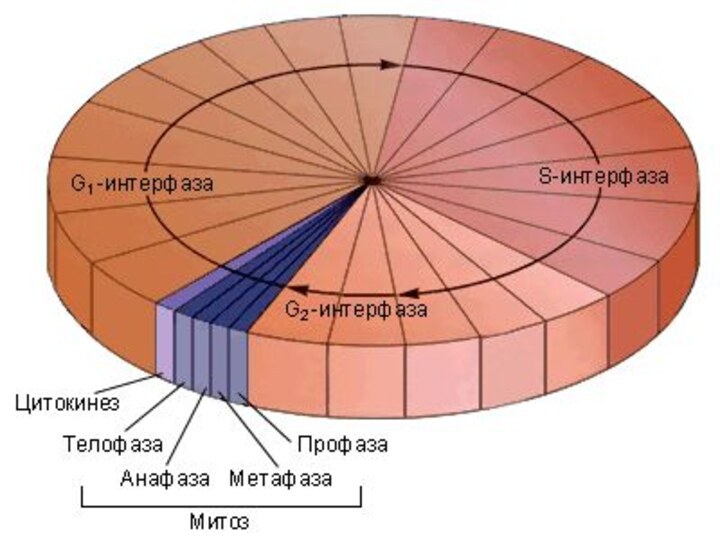
Жизненный цикл клетки
Профаза
Метафаза
Анафаза
Телофаза
Деление клетки
Интерфаза
Слайд 22
Митотический цикл
Митотический цикл = фаза М –
это цикл деления, который длится обычно 30-60 минут и
завершается делением клетки на две дочерние.
Слайд 24
G 0
Наступает за фазой G1
Клетка экспрессирует белки, которые
используются не для клеточного деления
Гены, кодирующие запуск клеточного деления
«выключены»
Гены, кодирующие белки, необходимые для клеточной дифференцировки «включены»
Кардиомиоциты, нейроны постоянно находятся в фазе G 0 и цикл деления в них не возобновляется (все гены деления «выключены» навсегда)
Исключением являются клетки крови и кишечного эпителия, где скорость клеточного деления высока
Размножение при помощи митоза называют бесполым или вегетативным, а также клонированием. При митозе генетический материал родительских и дочерних клеток идентичен.
Слайд 25
Когда нормальные клетки прекращают делиться?
Гены, включающие пролиферацию выключаются,
если клетка получает сигнал, что все точки «контактов» заняты.
Таким образом молекулы окружающей среды-межклеточное вещество-межклеточные контакты, участвуют в управлении клеточной пролиферацией (интегрины, кадгерины, катенины)
Слайд 26
Интегрины
Интегрины-поверхностные рецепторы клетки, переносящие сигналы от внеклеточного матрикса
к цитоскелету.
«включают» рост, метастазирование, опухолевых клеток, апоптоз, свертывание крови
и миграцию клеток в зоны воспаления
Нековалентно связанные гетеродимеры из α (16 разновидностей) и β (8 разновидностей ) субьединиц
Интегрины, формирующие межклеточные контакты, называются ICAM – межклеточными молекулами адгезии
Интегрины способсвуют связыванию клеток с внеклеточным матриксом: фибронектином, коллагеном, ламинином.
Слайд 27
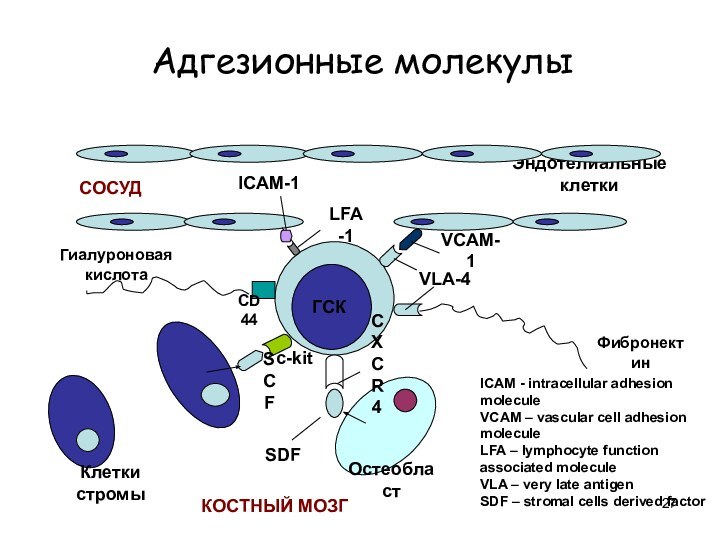
Адгезионные молекулы
c-kit
Клетки стромы
Эндотелиальные клетки
ГСК
Гиалуроновая кислота
CD44
Фибронектин
VLA-4
VCAM-1
LFA-1
ICAM-1
ICAM - intracellular adhesion
molecule
VCAM – vascular cell adhesion
molecule
LFA – lymphocyte function
associated
molecule
VLA – very late antigen
SDF – stromal cells derived factor
CXCR4
SDF
СОСУД
КОСТНЫЙ МОЗГ
SCF
Остеобласт
Слайд 28
Хоминг
Костный мозг
Сосуд
Остеобласты
SDF
Остеоциты
Стромальные
клетки
Эндотелиальные
клетки
ГСК
CXCR4
Главные агенты:
SDF-1/CXCR4
VLA-4/VCAM-1
CD44/Гиал.к-та
Слайд 29
Figure 1. G-CSF HSC mobilization. a: There are

adhesive interactions between HSC and matrix components in the
BM. HSC express a wide range of cell adhesion molecules (CAM) including CXCR4, VLA-4, c-kit, CD62L, and CD44. The BM stroma expresses cognate ligands for these CAMs such as SDF-1, VCAM-1, KL, PSGL, and HA. b: HSC mobilization results from cytokine-induced functional changes in the adhesion profile expressed by the HSC in their relation to the BM stromal cells, osteoblasts, and other matrix components. G-CSF induces, through an unknown cell, the release of a number of proteases into the BM, including NE, CG, and MMP9. IL-8 and Groâ release the same enzymes via neutrophils and monocytes. These proteases cleave several adhesion molecules thought to play an important role in HSC trafficking and mobilization, including c-kit, VCAM-1, CXCR4, and SDF-1. Recent data suggest that G-CSF treatment potently inhibits osteoblast SDF-1 expression at the mRNA level furthermore osteoblasts are the major source of SDF-1 in the BM. The resultant decrease in osteoblast SDF-1 may also contribute to enhanced HSC mobilization especially in response to G-CSF. Cathepsin G (CG), chemokine receptor-4 (CXCR4), hematopoieic stem cell (HSC), hyaluronic acid (HA), interleukin 8 (IL-8), kit ligand (KL), matrix metalloproteinase-9 (MMP-9), neutrophil elastase (NE), stromal cellderived factor-1 (SDF-1), vascular cell adhesion molecule-1 (VCAM-1), very late antigen-4 (VLA-4), P-selectin glycoprotein ligand-1 (PSGL).
B. Nervi et al. Journal of Cellular Biochemistry 99:690–705 (2006)
Слайд 31
ОСНОВНЫЕ ПОВЕРХНОСТНЫЕ МАРКЕРЫ ЭК
CD 62 E (E-селектин)
CD 62 P (Р-селектин)
CD 106 (VCAM-1)
CD
31 (PECAM-1)
VEGFR-2 (KDR)
СD 105 (endoglin)
CD 144 (VE-cadherin)
CD 146 (S-endo-1)
СD 54 (ICAM-1)
CD 34
CD54+/CD45-
CD146+/CD45-
CD34+/CD45-
проточная цитометрия
Слайд 32
Роль циклинов
Деление клетки запускается MPF
В клетках млекопитающих
существует семейство циклинзависимых киназ (cyclin-dependent kinases –Cdk). Cdk пронумерованы
с 1 по 5.
В период выхода клетки из фазы G0 под действием факторов роста первым образуется комплекс циклин Д- Cdk. Этот комплекс запускает синтез белков, необходимых для репликации ДНК.
Циклинов четыре: А, В, Е, Д.
Слайд 33
Циклин В
Циклин В – контролирует вхождение клеток в
митоз.
Состоит из 2 субьединиц:
- киназного домена (
способен к фосфорилированию специфических веществ в клетке) и
- регуляторной субьединицы (циклиновой), синтез которой усиливается и ослабевает в течение клеточного цикла.
Разрушение циклина Д происходит не за счет протеолиза, как у большинства белков, а за счет присоединения к N-концевому пептиду, который называется «блок разрушения» как минимум двух белков (распознающий и убиквитинлигазы) после чего его разрушение происходит в протеасоме.
Для вступления клетки в митоз необходим еще один сигнал – это MPF – регулятор митотических процессов. Разрушение MPF циклином Д вызывает выход из митоза.
MPF участвует в начальных этапах деления клетки: компактизации хромосом, разрушении эндоплазматического ретикулума и комплекса Гольджи.
Слайд 34
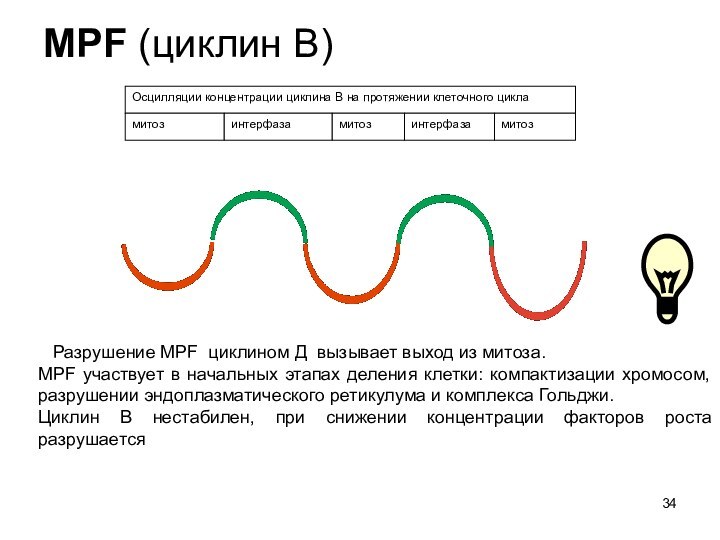
MPF (циклин В)
Разрушение MPF циклином Д
вызывает выход из митоза.
MPF участвует в начальных этапах деления
клетки: компактизации хромосом, разрушении эндоплазматического ретикулума и комплекса Гольджи.
Циклин В нестабилен, при снижении концентрации факторов роста разрушается
Сопровождается:
Компактизацией, конденсацией хромосом, в
10 000
раз в нуклеосомы в середине G2 фазы
Растворением ядерной оболочки (ламин А и В)
Формированием веретена деления и выравниванием хромосом в плоскости экватора клетки (с помощью центриолей, астральных и полярных микротрубочки, кинетохора)
Расхождением сестринских хроматид к полюсам клетки (динеин, кинезин), образуются борозды деления, клетка окончательно делится на две дочерние (актин, миозин).
Слайд 36
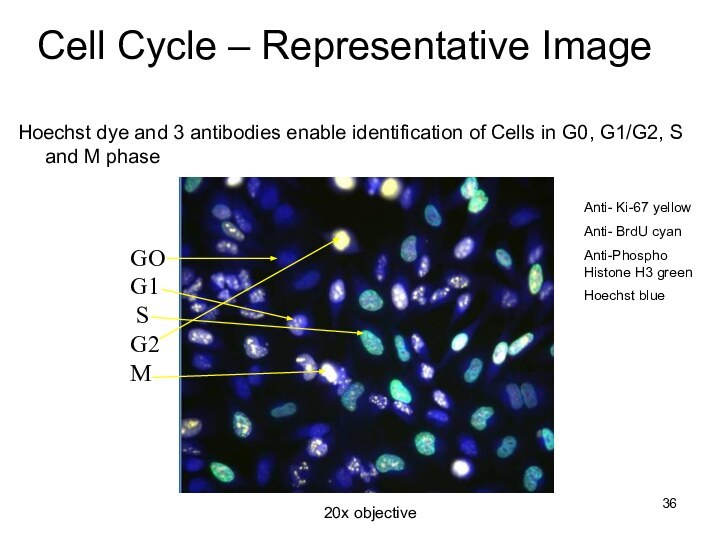
Cell Cycle – Representative Image
Hoechst dye and 3
antibodies enable identification of Cells in G0, G1/G2, S
and M phase
GO
G1
S
G2
M
20x objective
Anti- Ki-67 yellow
Anti- BrdU cyan
Anti-Phospho Histone H3 green
Hoechst blue
Слайд 37
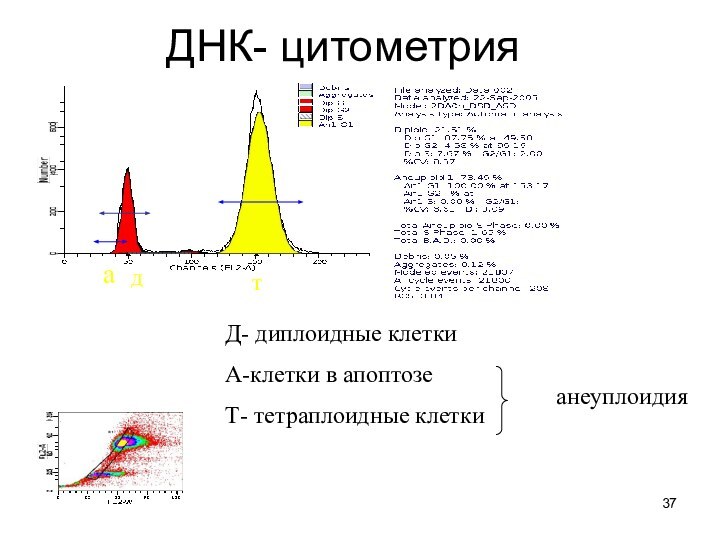
ДНК- цитометрия
а
д
т
Д- диплоидные клетки
А-клетки в апоптозе
Т- тетраплоидные клетки
анеуплоидия
Слайд 38
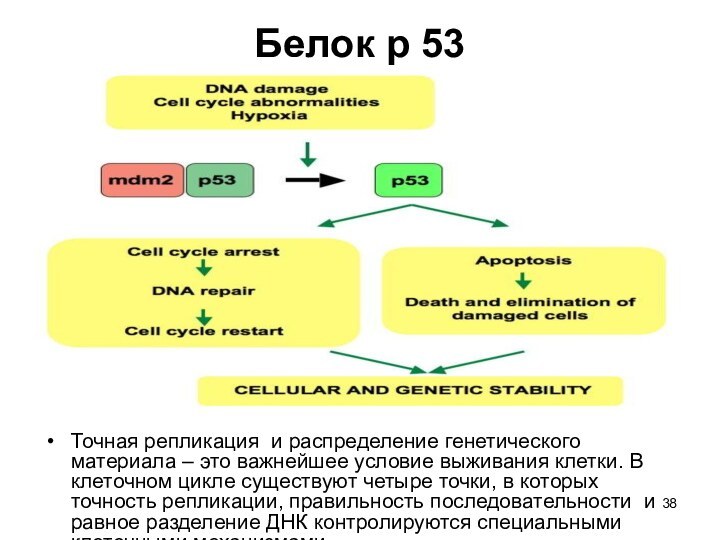
Белок р 53
Точная репликация и распределение генетического
материала – это важнейшее условие выживания клетки. В клеточном
цикле существуют четыре точки, в которых точность репликации, правильность последовательности и равное разделение ДНК контролируются специальными клеточными механизмами.
Слайд 39
Делеция 17p перед началом терапии
Прогрессия на фоне лечения
или рецидив в течение 12 месяцев от начала терапии
Определение
группы высокого риска при В-ХЛЛ
Слайд 40
N
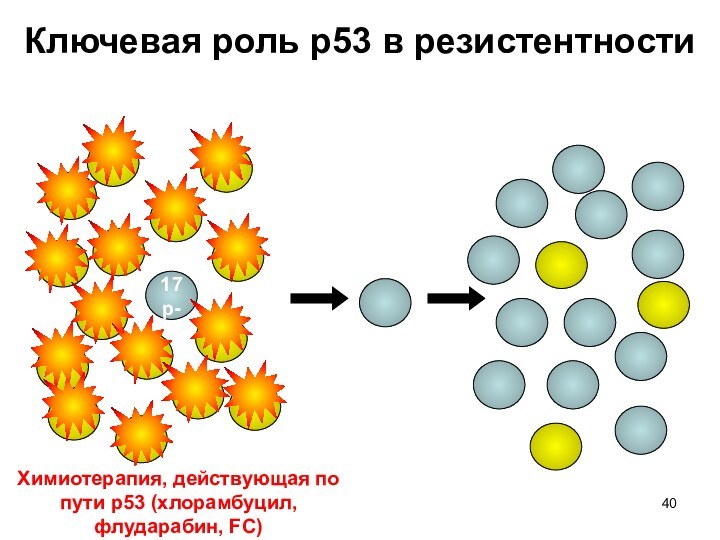
Ключевая роль p53 в резистентности
17p-
До лечения
Слайд 41
Делеция 17p
Прогрессия на фоне лечения или рецидив в
течение 12 месяцев от начала терапии
Преимущественное поражение костного мозга
– монотерапия
Большие размеры лимфоузлов – в комбинации с FC с CHOP
Гиперлейкоцитозные формы с цитопенией
Показания к кэмпас в первой линии
В-ХЛЛ
Слайд 42
Протоонкогены – гены, чьи продукты участвуют в регуляции
клеточной пролиферации.
Мутации этих генов приводят к неконтролируемой пролиферации и
протоонкоген может стать онкогеном (хромосомные транслокации, точечные мутации, амплификация)
Слайд 43
ЛКМЗ
В-клеточная опухоль, характеризующаяся транслокацией или амплификацией локуса

11q13, приводящими к гиперэкспрессии ядерного белка циклина D1
Циклин
D1, в комплексе с циклинзависимыми киназами 4 и 6 (ЦЗК4/6) является регулятором перехода клеток из G1 в S-фазу клеточного цикла.
В группу циклинов D1 входят 3 белка: D1 D2 D3, в лимфоцитах в норме эксперессируется D3. (D1 эксапрессируется только в эпителиальных и мезенхимальных клетках. )
В кариотипе опухолевых клеток выявляется патогенетическая транслокация t(11;14)(q13;q32), приводящая к гиперэкспресии ядерного белка циклина D1 и нарушению обратной регуляции клеточного цикла.
В клетке существует два класса ингибиторов комплекса циклин D1:
- семейство Cip/Kip представлено белками р21, р27 и р57
- семейство INK4 представлено белками р15 и р16, р18 и р19.
Эти гены избирательно блокируют циклин D-зависимые киназы. Вторичные цитогенетические нарушения при прогрессии лимфомы из клеток мантийной зоны связаны с делециями именно этих генов.
Циклин D1
Слайд 44
1-2 – толстые ригидные складки;
3-5 – лимфатические
фолликулы подслизистого слоя; 6-8 – лимфоматозный полипоз; 9-12 –
опухоли.
Слайд 45
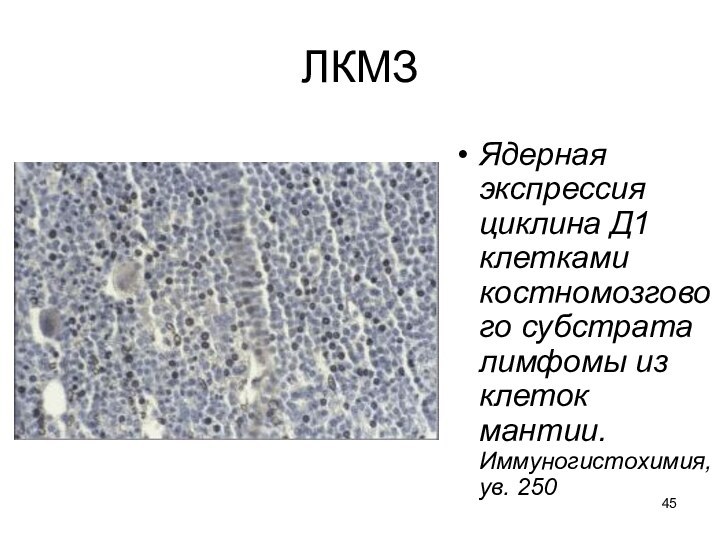
ЛКМЗ
Ядерная экспрессия циклина Д1 клетками костномозгового субстрата лимфомы
из клеток мантии. Иммуногистохимия, ув. 250
Слайд 46
Регуляция клеточного цикла в тканях
При разработке метода выращивания
клеток в культуре, было отмечено, что клетки растут лучше,
если находятся внутри кровяных сгустков. Это вещество – тромбоцитарный фактор роста – PDGF
Факторы роста с широким диапазоном клеточной и тканевой специфичности: PDGF, EGF, FGF, NGF, EPO, IL-2,IL-3
Слайд 47
Факторы роста
Факторы роста
Семейство тромбоцитарных факторов роста (PDGF) :
PDGF A, PDGF B, VEGF, PLGF,CSF-1 SCF-стабильный фактор;
Семейство факторов
роста фибробластов (FGF) : α FGF, βFGF, int-2, K-FGF, FGF-5, GFG-6, KGF,FGF-8, FGF-9;
Cемейство инсулинов: инсулин, инсулиноподобный фактор роста IGF-1, инсулиноподобный фактор роста IGF-2;
Семейство эпидермальных факторов роста (EGF)
Фактор роста опухолей α
Семейство факторов роста нервов NGF NGF, BDNF, NT-3,4,5,
Семейство факторов роста гепатоцитов HGF
Колониестимулирующие факторы CSF
Гранулоцит-колониестимулирующий фактор G-CSF,
Моноцит-колониестимулирующий фактор M-CSF,
Гранулоцит-моноцит-колониестимулирующий фактор GM-CSF
Трансформирующие фактор роста
TGFβ
BMP
Слайд 48
Старение - феномен Хейфлика.
Клетки запрограммированы на определенное число
делений, а затем прекращают делиться
Репликативное старение
– сокращение
длины теломер
– повышение экспрессии р21, ингибитора циклинзависимых киназ
Существуют серьезные доказательства, что окислительное воздействие и ограничение калорий являются ключевыми факторами в процессе старения
Слайд 49
Теломеры
Теломеры-это концевые участки хромосом, которые содержат повторяющиеся последовательности
ДНК и укорачиваются с каждой репликацией.
В самообновляющихся и
активно делящихся популяциях клеток (например, стволовых) действует фермент теломераза, способный наращивать теломерные последовательности.
От степени сохранности теломер зависит пролиферативный потенциал клетки; в опухолевых клетках длины теломер обычно поддерживается на постоянном уровне
Слайд 50
Апоптоз – программируемая клеточная гибель.
Регуляция процессов клеточного деления
необходима для выживания организма. Размножение клеток зависит от скорости
пролиферации и смерти клеток. Скорость клеточной смерти зависит от скорости стимулирования и ингибирования клеточной смерти.
Систематическое удаление клеток путем апоптоза ( apo-полное ptosis –падение,утрата) в переводе с греческого опадание цветочных лепестков, «осенний листопад»). Этот термин впервые применен в 1972 году J.F.Kerr для описания конкретной морфологической картины одного из видов клеточной смерти.
Удаление умирающих клеток при апоптозе происходит без воспаления
Некроз-патологическая форма смерти клеток в результате их острого повреждения, разрыва оболочки, высвобождения содержимого цитоплазмы и индукции воспалительного процесса
Слайд 51
Апоптоз – программируемая клеточная гибель.
француз Бонне различал следующие
четыре типа ядерной дегенерации:
Кариорексис - хроматин распадается на
бесформенные скопления обломков и гранул, которые после разрыва ядерной оболочки попадают в цитоплазму и там дегенерируют
Кариопикноз - "хроматиновая сеть" отстает полностью или почти полностью от ядерной оболочки и слипается в гомогенную массу. Ядерная оболочка сморщивается, ядро теряет тургор, хроматин распыляется и отдельные его гранулы растворяются в цитоплазме.
Кариолизис или хроматолиз - хроматин постепенно растворяется. Ядро и цитоплазма в начале окрашиваются основными красителями весьма интенсивно, но затем хроматин теряет свои морфологические и химические особенности и ядерное вещество переходит в цитоплазму и там растворяется.
Вакуолизированная ядерная дегенерация - в ядре появляется одна или несколько вакуолей, которые постепенно увеличиваются, оттесняя хроматин к периферии ядра и здесь он образует отдельные скопления
Слайд 52
Этапы апоптоза
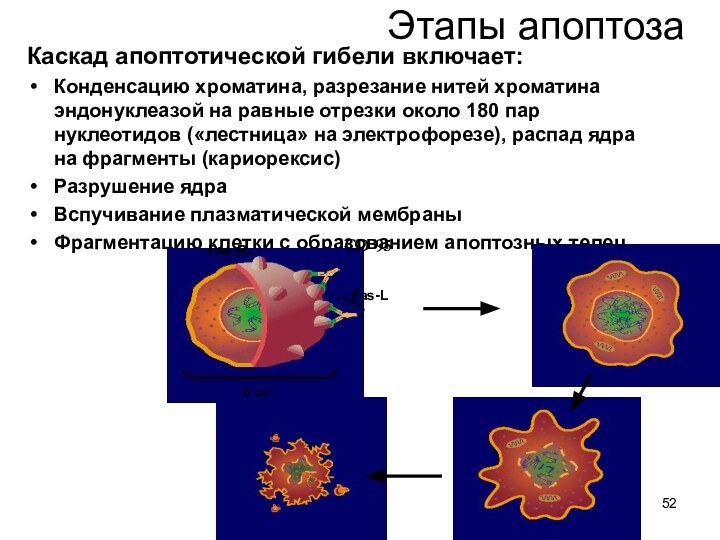
Каскад апоптотической гибели включает:
Конденсацию хроматина, разрезание нитей
хроматина эндонуклеазой на равные отрезки около 180 пар нуклеотидов
(«лестница» на электрофорезе), распад ядра на фрагменты (кариорексис)
Разрушение ядра
Вспучивание плазматической мембраны
Фрагментацию клетки с образованием апоптозных телец.
CD 95
Слайд 53
Механизмы апоптоза
2 фазы:
Формирование и проведение апоптотического сигнала –фаза
принятия решения
Демонтаж клеточных структур –эффекторная фаза. Каспазы (цистеиновые протеазы)
расщепляют белки в местах расположения аспарагиновых оснований
Слайд 54
Каспазы
Семейство протеаз, участвующих в апоптозе
Существует 14 видов каспаз
Активаторы
цитокинов (каспазы 1,4, 5, 13)
Индукторы активации эффекторных каспаз (каспазы
2,8,9,10) ICAD
Эффекторные каспазы-исполнители апоптоза (каспазы 3,6,7)
После активации казпазы 9, затем каспазы 3, белок Bax накапливается, образует гомодимеры и инициирует высвобождение цитохрома С.
Ингибирует апоптоз каспаза Bcl-2
Ускоряет апоптоз белок Bad, образующий гетеродимеры с Bcl-2
Слайд 55
Сигнальные пути апоптоза
Повреждение ДНК, радиация, токсические воздействия, глюкокортикоиды,
укорочение теломер приводит к
активации каспазы 9
Проапоптотические сигналы Fas-R, TNF-R, активация каспазы 8, Ca 2+ (зависимый от протеинкиназы C)
Инициация апоптоза происходит под действием :
двухвалентных ионов Ca 2+ (проапоптоз-мобилизация внутриклеточного депо Са) ,
недостатка Zn2+ (антиапоптоз, за счет подавления эндонуклеазы)
изменения мембран апоптотических клеток
Слайд 56
Изменения мембран апоптотических клеток
Клеточная мембрана апоптозной клетки теряет
сиаловую кислоту на гликопротеинах и гликолипидах, входящих в ее
состав
Клетка становится доступной для фагоцитоза
Макрофаги притягивают экспрессирующиеся рецепторы для витронектина
Поверхностное расположение фосфатидилсерина
Слайд 57
слияние
в результате
слияния
получаются
гибридомы
СХЕМА ПОЛУЧЕНИЯ ГИБРИДОМ
для производства моноклональных
антител
бессмертная
клеточная линия
клетки, секретирующие антитела
Слайд 58
Клинический случай 1
Б-ая В.66 лет , поступила в отделение
гематологии 21.05.2007 , ОАК:
L-8.66*10 9/л,
СОЭ 82 мм/ч
Нв 52 г/л, Эр.1.52 66*10 9/л тромбоцитопения, Бластных клеток 48%.
Печень, селезенка не увеличены, л/узлы передне-шейные, надключичные, подмышечные до 1.5-2 см плотной консистенции.
На коже рук, ног петехиально-экхимозные геморрагии
В костномозговом пунктате бластных клеток 72%,
Цитохимически: МПО в 1%, гликоген гранулярный в 63% , преимущественно одиночные крупные гранулы
Слайд 59
HLA-DR
CD 34
CD7
CD 9
Клинический случай 1
Иммунофенотип опухолевых клеток: СD34+,
HLA-DR+, СD19+, СD79а+, СD10-/+, СD9+, СD38+, Ki-67+, TDT-, СD45+.
Заключение: Данный иммунофенотип соответствует В-клеточному острому лимфобластному лейкозу, B I варианту.
CD19
CD10
CD19
Ki 67
CD 38
CD 79а
Слайд 61
Клинический случай 2
Б-й Ш.,39 лет, поступил с жалобами
на повышение температуры до 40
наблюдается в отделении гематологии с
апреля 2006 года
В миелограмме обнаруживалось до 31 % атипичных лимфоцитов
Биопсия лимфоузла 12.05.2006: фрагмент лимфоузла а паранодальной клетчаткой с наличием пролиферации крупных клеток (в 3-5 раз больше лимфоцита). Определяются крупные клетки с пузырьковидными ядрами и центрально расположенных базофильным ядрышком, клетки средних размеров с 2-3 ядрышками, клетки с ращепленными ядрами и участки с наличием зрелых лимфоидных клеток. Патологические митозы.Инфильтрация капсулы и паранодальной клетчатки. Закл.:больше данных за диффузную крупноклеточную лимфому.
Выявлен М-градиент 41,4 г/л (46%), секреция легких цепей каппа-типа
Гепатомегалия+3см.,
Внутрибрюшинные лимфоузлы увеличены до 4.5см
Проведено 8 курсов ПХТ (R-CHOP), ремиссия не достигнута.
Слайд 62
Клинический случай 2
Заключение: Данный иммунофенотип в наибольшей
степени соответствует плазмоклеточной пролиферации.
Иммунофенотип опухолевых клеток: СD138+, CD38+, СD56+,
СD13+, СD71+, Кi-67+, CD45+.
CD10
CD19
CD19
CD138
CD38
CD16.56
CD45
CD16.56
Слайд 63
Клинический случай 3
Ki 67
Ki 67
CD 79a
CD3
Слайд 64
Комбинация флудара + ритуксимаб
Функциональный
синергизм
CD55, CD46, CD59
CD 55 мешает действию ритуксимаба
Флударабин ингибирует CD55
Ритуксимаб:
вызывает апоптоз
(активация каспаз, подавление Bcl-2 и Bcl-x(L))
Активирует комплемент
Флударабин: вызывает апоптоз,
Блокирует репарацию ДНК
Снижение экспрессии CD55
Усиление апоптоза
Ритуксимаб + флударабин
1. Wierda W, et al. J Clin Oncol 2005; 98:3383–3389;
2. Chow KU, et al. Haematologica 2002; 87:33–43.
3. Byrd J, et al. Blood 2002; 99:1038–1043.
4. Alas S, et al. Clin Cancer Res 2001; 7:709–723.
5. Di Gaetano N, et al. Br J Haematol 2001; 114:800–809.
Слайд 65
Совместное российское исследование
Слайд 67
ЛИТЕРАТУРА
Кассирский И.А. и Алексеев Г.А. Клиническая гематология. М., 1970; Максимов А.А.
Основы гистологии, ч. 1—2, Л., 1925;
Руководство по гематологии,
под ред. А.И. Воробьева, М., 2002;
Чертков И.Л. и Воробьев А.И. Современная схема кроветворения, Пробл. гематол и перелив. крови, 1973, т. 18, №10, с, 3, библиогр.;
Чертков И.Л. и Фриденштейн А.Я. Клеточные основы кроветворения, М., 1977, библиогр.
Д.М. Фаллер, Д. Шилдс Молекулярная биология клетки. М., Бином-пресс, 2006, 260 с.
Е.Б.Владимирская
Биологические основы противоопухолевой терапии.-М.,2001.-110 с.