Слайд 2
Корь
Measles
Сем. Paramyxoviridae
Род Morbillivirus
Вид вирус кори
Слайд 3
Корь –острая вирусная инфекция
Отличительные черты:
высокая контагиозность,
восприимчивость разных
возрастных групп,
возможные тяжелые осложнения
продолжительная иммуносупрессия у
переболевших
Английское название болезни measles происходит от латинского слова misellus, что означает «несчастный». Иногда это заболевание называют rubeola (от латинского rubeolus - красноватый) или morbilli (от латинского morbus - болезнь).
Слайд 4
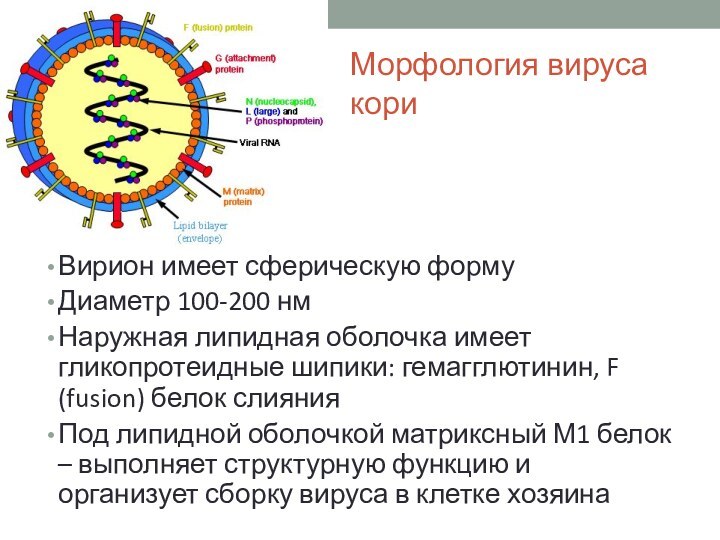
Морфология вируса кори
Вирион имеет сферическую форму
Диаметр 100-200 нм
Наружная
липидная оболочка имеет гликопротеидные шипики: гемагглютинин, F (fusion) белок
слияния
Под липидной оболочкой матриксный М1 белок – выполняет структурную функцию и организует сборку вируса в клетке хозяина
Слайд 5
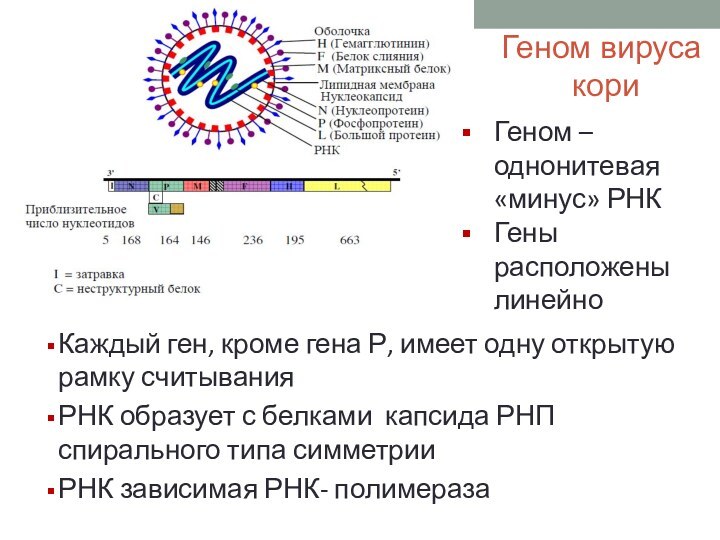
Геном вируса
кори
Каждый ген, кроме гена Р, имеет
одну открытую рамку считывания
РНК образует с белками капсида РНП
спирального типа симметрии
РНК зависимая РНК- полимераза
Геном – однонитевая «минус» РНК
Гены расположены линейно
Слайд 6
Известен 1 серотип вируса кори
Но имеются 23 генетических
варианта (генотипы)
Генетические различия не являются биологически значимыми
Вирус имеет общие
антигенные детерминанты с вирусом чумы собак и рогатого скота. У людей, переболевших корью, появляются антитела к указанным вирусам.
Основные антигены вируса кори —гемагглютинин, белок F и нуклеокапсидный белок NP. AT к гемагглютинину и F-протеину проявляют цитотоксическое действие, направленное против инфицированных клеток.
Слайд 8
Неструктурные C и V белки функционируют как факторы
вирулентности при коревой инфекции ЦНС.
С белок способен подавлять вирусную
транскрипцию и увеличивать сборку частиц
Эти белки ингибируют продукцию интерферона
Слайд 9
Свойства вируса кори
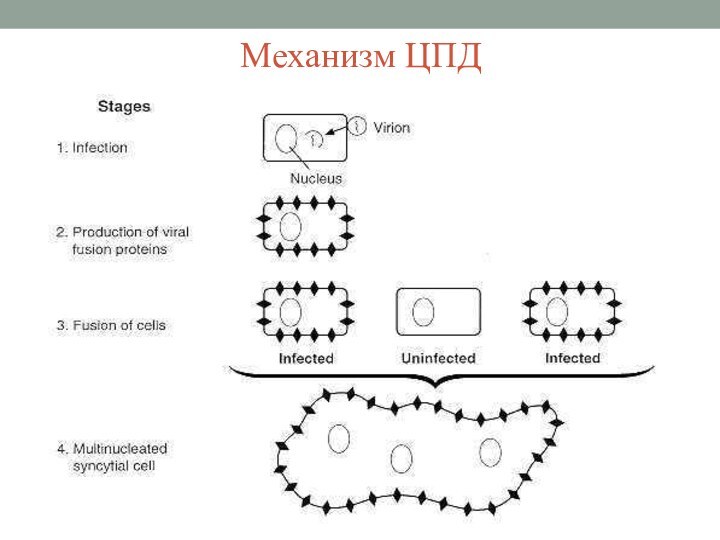
Вирус обладает гемагглютинирующей, гемолитической и симпластообразующей
активностью; агглютинирует эритроциты обезьян, но не агглютинирует эритроциты кур,
морских свинок и других видов животных.
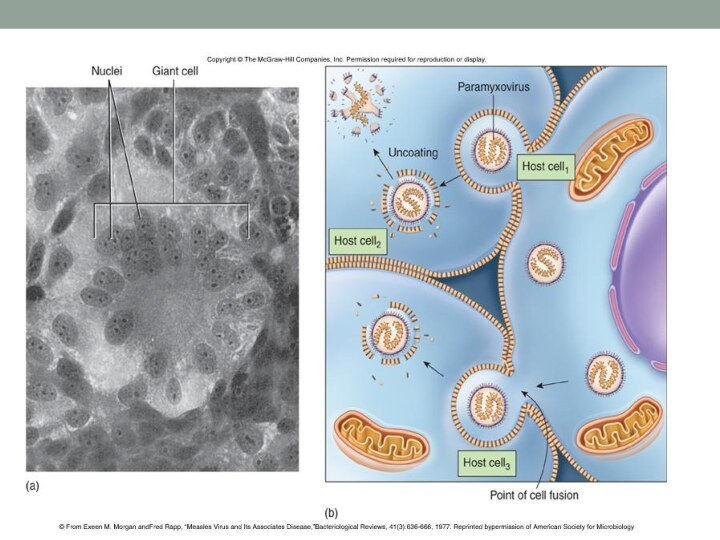
В культуре клеток почек человека и обезьян вирус проявляет цитопатическое действие (ЦПД) с образованием гигантских клеток и/или синцитиев, либо зернистых включений в цитоплазме и ядре
Слайд 11
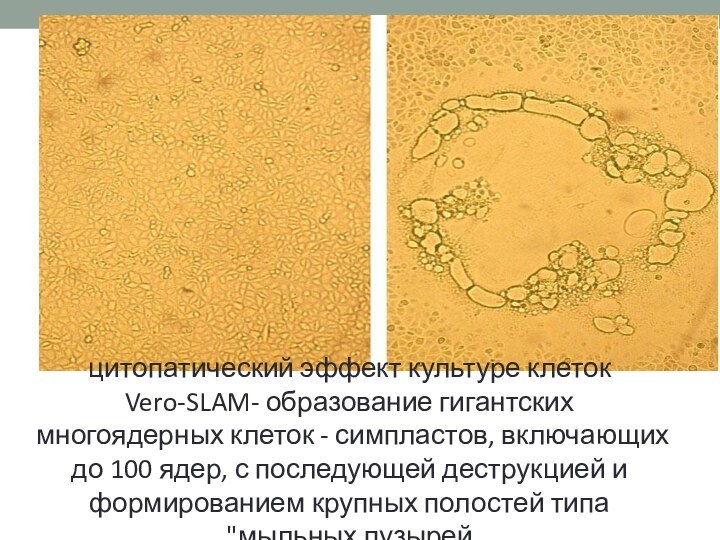
цитопатический эффект культуре клеток Vero-SLAM- образование гигантских многоядерных
клеток - симпластов, включающих до 100 ядер, с последующей
деструкцией и формированием крупных полостей типа "мыльных пузырей
Слайд 12
Свойства вируса кори
Вирус чувствителен к эфиру и
детергентам, дезинфектантам
быстро инактивируется при рН 2,0—4,0, УФ
при
температуре 56° С инактивируется в течение 30 мин.
В высохших каплях слизи при температуре 12—15° С он может сохраняться несколько дней.
Устойчив к лиофилизации
Слайд 13
Взаимодействие вируса с клеткой
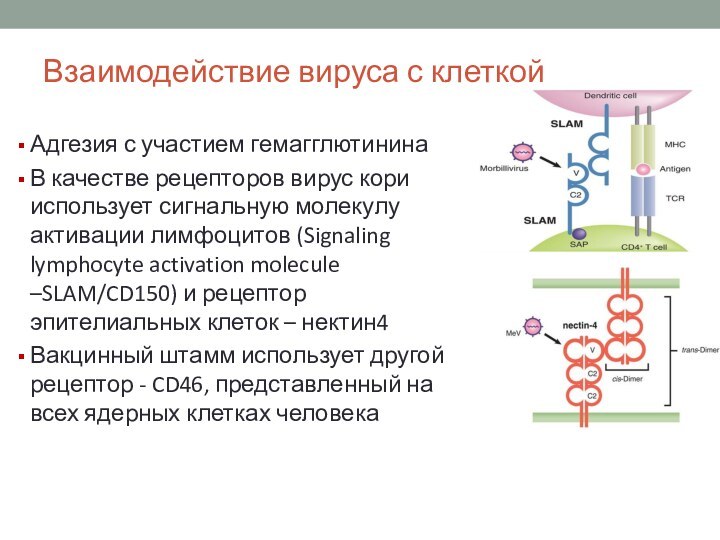
Адгезия с участием гемагглютинина
В качестве
рецепторов вирус кори использует сигнальную молекулу активации лимфоцитов (Signaling
lymphocyte activation molecule –SLAM/CD150) и рецептор эпителиальных клеток – нектин4
Вакцинный штамм использует другой рецептор - CD46, представленный на всех ядерных клетках человека
Слайд 14
Взаимодействие вируса с клеткой
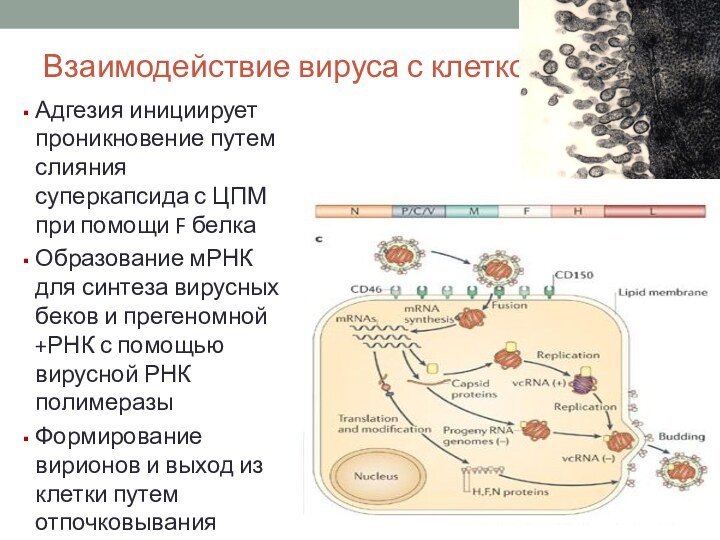
Адгезия инициирует проникновение путем слияния
суперкапсида с ЦПМ при помощи F белка
Образование мРНК для
синтеза вирусных беков и прегеномной +РНК с помощью вирусной РНК полимеразы
Формирование вирионов и выход из клетки путем отпочковывания
Слайд 15
Эпидемиология
Корь является эндемичной инфекцией.
Определяющим фактором, обусловливающим распространение
инфекции, является состояние коллективного иммунитета населения.
Вспышки кори возникают
при появлении прослойки восприимчивых детей.
Источник инфекции – больной человек, выделяющий вирус кори с последних 2-х дней инкубационного периода до 4-го дня после высыпания
Путь передачи – воздушно-капельный
В основном вспышки кори регистрируются в конце зимы и весной.
Слайд 16
Статистика по миру
Европа: По состоянию

на 20 сентября 2011 года корь зарегистрирована в 40
из 53 государств-членов. За период с января по июль 2011 года подтверждены 26 025 случаев кори. Наибольшее число случаев было зарегистрировано во Франции - за первые шесть месяцев года - 14 025 случаев кори. Также много заболевших корью зарегистрировано в Германии, Италии, Испании, Румынии, Бельгии, Швейцарии, Соединенном Королевстве, Узбекистане
Из всех случаев заболевания в Европейском регионе 11 случаев закончились смертельным исходом (6 во Франции и по одному в бывшей югославской Республике Македонии, Германии, Кыргызстане, Румынии и Соединенном Королевстве Великобритании и Северной Ирландии). Последняя вспышка кори с 12 случаями заболевания была зарегистрирована в сентябре в Израиле.
Африка: Региональное бюро сообщает, что по состоянию на сентябрь 2011 года крупные вспышки кори регистрируются в Демократической Республике Конго (103 000 случаев), Нигерии (17 428 случаев), Замбии (5 397 случаев) и Эфиопии (2 902 случая). В Демократической Республике Конго зарегистрировано более чем 1 100 летальных исходов, связанной с корью, которые произошли в стране в течение 2011 года.
Слайд 17
Америка: Последний случай эндемической кори был

зарегистрирован в регионе в 2002 году. В 2011 году
в регионе зарегистрировано несколько вспышек кори, связанных с ввозом вируса кори из других регионов. Самая крупная вспышка кори произошла в Квебеке, Канада, там было зарегистрировано 742 случая заболевания, в 89 случаях потребовалась госпитализация, но случаев смерти, связанной с корью, не было. Другие вспышки болезни зарегистрированы в Соединенных Штатах Америки (213 случаев), Эквадоре (41 случай), Бразилии (18 случаев), Колумбии (7 случаев), Мексике (3 случая) и Чили (6 случаев). Большинство из этих вспышек кори связано со случаями ввоза вируса из Европы, за исключением вспышек болезни в Соединенных Штатах Америки и Чили, связанных со случаями в Малайзии, и вспышки в Эквадоре, связанной с завозом из Кении.
Российская Федерация: за 7 месяцев 2011 года в Российской Федерации зарегистрировано 167 случаев кори в 18 субъектах страны. Еще 3 случая заболевания корью выявлены среди служащих различных ведомств. Наибольшее число случаев кори зарегистрировано в г. Москве (59случаев), Астраханской области (26 случаев), Красноярском крае (20 случаев), Томской области (14 случаев) и Ставропольском крае (17случаев).
Слайд 18
Патогенез
После заражения вирус кори внедряется в клетки респираторного
эпителия носоглотки и попадает в региональные лимфатические узлы
Первичная
репродукция в клетках эпителия и лимфоидных клетках слизистой оболочки, носоглотки, трахеи и бронхов (2-3 дня).
Первичная виремия, обеспечивающая распространение инфекции на ретикуло-эндотелиальную систему.
Дальнейшее размножение вируса приводит к вторичной виремии, которая возникает на 5-7-й день после инфицирования (конец инкубационного периода) и сохраняется 4-7 дней.
Слайд 19
Патогенез
В этот период возможно внедрение и последующее размножение
вируса в коже, конъюнктиве, дыхательных путях и других органах,
включая селезенку, тимус, легкие, печень и почки.
Виремия достигает пика на 11-14 день после инфицирования, а затем быстро снижается в течение нескольких дней.
Инфицирование респираторного тракта характеризуется нарастанием кашля и насморка, а также такими более редкими осложнениями как круп, бронхит, пневмония.
Слайд 20
Патогенез
Возбудитель обладает выраженной эпителиотропностью и поражает кожные покровы,
коньюктивы, слизистые оболочки респираторного тракта и ротовой полости (пятна
Бельского-Филатова-Коплика).
Вирус можно обнаружить также в слизистой оболочке трахеи, бронхов, иногда в моче.
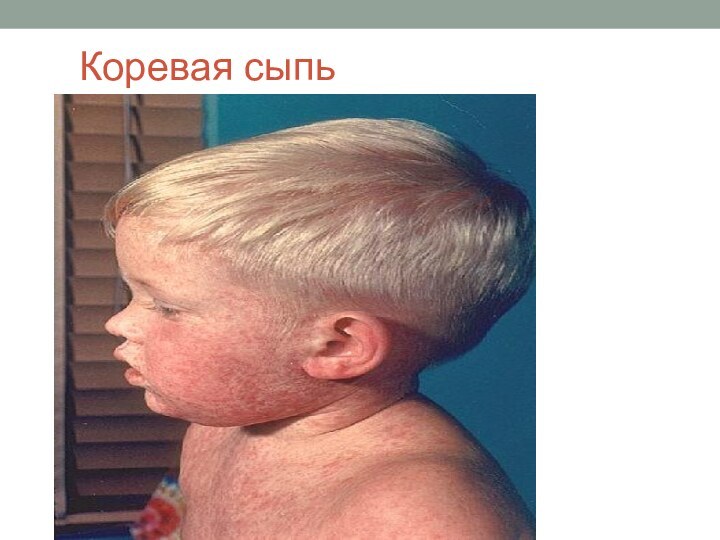
Иммуноопосредованное повреждение эндотелия кожных капилляров - причина коревой сыпи
Генерализованное поражение дыхательных путей приводит к потере ресничек эпителия, что создает условия для развития вторичных бактериальных инфекций, таких как средний отит и пневмония.
Происходит генерализованная гиперплазия лимфоидной ткани, в лимфатических узлах, миндалинах, аденоидах, селезенке обнаруживаются многоядерные гигантские клетки.
Слайд 21
Insert figure 25.5
Effects of paramyxoviruses
Слайд 22
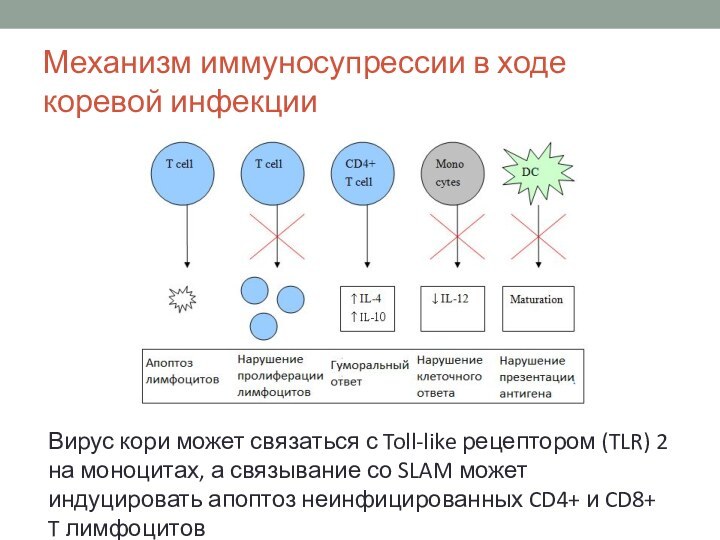
Механизм иммуносупрессии в ходе коревой инфекции
Вирус кори может
связаться с Toll-like рецептором (TLR) 2 на моноцитах, а
связывание со SLAM может индуцировать апоптоз неинфицированных CD4+ и CD8+ T лимфоцитов
Слайд 23
1.Инкубационный период (3-4 дня) – размножение вируса в
эпителиальных клетках вдп и региональных лифоузлах, проникновение из крови
(виремия) в лимфоидную ткань
2.Катаральный период (2-4 дня) – поражение слизистой вдп и полости рта (участки некротизированного эпителия, например пятна Коплика-Филатова), конъюнктивы, ЦНС
Клиника
Слайд 24
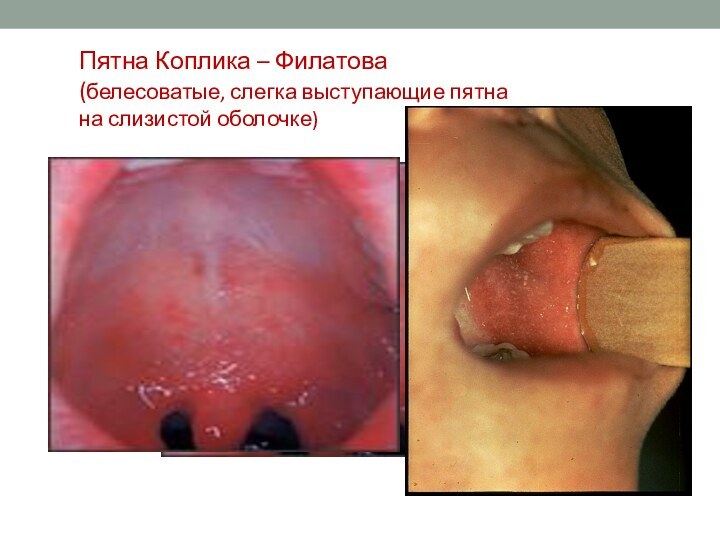
Пятна Коплика – Филатова
(белесоватые, слегка выступающие пятна
на
слизистой оболочке)
Слайд 25
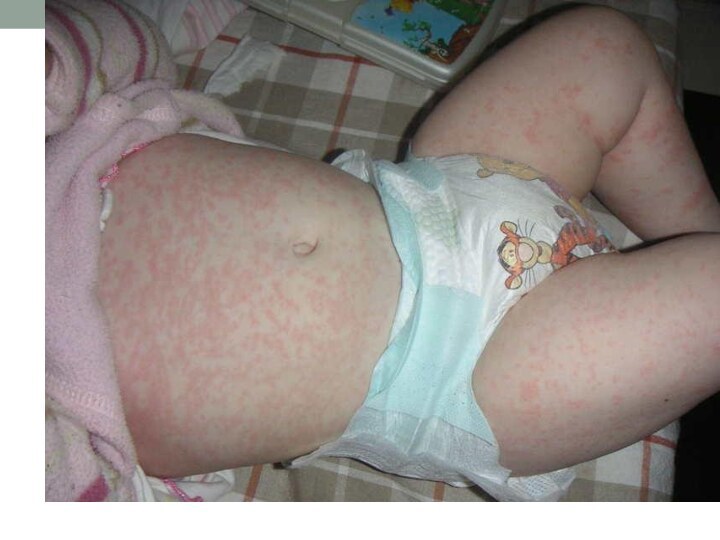
3.Период высыпания (около 5дней) - пятнисто-папуллезная сыпь как
следствие развития периваскулярного воспаления капилляров
4.Период пигментации – появление бурого
оттенка на месте элементов сыпи и далее мелкое отрубевидное шелушение
Клиника
Слайд 26
Корь имеет сходство с такими заболеваними, как
Краснуха
Лихорадка Денге
Инфекции,
вызванные вирусами Коксаки, ЕСНО, парвовирусом В19, вирусом герпеса 6
типа
Некоторые бактериальные инфекции, риккетсиозы
Сходные проявления имеют: болезнь Кавасаки, токсический шок, лекарственные аллергии
Слайд 27
ФОРМЫ ИНФЕКЦИИ
Типичная(манифестная) и атипичная
Легкая, средней тяжести, тяжелая
Митигированная
(встречается у привитых людей)
Как правило, дети умирают не непосредственно
от кори, а от ее осложнений, таких как пневмония и диарея, возникающих на фоне иммуносупрессии, сопровождающей коревую инфекцию.
Кроме того, корь может приводить к стойкой инвалидизации больного вследствие развития тяжелых поражений мозга, слепоты и глухоты
Слайд 28
После перенесенного заболевания остается прочный (пожизненный) иммунитет. Вирус
кори подавляет активность Т-лимфоцитов и вызывает ослабление защитных реакций
организма.
У лиц с нарушением Т-клеточного иммунитета болезнь протекает крайне тяжело (ВИЧ-инфицированные, онкология)
Через 10-12 лет после перенесенного заболевания может развиться ПСПЭ (подострый склерозирующий панэнцефалит)
Иммунитет
Слайд 29
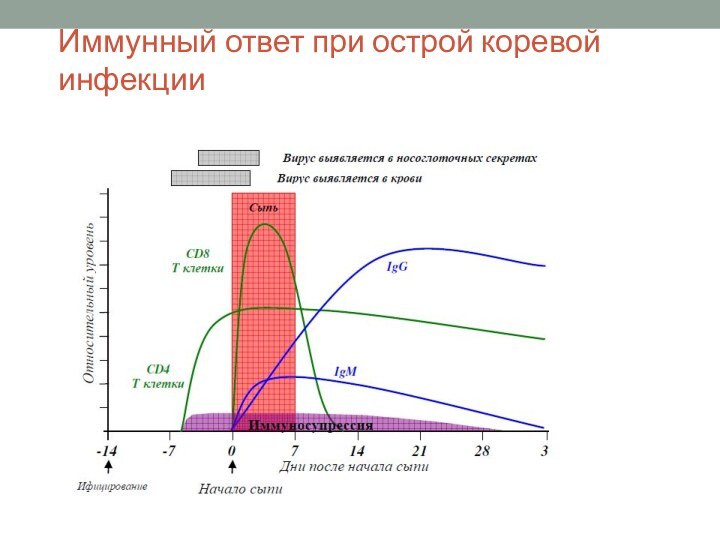
Иммунный ответ при острой коревой инфекции
Слайд 30
Подострый склерозирующий панэнцефалит
Медленная вирусная инфекция со смертельным исходом
Связана
с персистированием вируса кори в ЦНС
В клетках нейроглии накапливается
большое количество дефектных вирусов(нуклеокапсидов)
Разрушение мозговых клеток, гибель нейронов и олигодендроцитов
Диагностика – обнаружение противокоревых АТ в спинномозговой жидкости и сыворотке
Слайд 34
Профилактика и лечение
Специфической терапии нет
Нормальный донорский
иммуноглобулин может предотвратить развитие тяжелой клинической картины заболевания
Слайд 35
Профилактика и лечение
Для специфической профилактики применяется живая аттенуированная
коревая вакцина ( в РФ из штамма Л16), а
также комплексная вакцина MMR (против кори, эпидемического паротита и краснухи)
Слайд 36
ЛАБОРАТОРНАЯ ДИАГНОСТИКА
ЭКСПРЕСС-ДИАГНОСТИКА
Для раннего выявления АГ(метод иммунофлюоресценции, материал
– пораженные эпит.кл. из отделяемого носоглотки или соскобов элементов
сыпи)
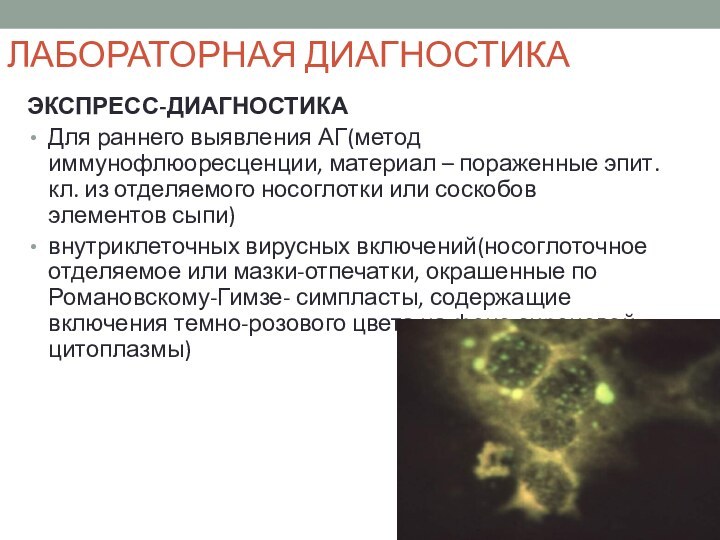
внутриклеточных вирусных включений(носоглоточное отделяемое или мазки-отпечатки, окрашенные по Романовскому-Гимзе- симпласты, содержащие включения темно-розового цвета на фоне сиреневой цитоплазмы)
Слайд 37
С помощью высокочувствительного иммуноферментного анализа (ИФА) IgM антитела
выявляются в 90% случаев кори спустя три дня после
появления сыпи.
Уровень IgM антител достигает пика через 7-10 дней, а затем быстро снижается, и позднее 6-8 недель IgM антитела выявляются крайне редко.
Уровень IgG антител нарастает в течение 4 недель и сохраняется длительное время после инфекции (4х кратное повышение титра).
Кроме того, вырабатываются сывороточные и секреторные IgA антител
Серологическая диагностика
Слайд 38
При лабораторном подтверждении случаев с клиническим диагнозом "корь"
на территории республики Беларусь диагноз подтверждался по серологическим показателям
только у 6 пациентов из 14. В то же время генодиагностика кори подтверждала клинический диагноз у всех пациентов (14 из 14).
Большинство случаев кори на территории с высоким показателем применения профилактических прививок представляют собой случаи нетипично протекающей "вакцинно модифицированной" кори, для правильной диагностики которых необходимо применение как серологических, так и молекулярно-вирусологических методов анализа клинических образцов в комплексе.
Молекулярно-генетические методы