Слайд 2
Лейшманиозы - группа трансмиссивных болезней человека преимущественно зоонозной
природы.
Существует две группы лейшманиозов человека:
висцеральные, характеризующиеся преимущественным
поражением внутренних органов,
кожные, при которых наблюдаются локальные патологические изменения кожи, иногда слизистых оболочек.
Слайд 3
Лейшмании относятся к типу Sarcomastigophora, подтипу Mastigophora (жгутиконосцы),
роду Leishmania.
Инфекцию у людей вызывают 21 из 30 видов,
инфицирующих млекопитающих. Они включают
L. donovani-комплекс с 3 видами (L donovani, L. infantum, L. chagasi);
L. mexicana-комплекс с З главными видами (L. mexicana, L. amazonensis, L. venesuelensis);
L tropica; L. major; L. aethiopica;
подрод Viannia с 4 главными видами: L.(V.) braziliensis, L (V.) guyanensis, L. (V.)panamensis, L. (V.)peruviana
Слайд 4
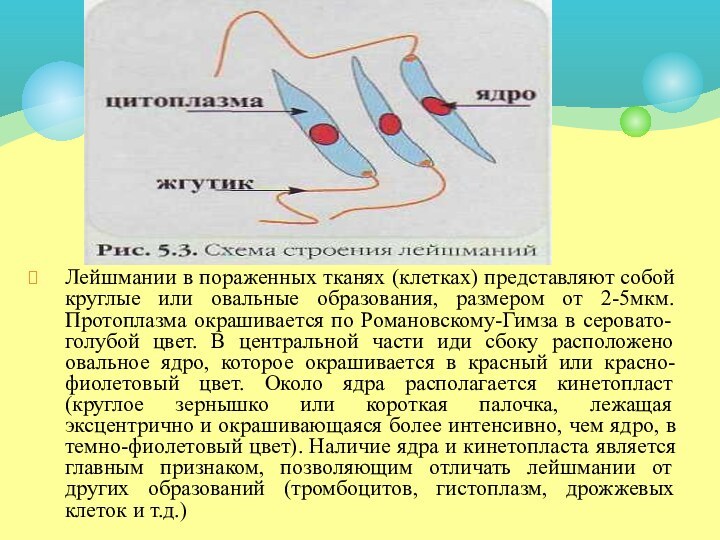
Лейшмании в пораженных тканях (клетках) представляют собой круглые
или овальные образования, размером от 2-5мкм. Протоплазма окрашивается по
Романовскому-Гимза в серовато-голубой цвет. В центральной части иди сбоку расположено овальное ядро, которое окрашивается в красный или красно-фиолетовый цвет. Около ядра располагается кинетопласт (круглое зернышко или короткая палочка, лежащая эксцентрично и окрашивающаяся более интенсивно, чем ядро, в темно-фиолетовый цвет). Наличие ядра и кинетопласта является главным признаком, позволяющим отличать лейшмании от других образований (тромбоцитов, гистоплазм, дрожжевых клеток и т.д.)
Слайд 5
Жизненный цикл лейшманий протекает со сменой хозяев: позвоночного
животного или человека и переносчика – москита.
Москиты –
мелкие двукрылые насекомые, величиной от 1,2 до 3,7 мм. Москиты распространены во всех частях света в тропической и субтропической зонах, в поясе, заключенном между 500 с.ш. и 400 ю.ш. Москиты обитают как в населенных пунктах, так и природных биотопах.В населенных пунктах местами выплода москитов служат подполья, свалки мусора и другие места, где скапливаются гниющие органические вещества. В природных условиях москиты выплаживаются в норах грызунов, гнездах птиц, пещерах, дуплах деревьев.
Слайд 6
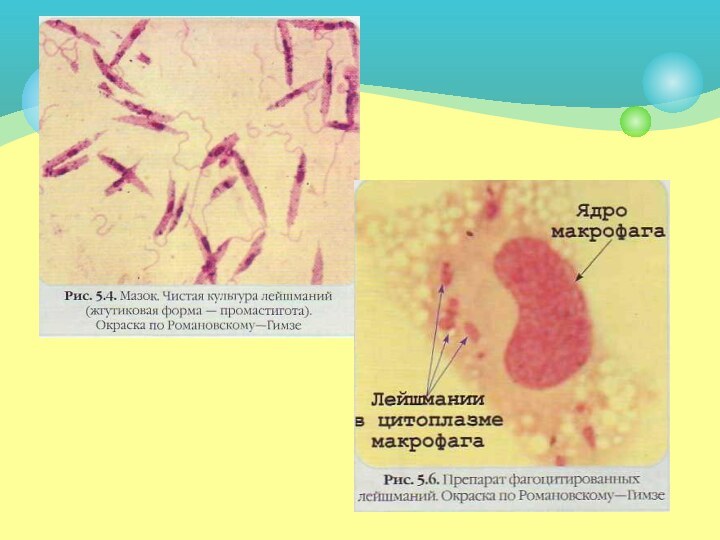
В жгутиковом цикле паразиты развиваются на питательных средах
или в кишечнике москита, зараженного при сосании крови больных
людей или животных. Заглоченные москитом амастиготы превращаются в кишечнике в промастиготы, делятся и на 6—8-е сутки накапливаются в глотке москита. Возбудитель имеет удлиненную веретенообразную форму (длина 10—20 мкм, поперечник — около 5 мкм). Протоплазма содержит ядро, цитоплазму, зерна волютина и кинетопласт. Жгутик, отходящий от заостренного конца, способствует перемещению лейшманий.
Безжгутиковый цикл проходит в ретикулоэндотелиальных клетках печени, селезенки, лимфатических узлов, в макрофагах (рис. 19.2, 6) инфицированного организма. Паразиты имеют округлую форму (2—5 мкм), без жгутиков.
Слайд 8
По данным Всемирной организации здравоохранения лейшманиозы распространены в
88 странах мира, в 32 странах заболевания подлежат обязательной
регистрации.
В настоящее время выделяют следующие основные формы лейшманиозов:
I. Лейшманиозы Старого Света:
1. Висцеральный (индийский кала-азар – антропоноз и средиземноморско-среднеазиатский – зооноз), возбудитель L.donovani.
2. Кожный лейшманиоз: антропонозный или «городской», вызываемый L.Tropica, зоонозный или «сельский», вызываемый L.Major и диффузный кожный лейшманиоз, вызываемый L.Aethiopica.
Эпидемиология.
Слайд 9
II. Лейшманиозы Нового Света:
1. Висцеральный лейшманиоз.
2. Кожные и
кожно-слизистые лейшманиозы (мексиканский - L.Mexicana, перуанский (Ута) - L.Peruviana,
гвианский (лесная фрамбезия) - L.Guyаnensis, панамский - L.Panamensis, кожно-слизистый лейшманиоз (эспундия) - L.Braziliensis или L.Peruviana).
Слайд 10
Источником заражения при висцеральном антропонозном лейшманиозе является больной
человек.
При висцеральном зоонозном лейшманиозе основным природным резервуаром возбудителя
являются собаки. Дополнительным резервуаром выступают шакалы, лисы, волки, енотовидные собаки, в Судане – грызуны, в Италии – черные крысы.
Источником инвазии при кожном антропонозном лейшманиозе является человек, дополнительным резервуаром является больная собака.
При зоонозном кожном лейшманиозе основным природным резервуаром служат грызуны, например, большая песчанка.
Переносчиком во всех случаях служит москит.
Слайд 11
Инкубационный период от нескольких дней до года. Возможно
длительное бессимптомное присутствие лейшманий в организме зараженного. Заболевание может
развиться на фоне появившегося иммунодефицита. В типичных случаях на месте укуса у 50% больных развивается уплотненный узелок или небольшая бледно-розовая папула – первичный эффект. Наиболее частые симптомы – лихорадка, слабость, ознобы, потеря веса, снижение аппетита, болезненность в левом подреберье. Практически во всех случаях присутствует ненапряженная спленомегалия, которая может сопровождаться гепатомегалией, лимфаденопатией, бледностью кожных покровов и слизистых оболочек.
Клинические проявления
Слайд 12
В Индии для висцерального лейшманиоза характерно потемнение кожи.
В Восточной Африке часто развиваются признаки недостаточности питания (отеки,
изменения кожи и волос).
У местного населения очагов частой сопутствующей инфекцией выступает туберкулез.
У пришлых контингентов часто развиваются осложнения: острая гемолитическая анемия, острая почечная недостаточность, обширные геморрагии в слизистые оболочки.
Слайд 13
При антропонозном кожном лейшманиозе на месте укуса зараженных
москитов (чаще лицо, верхние конечности) появляются малозаметные бугорки диаметром
2-3 мм, которые медленно увеличиваются и через 3-4 месяца достигают 5-10 мм в диаметре. Чаще на поверхности бугорка появляется едва заметное западение и образуется чешуйка, которая превращается затем в плотно прикрепленную к бугорку желтовато-буроватую корочку. После перенесенного кожного лейшманиоза примерно в 10% случаев развивается вялотекущий хронический туберкулоидный кожный лейшманиоз, клинически напоминающий туберкулезную волчанку.
Слайд 14
При зоонозном кожном лейшманиозе в месте укуса москита
(чаще всего на коже конечностей, особенно нижних) появляется бугорок
более крупных размеров, окруженный ободком воспаленной кожи. Появляющаяся воспалительная папула или фурункулоподобный узел в процессе развития через 1-2 недели подвергается центральному некрозу, вследствие чего образуется язва с круто обрывистыми краями диаметром 2-4 мм. Дно язвы неровное, обычно покрыто желтовато-серым или желтовато-зеленым налетом; отделяемое язв серозно-гнойное, обильное.
Слайд 15
У переболевших людей остается стойкий пожизненный иммунитет.
Иммунитет.
Слайд 16
Основной метод лабораторной диагностики – микроскопический.
Материалом для
исследования являются:
костный мозг для диагностики висцерального лейшманиоза,
язвенный
краевой инфильтрат, содержимое кожных бугорков для диагностики кожного лейшманиоза.
Лейшмании легко обнаруживаются в бугорках и в краевом инфильтрате язвы на начальных стадиях изъязвления; в гнойном отделяемом язвы могут быть обнаружены лишь деформированные и разрушающиеся лейшмании (по которым трудно поставить диагноз); на стадии заживления в пораженных тканях лейшмании обнаруживаются редко.
Лабораторная диагностика.
Слайд 18
Висцеральный лейшманиоз лечат препаратами 5-валентной сурьмы: натрия стибоглюконат
(пентостам, натрия антимониглюконат) или меглумин антимонат (глюкантим). Суточная доза
препарата вводится за один прием внутримышечно, детям предпочтительно внутривенное введение. Расчет суточной дозы составляет 20 мг/кг (из расчета по сурьме). Инъекции делают ежедневно. Курс лечения 30 дней. При тяжелом течении болезни и неэффективном лечении препаратами сурьмы назначают амфотерицин В и паромомицин. Амфотерицин В назначают по 0,5 мг/кг внутривенно ежедневно или через день до достижения курсовой дозы 20 мг/кг. Паромомицин – по 15мг/кг ежедневно внутримышечно в течение 30 дней. Возможно поражение почек и слухового нерва. Для лечения висцерального лейшманиоза также применяют пентамидин изотионат, 4 мг/кг через день в течение 11 недель и лизосомальный амфотерицин В, курсовая доза 20-30 мг/кг вводится в течение 10-20 дней.
Лечение.
Слайд 19
Первый пероральный препарат для лечения висцерального лейшманиоза –
милтефозин – зарегистрирован в Индии после проведения полномасштабных испытаний.
Предполагается, что этот препарат заменит препараты 5-валентной сурьмы и амфотерицин В в качестве лекарства первой линии. ВОЗ считает целесообразным массовое использование милтефозина во всех высокоэндемичных странах, прежде всего в Индии, Непале, Судане, Бразилии.
Слайд 20
При кожном лейшманиозе если заболевание не сильно беспокоит
больного, этиотропную терапию лучше не проводить, а предоставить течению
болезни естественное развитие. В качестве специфического лечения применяют те же препараты, что и для лечения висцерального лейшманиоза. На ранних стадиях при образовании единичных бугорков возможно обкалывание специфическими препаратами или применение мазей, содержащих хлорпромазин (2%), паромомицин (15%) или клотримазол (1%).
Слайд 22
Амебиаз – протозойный антропоноз, в клинически выраженных случаях
проявляющийся преимущественно язвенным поражением толстого отдела кишечника, а также
развитием абсцессов в печени и в других органах.
Возбудителем амебиаза является дизинтерийная амеба – Entamoeba histolytica, которая относится к типу Sarcomastigophorae, подтипу Sarcodina (саркодовые).
Слайд 23
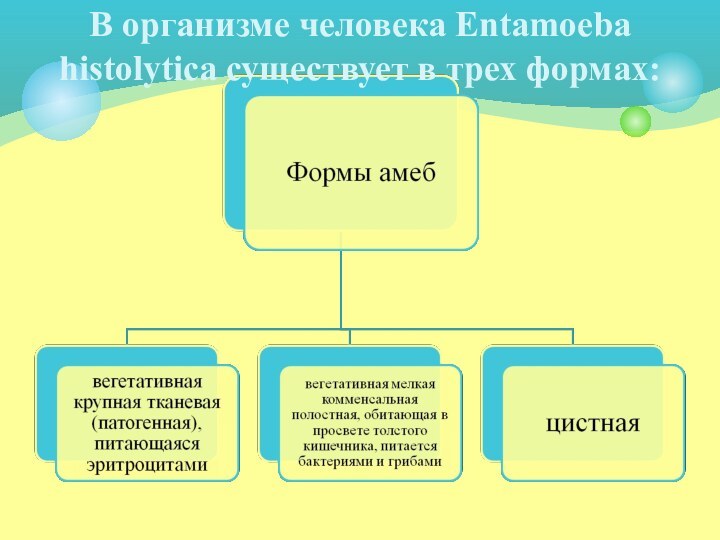
В организме человека Entamoeba histolytica существует в трех
формах:
Слайд 25
Источником инвазии служит человек, выделяющий зрелые цисты амеб.
Механизм передачи амеб фекально-оральный.
Пути передачи – водный, алиментарный
и контактно-бытовой.
Важными факторами передачи служат вода из открытых источников, загрязненных фекалиями и содержащих цисты амеб, а также пищевые продукты, особенно овощи, употребляемые без термической обработки. Амебиазом можно заразиться при непосредственном контакте с носителем через грязные руки и предметы обихода. Известную роль в распространении цист играют тараканы и мухи.
Эпидемиология.
Слайд 26
Под влиянием ряда факторов (понижение сопротивляемости человеческого организма
вследствие перенесения различных болезней, интоксикацией, перегревания, переутомления, травм, ранений)
Entamoeba histolytica проникает в ткани толстой кишки. Она продуцирует протеолитические вещества, лизирующие клетки и ткани, увеличивается в размерах до 30-50 мкм, приобретает способность фагоцитировать эритроциты. Она обычно обнаруживается в кровянистом слизистом стуле больного амебиазом.
Патогенность и патогенез
Слайд 29
Может протекать в острой и хронической формах.
При
остром кишечном амебиазе продолжительность инкубационного периода составляет от нескольких
дней до нескольких месяцев. Больные предъявляют жалобы на вздутие живота и боль в правой подвздошной области. Стул обильный, кашицеобразный, 3-5 раз в сутки с незначительным количеством слизи и крови. Затем стул становится жидким, учащается до 15 раз в сутки, в нем появляется большое количество прозрачной стекловидной слизи. Если язвы расположены в проксимальном отделе толстой кишки, слизь иногда диффузно пропитывается изменившей свой цвет кровью и приобретает вид «малинового желе».
Манифестный кишечный амебиаз
Слайд 30
Вследствие глубокого поражения слизистой всех отделов толстого кишечника
развивается молниеносный амебный колит, который заканчивается летальным исходом в
результате перфораций стенки кишки и развития перитонита.
С течением времени болезнь переходит в хроническую стадию, которая может протекать в рецидивирующей и непрерывной формах.
Слайд 31
Наиболее часто проявляется развитием амебных абсцессов, которые могут
формироваться практически в любом органе. Их развитие обусловлено попаданием
амеб в кровяное русло при нарушении целостности кровеносных сосудов. По системе воротной вены амебы попадают, в первую очередь, в печень, где большинство их задерживается. Поэтому амебные абсцессы образуются в печени гораздо чаще, чем в других органах.
Внекишечный амебиаз
Слайд 32
При кишечном амебиазе могут развиться перфорация стенки кишки,
амебный аппендицит, кишечная непроходимость, выпадение прямой кишки, кишечные кровотечения.
При внекишечном амебиазе наиболее грозным осложнением является прорыв абсцесса в окружающие органы.
Осложнения
Слайд 33
Нестойкий, активируется преимущественно клеточное звено.
Иммунитет.
Слайд 34
Диагноз амебной дизентерии может считаться установленным только при
обнаружении в испражнениях больного тканевых форм дизентерийной амебы или
гаматофагов. Такие амебы-гематофаги выявляются обычно в острой стадии болезни в жидких кроваво-слизистых испражнениях при просмотре комочков слизи или при исследовании субстрата из-под краев язв, взятого при ректороманоскопии. Материал должен просматриваться не позднее 15-20 мин после его получения, желательно, с применением нагревательного столика, так как при охлаждении амебы быстро теряют подвижность и округляются. В таком состоянии их трудно отличить от других клеточных элементов.
Лабораторная диагностика.
Слайд 35
В диагностике внекишечного амебиаза широко используют инструментальные методы
обследования (рентгенография и компьютерная томография, УЗИ), которые позволяют выявить
амебные абсцессы, характерным признаком которых является неполное их заполнение полужидким содержимым.
Слайд 36
Серологические методы исследования на основе ИФА и НРИФ.
Специфические антитела в организме больного вырабатываются только на тканевые
формы Entamoeba histolytica, тогда как присутствие просветных форм не вызывает иммунного ответа. Данные методы позволяют в 75-80% случаев подтвердить диагноз кишечного амебиаза и в 95% - внекишечного. У переболевших через 6-12 месяцев титры антител постепенно снижаются. В лабораторной диагностике амебиаза используют также метод ПЦР.
Слайд 37
Используют метронидазол взрослым и детям с 12 лет
внутривенно капельно по 500 мг 4-6 раз в сутки
(максимальная суточная доза 4 г) или перорально по 750 мг 3 раза в сутки на протяжении 10 дней. Тинидазол назначается из расчета 30 мг/(кгхсут) на протяжении 3 дней. Секнидазол 2 г однократно, только один день (детям – в дозе 30 мг/кг), дигидроэметин в суточной дозе 1 мг/кг в/мышечно или подкожно (не более 60 мг) однократно в течение 4-6 дней, детям не более 5 дней.
Лечение.
Слайд 38
Выявление и лечение больных, санация бессимптомных носителей.
При плановых
бактериологических обследованиях работников системы водоснабжения и питания обследуют на
амебиаз.
Профилактика.
Слайд 40
Трипаносомы относятся к роду Tripanosoma
Для человека патогенны:
Tripanosoma
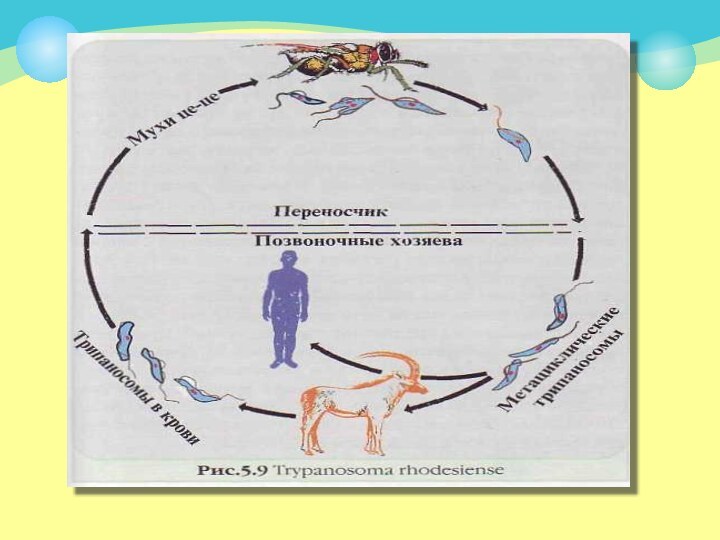
brucei gambiense и Tripanosoma brucei rhodesiense (разновидности Tripanosoma brucei),
вызывающие африканский трипаносомоз, или сонную болезнь,
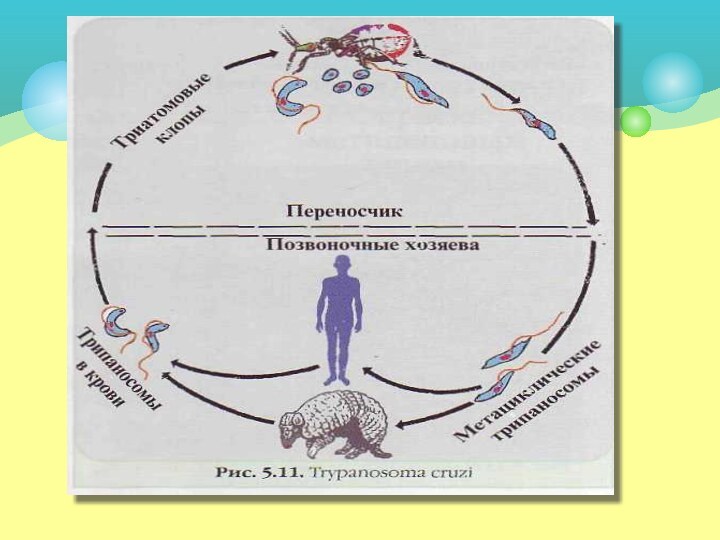
Tripanosoma cruzi — возбудитель американского трипаносомоза (болезнь Шагаса).
Слайд 41
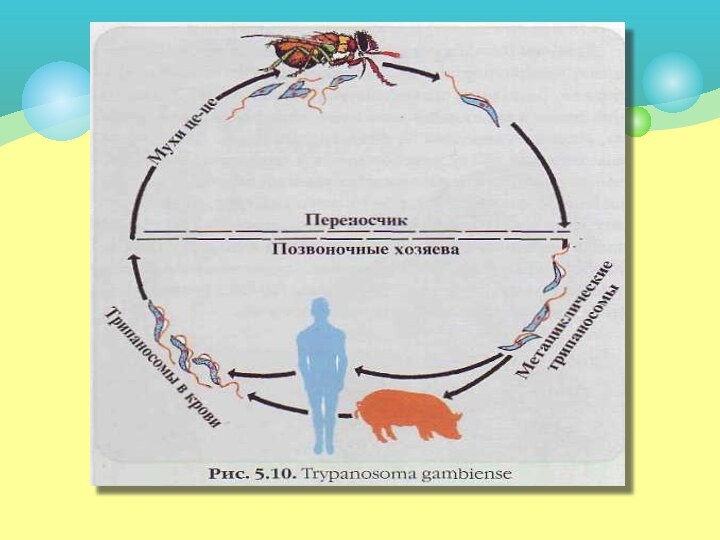
Трипаносомозы — трансмиссивные болезни. Источником инфекции являются домашние
и дикие животные, инфицированный человек.
Переносчиком африканского трипаносомоза являются
кровососущие мухи цеце, а болезни Шагаса — триатомовые клопы
Эпидемиология
Слайд 42
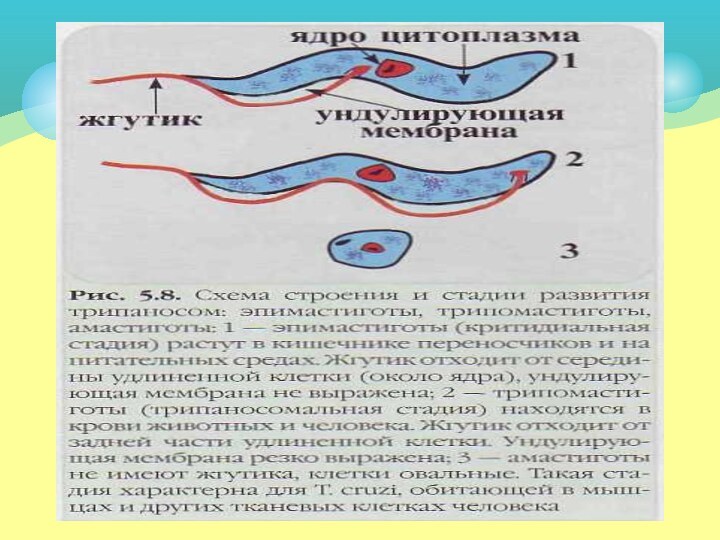
Возбудители имеют различные стадии развития:
Слайд 44
Африканский трипаносомоз, вызываемый Т. gambiense (гамбийская форма), протекает
хронически, а если возбудителем является Т. rhodesiense (родезийская форма)
— развивается острая, более тяжелая форма болезни.
Патогенез и клиника
Слайд 45
В месте укуса переносчиком — мухой цене к
концу недели развивается изъязвляющаяся папула — «трипаносомный» шанкр, откуда
размножающиеся паразиты попадают в кровь (паразитемия), где продолжают размножение. Возбудитель обнаруживается также в лимфоузлах, цереброспинальной жидкости.
Развиваются лихорадка, менингоэнцефалит, сонливость, утомляемость, истошение и другие нарушения, приводящие к летальному исходу. Возможно бессимптомное носитсльство возбудителя.
Слайд 46
Американский трипаносомоз развивается в течение 1—3 недель после
попадания Т. cruzi в слизистые оболочки или ранку от
укуса триагомовыми клопами: возбудитель попадает вместе с инфицированными фекалиями клопов. В участке внедрения паразита образуется плотный инфильтрат темно-красного цвета.
Слайд 47
Попав в кровоток, паразит циркулирует в виде трипомастиготы,
не размножается. Внедрившись в тканевую клетку, трипомастигота превращается в
безжгутиковую форму амастиготу. размножающуюся бинарным делением. Клетки, содержащие большие количества амастигот, разрываются, освобождая многочисленные трипомастиготы, которые вторгаются в другие клетки.
Слайд 48
У больных развиваются лимфаденит, миокардит, лихорадка. Поражаются ЖКТ.
печень, селезенка, головной мозг. Характерен длительный латентный период, вплоть
до нескольких десятилетий. Болезнь протекает остро или хронически.
Слайд 52
В ответ на инвазию образуются в большом количестве
IgM: специфические протективные и неспецифические антитела. В хронической фазе
проявляются lgG-антитела. Трипаносомы способны образовывать многочисленные новые антигенные варианты, изменяющие иммунный ответ. Раширяются аутоиммунные механизмы.
Иммунитет.
Слайд 53
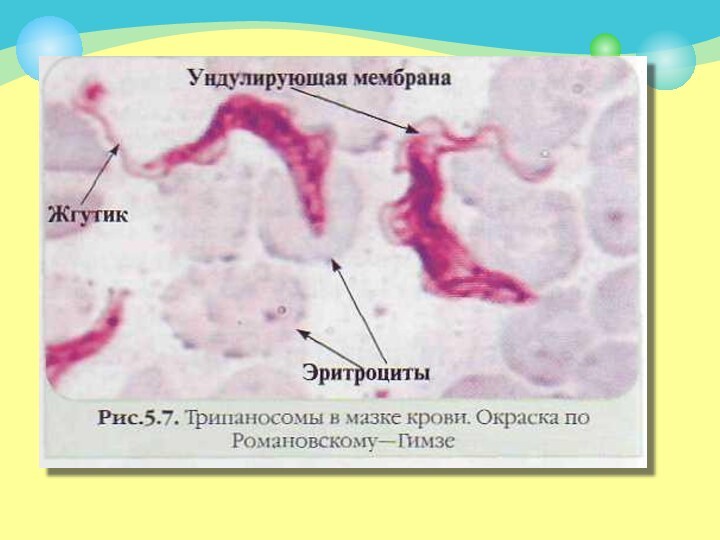
Применяется микроскопический метод диагностики трипаносомозов: мазки из крови,
пунктата шейных лимфатических узлов, цереброспинальной жидкости красят по Романовскому—Гимзе
или по Райту.
Для выделения возбудителя можно заражать белых мышей или крыс, а также делать посев на питательные среды с кровью.
При серологическом методе определяют антитела (IgM) с помощью ИФА, РСК, непрямой РИФ и др.
Микробиологическая диагностика
Слайд 55
Для лечения африканского трипаносомоза назначают сурамин или центамидин,
а при поражении ЦНС — меларсопрол. Лечение американского трипаносомоза
неэффективно.
Лечение.
Слайд 56
Проводят неспецифическую профилактику трипаносомоза путем ликвидации мест выплода
переносчиков возбудителя и уничтожения инфицированных животных.
В личной профилактике
применяют репелленты и защитную одежду. Также выявляют и лечат инфицированных лиц.
Профилактика.
Слайд 58
Трихомоноз — антропонозная болезнь (инвазия), вызываемая мочеполовой трихомонадой
(Trichomonas vaginalis); сопровождается поражениями мочеполовой системы.
Возбудитель относится к типу
Sarcomastigophora, подтипу Mastigophora, классу Zoomastigophoreae, отряду Trichomonadida. Род Trichomonas.
Разлиичают также комменсалы — ротовую (Т. tenax) и кишечную (Т. hominis) трихомонады.
Слайд 59
Трихомонады: а — T. vaginalis; б —
T. tenax; в — T. hominis. 1 — ядрышко;
2 — парабазальный аппарат; 3 — ундулирующая мембрана; 4 — аксостиль; 5 — парабазальная нить; 6 — ядро; 7 — блефаропласт; 8 — передние жгутики; 9 — конечный жгутик.
Слайд 61
Заболевание передается половым путем, через родовые пути (младенцу),
редко — через предметы личной гигиены.
Эпидемиология.
Слайд 62
Trichomonas vaginalis вызывает вагинит, уретрит, простатит. Воспалительный процесс
сопровождается болью, зудом, гнойносерозными выделениями. Часто болезнь протекает бессимптомно.
При
трихомониазе у мужчин поражается мочеиспускательный канал, а у женщин - влагалище и уретра. У девочек заболевание протекает в виде вульвовагинита или вульвовестибуловагинита, при которых не происходит поражение органов малого таза.
Инкубационный период составляет от 5 до 15 дней.
Выделяют несколько форм трихомониаза:
свежая острая, подострая, торпидная
хроническая
трихомонадоносительство
Патогенез и клиника
Слайд 63
Хроническая форма заболевания характеризуется малосимптомным течением, когда с
момента заражения прошло более 2 месяцев. Периодические обострения могут
быть спровоцированны снижением сопротивляемости организма, чрезмерным употреблением алкоголя, изменением рН содержимого влагалища или нарушениями функции яичников. В зависимости от того, насколько часты рецидивы и как тяжело они переносятся, выделяют трихомониаз неосложненный и с осложнениями.
Трихомонадоносительство - форма заболевания, при которой отсутствуют какие-либо симптомы.
Острый трихомониаз проявляется у женщин в виде вагинита.
Слайд 64
Диагностика трихомониаза осуществляется на основании клинических признаков и
лабораторных исследований. Для получения более точного результата применяется среазу
несколько методов, а материал для изучения берется из различных очагов воспаления.
Применяют следующие лабораторные методы:
латекс-агглютинация (используется для выявления трихомонадоносительства)
культуральные (используется для диагностики атипичных форм)
иммунологические (применяются в качестве отборочного теста у женщин)
микроскопия (мазок) нативного препарата (позволяет по грушевидной или овальной форме, а также характерным движениям микроорганизма определить наличие трихомонады)
микроскопия окрашенного препарата (дают возможность проводить исследования, когда материал взят достаточно давно)
люминесцентная микроскопия (основан на свечении микроорганизма в ультрафиолетовых лучах)
Лабораторная диагностика
Слайд 66
Лечение трихомониаза проводят всем половым партнерам, если у
одного из них обнаружена инфекция (трихомонада). Особенностью заболевания является
наличие множества очагов инфекции.
Учитывая этот факт, больным назначается комплексная терапия, включающая:
местное лечение
этиотропные методы (применяют метронидазол, тинидазол, осарсол, аминарсон, фуразолидон)
витамины
биостимуляторы
иммунокорригирующие методы
Лечение.
Слайд 67
Первое контрольное исследование у женщин проводится через 7
дней после окончания лечения. Забор материал для исследования берут
перед менструацией или через 1 - 2 дня после ее. Необходимо лабораторно исследовать образцы из всех очагов поражения. В течение следующих 3-х менструальных циклов женщина проходит контрольное обследование.
Первое контрольное обследование у мужчин проводится на 7-10 день после окончания лечения трихомониаза: пальпаторное обледование предстательной железы и семенных пузырьков, микроскопическое исследование их секрета. Через неделю назначается провокация. Если после провокации трихомонадная инфекция не обнаружена, то на последнее контрольное обследование пациент приходит через месяц.