- Главная
- Разное
- Бизнес и предпринимательство
- Образование
- Развлечения
- Государство
- Спорт
- Графика
- Культурология
- Еда и кулинария
- Лингвистика
- Религиоведение
- Черчение
- Физкультура
- ИЗО
- Психология
- Социология
- Английский язык
- Астрономия
- Алгебра
- Биология
- География
- Геометрия
- Детские презентации
- Информатика
- История
- Литература
- Маркетинг
- Математика
- Медицина
- Менеджмент
- Музыка
- МХК
- Немецкий язык
- ОБЖ
- Обществознание
- Окружающий мир
- Педагогика
- Русский язык
- Технология
- Физика
- Философия
- Химия
- Шаблоны, картинки для презентаций
- Экология
- Экономика
- Юриспруденция
Что такое findslide.org?
FindSlide.org - это сайт презентаций, докладов, шаблонов в формате PowerPoint.
Обратная связь
Email: Нажмите что бы посмотреть
Презентация на тему Из чего всё на свете? Презентация презентация к уроку (2 класс)
Содержание
- 2. Что такое атомы?Из чего состоит окружающий мир?
- 3. Оказывается, все предметы, все вещества на свете
- 4. Атомы такие маленькие, что их не разглядеть
- 5. Из чего построены атомы?Известна простейшая модель для
- 6. Много ли на свете видов атомов?Атомов «разного
- 7. Что такое молекулы?Это мельчайшие, невидимые глазом частички
- 8. Как выглядят молекулы?Так выглядит молекула воды. Правда,
- 9. Как выглядят молекулы?Так выглядит молекула кислорода. Когда
- 10. Как выглядят молекулы?Так выглядит молекула углекислого газа.
- 11. Как малы молекулы?Давайте сравним размер молекулы с
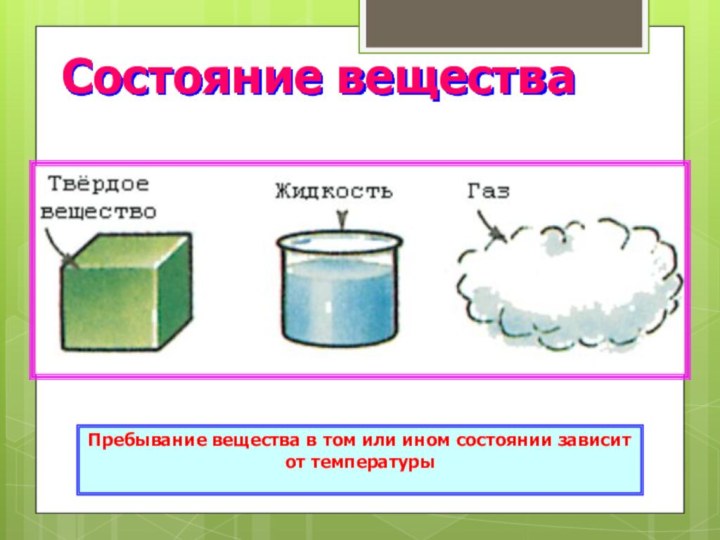
- 12. Состояние веществаПребывание вещества в том или ином состоянии зависит от температуры
- 13. Твердое состояниеТвердое вещество сохраняет свою формуВ твердых веществах частицы расположены упорядоченно и плотно прилегают друг другу
- 14. Жидкое состояниеЖидкость обладает свойством текучести и не
- 15. Газообразное состояниеГаз имеет способность распространятся В газах
- 17. Опыт с монетой.Возьмите монету 10 копеек. Закрепите
- 18. Опыт с монетой.Нагретая металлическая монета не помещается между булавками, где она лежала до нагревания.Почему?
- 19. Скачать презентацию
- 20. Похожие презентации
Что такое атомы?Из чего состоит окружающий мир?















Слайд 3 Оказывается, все предметы, все вещества на свете состоят
из крошечных- прекрошечных частичек –АТОМОВ.
Греции. Оно означает «неделимый».Слайд 4 Атомы такие маленькие, что их не разглядеть даже
в микроскоп, который увеличивает в сто тысяч раз. Для
того, чтобы увидеть атом, его надо увеличить в миллион раз.Атомы маленькие как эта точка? .
В миллион раз меньше!
Слайд 5
Из чего построены атомы?
Известна простейшая модель для описания
атома, которая была придумана почти 100 лет назад – Модель
РезерфордаПредставать её себе можно так: есть большое положительно заряженное ядро – такой большой красный шарик с зарядом “+”. Вокруг этого красного шарика, как планеты вокруг Солнца, летают электроны – маленькие синие шарики с зарядом “–“
Слайд 6
Много ли на свете видов атомов?
Атомов «разного сорта»
больше, чем букв в алфавите. Насчитывается 107 видов атомов,
причём не все они встречаются в природе- некоторые получены учёными искусственно.О некоторых атомах вы уже слышали: железо, золото, серебро, йод, кислород, ртуть и другие.
Слайд 7
Что такое молекулы?
Это мельчайшие, невидимые глазом частички вещества.
Как из букв алфавита образуются слова, так из атомов
образуются молекулы.Какие атомы «соберутся», в каком порядке построятся, такая молекула из них и получится.
Например, в молекуле воды – три атома.
Слайд 8
Как выглядят молекулы?
Так выглядит молекула воды. Правда, похожа
на голову медвежонка Винни-Пуха? Вон как ушки навострила! Конечно,
никакие это не ушки, а два атома водорода, присоединившиеся к «голове» – атому кислорода.
Слайд 9
Как выглядят молекулы?
Так выглядит молекула кислорода. Когда говорят
«мы дышим кислородом», имеют в виду именно молекулы двух
атомов кислорода. И в кислородной подушке, которую дают тяжелобольным людям, такие молекулы, и в стальном баллоне со сжатым кислородом, и в жидком кислороде, которым заправляют ракеты, - точно такие же двухатомные молекулы.
Слайд 10
Как выглядят молекулы?
Так выглядит молекула углекислого газа. В
ней два атома кислорода присоединились с разных сторон к
атому углерода.
Слайд 11
Как малы молекулы?
Давайте сравним размер молекулы с кристаллами
поваренной соли.
Итак, насыпьте на стол немного соли. Выберите из
кучки самый мелкий кристаллик. А теперь вообразите себя Алисой в Стране чудес. Сейчас вы начнёте стремительно уменьшаться в размерах. При этом кристаллик соли заметно вырастает. Вот он с детскую кроватку. Вот он стал размером с дом. Вот кристалл упирается в небо. Постепенно вершина кристалла соли исчезает из виду. Теперь он для вас имеет высоту ста небоскрёбов, поставленных один на другой. И вдруг вы замечаете пушинку и пытаетесь её поймать.Так вот, то, что лежит у вас на ладони, и есть молекула.
Слайд 13
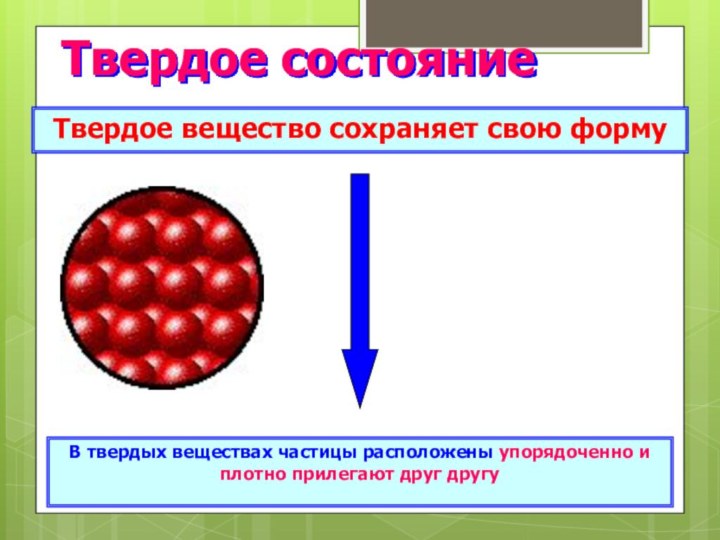
Твердое состояние
Твердое вещество сохраняет свою форму
В твердых веществах
частицы расположены упорядоченно и плотно прилегают друг другу
Слайд 14
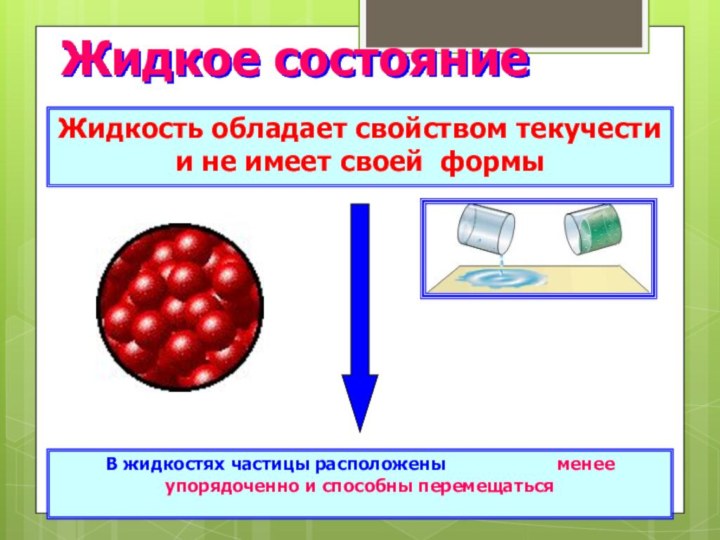
Жидкое состояние
Жидкость обладает свойством текучести и не имеет
своей формы
В жидкостях частицы расположены
менее упорядоченно и способны перемещаться
Слайд 15
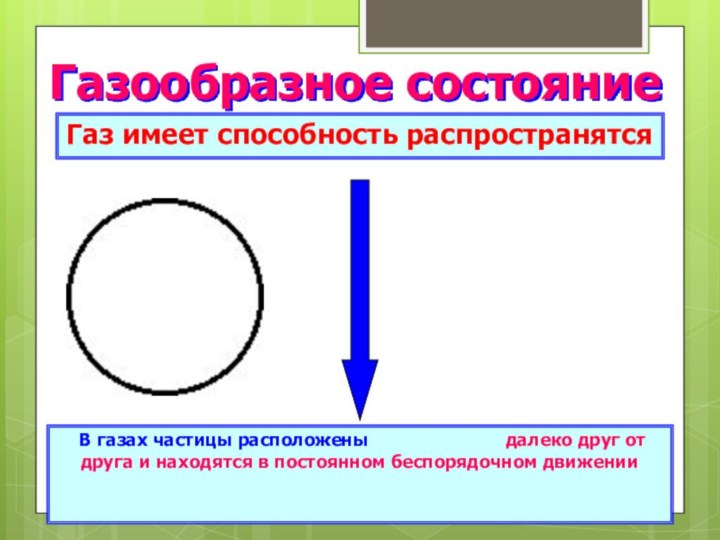
Газообразное состояние
Газ имеет способность распространятся
В газах частицы
расположены
далеко друг от друга и находятся в постоянном беспорядочном движении
Слайд 17
Опыт с монетой.
Возьмите монету 10 копеек.
Закрепите её
между двумя булавками.
Нагрейте монету.
Попробуйте её положить на прежнее место
между булавками.Что происходит?





























