Слайд 2
КЛАССИФИКАЦИЯ АМИНОКИСЛОТ АРОМАТИЧЕСКОГО РЯДА И ПРОИЗВОДНЫХ АРОМАТИЧЕСКИХ АМИНОВ
Производные
пара-аминобензойной кислоты
Сложные эфиры (новакаин, анестезин)
Амиды (новокаинамид)
Проиводные пара-аминосалициловой кислоты (натрия
пара-амино салицилат)
Производные ароматического амина (анилина) (тримекаин, лидокаин, бупивакаин, парацетамол)
Слайд 3
Лекарственные вещества, производные ПАБК
Слайд 4
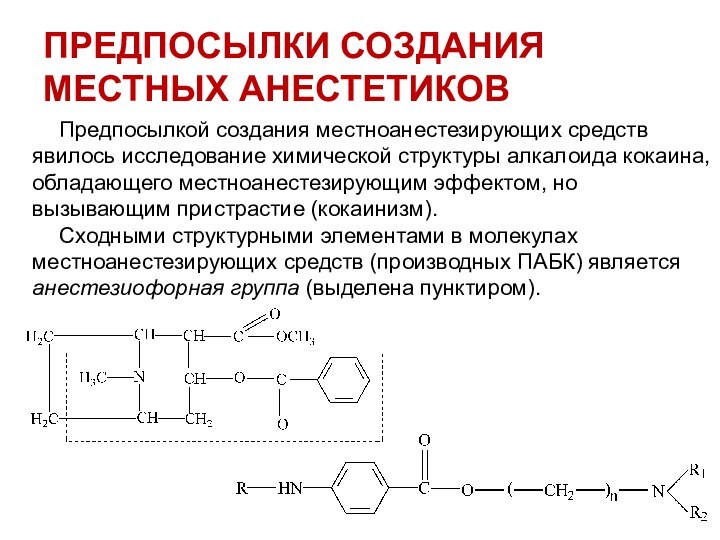
ПРЕДПОСЫЛКИ СОЗДАНИЯ МЕСТНЫХ АНЕСТЕТИКОВ
Предпосылкой создания местноанестезирующих средств
явилось исследование химической структуры алкалоида кокаина, обладающего местноанестезирующим эффектом,
но вызывающим пристрастие (кокаинизм).
Сходными структурными элементами в молекулах местноанестезирующих средств (производных ПАБК) является анестезиофорная группа (выделена пунктиром).
Слайд 5
Свойства лекарственных веществ, производных ПАБК
Anaesthesinum
Aнестезин
МНН Бензокаин
Белый кристаллический порошок
без запаха, слабо-горького вкуса. Тпл.= 89-91,5ºС.
Очень мало растворим в
воде, легко – в спирте, эфире, хлороформе, трудно – в жирных маслах и разведённых соляной кислоты.
этиловый эфир n-аминобензойной
кислоты
Слайд 6
Novocainum новокаин
МНН Прокаина гидрохлорид
Бесцветные кристаллы или белый кристаллический
порошок без запаха, горького вкуса. Т. пл. 154 –
156 ºС
Очень легко растворим в воде, мало – в хлороформе, практически нерастворим в эфире.
β-диэтиламиноэтилового эфира
n-аминобензойной кислоты гидрохлорид
Слайд 7
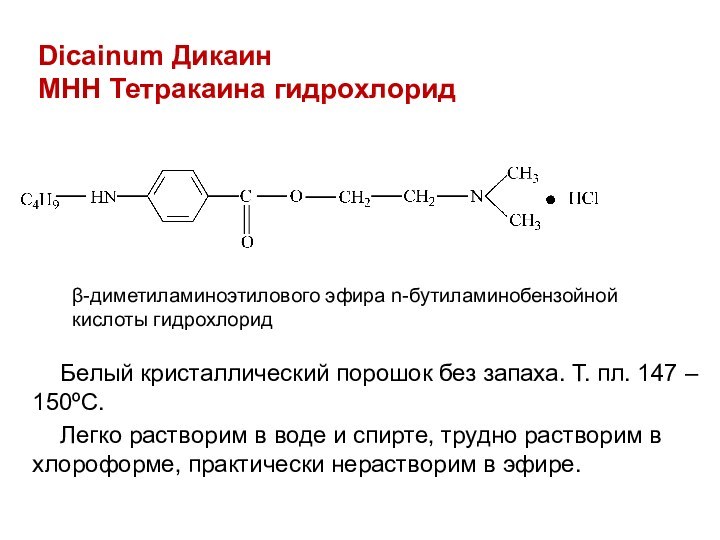
Dicainum дикаин
МНН Тетракаина гидрохлорид
Белый кристаллический порошок без запаха.
Т. пл. 147 – 150ºС.
Легко растворим в воде и
спирте, трудно растворим в хлороформе, практически нерастворим в эфире.
β-диметиламиноэтилового эфира n-бутиламинобензойной кислоты гидрохлорид
Слайд 8
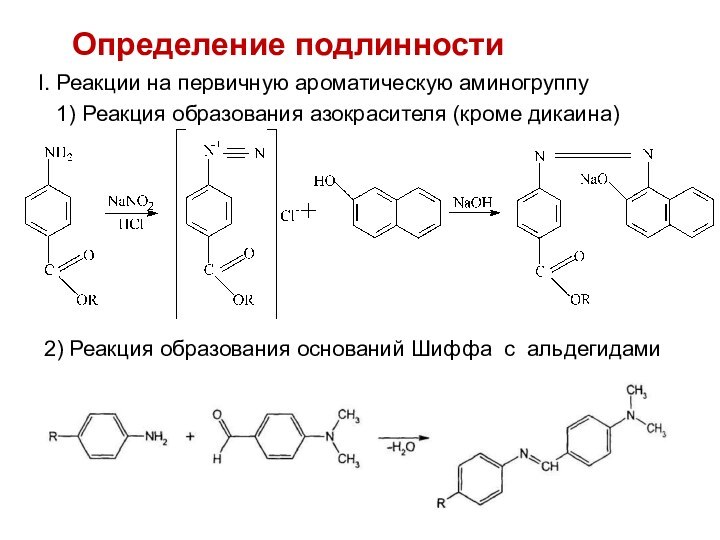
Определение подлинности
I. Реакции на первичную ароматическую аминогруппу
1) Реакция образования азокрасителя (кроме дикаина)
2) Реакция образования оснований
Шиффа с альдегидами
Слайд 9
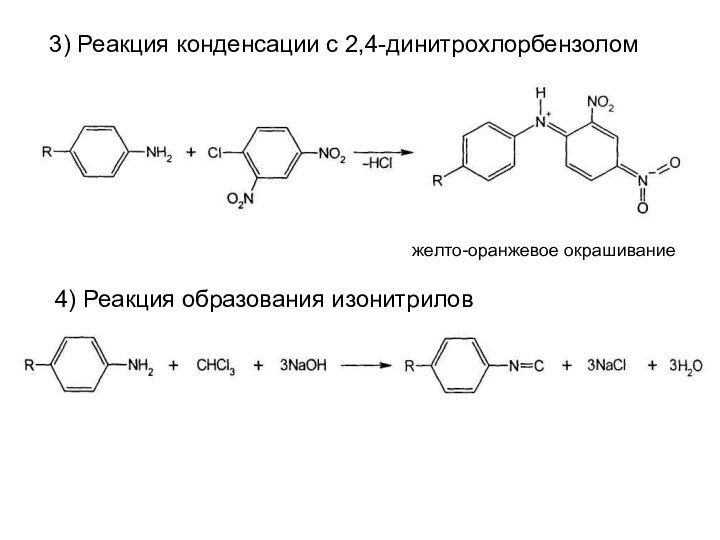
3) Реакция конденсации с 2,4-динитрохлорбензолом
желто-оранжевое окрашивание
4) Реакция образования
изонитрилов
Слайд 10
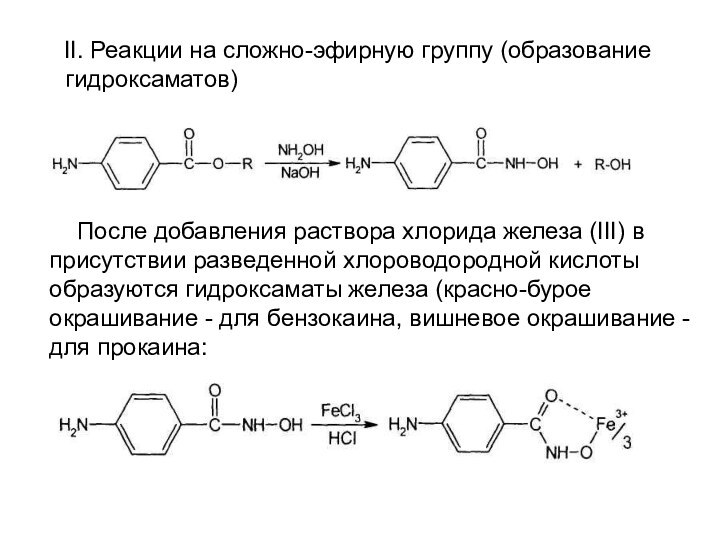
II. Реакции на сложно-эфирную группу (образование
гидроксаматов)
После добавления раствора хлорида железа (III) в присутствии разведенной
хлороводородной кислоты образуются гидроксаматы железа (красно-бурое окрашивание - для бензокаина, вишневое окрашивание - для прокаина:
Слайд 11
Конденсация производных n-аминобензойной кислоты с гексаметилентетрамином в присутствии
концентрированной серной кислоты, слабо-фиолетовая флуоресценция
Осадительные реакции
ИК- и УФ-спектрофотометрия
Определение подлинности
Слайд 12
Частные реакции
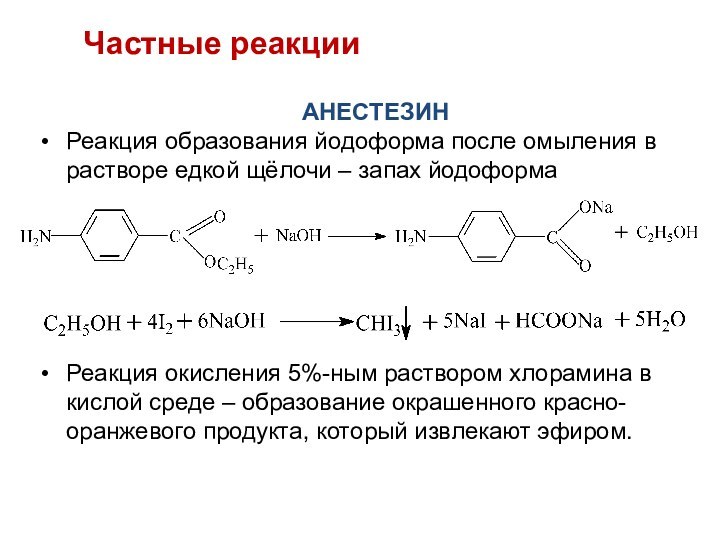
АНЕСТЕЗИН
Реакция образования йодоформа после омыления в
растворе едкой щёлочи – запах йодоформа
Реакция окисления 5%-ным раствором
хлорамина в кислой среде – образование окрашенного красно-оранжевого продукта, который извлекают эфиром.
Слайд 13
Реакция с пергидролем и концентрированной серной кислотой -
постепенно появляется сиреневое окрашивание.
Реакция со смесью концентрированных серной и
азотной кислот при нагревании - образуется оранжево-красное окрашивание.
Обесцвечивание 0,1 н. раствора перманганата калия в кислой среде (реакция позволяет отличать новокаин от других местноанестезирующих лекарственных веществ).
НОВОКАИН
Слайд 14
Осаждение йодидом калия в виде йодоводородной соли.
Под действием
изотиоцианата аммония выпадает в осадок изотиоцианат тетракаина, температура плавления
которого 130-132 °С.
Реакция взаимодействия с йодатом калия в фосфорнокислой среде при нагревании - образуется фиолетовое окрашивание (максимум светопоглощения - 552 нм). Реакция является специфичной и позволяет отличить дикаин от анестезина и новокаина.
ТЕТРАКАИНА ГИДРОХЛОРИД
Слайд 15
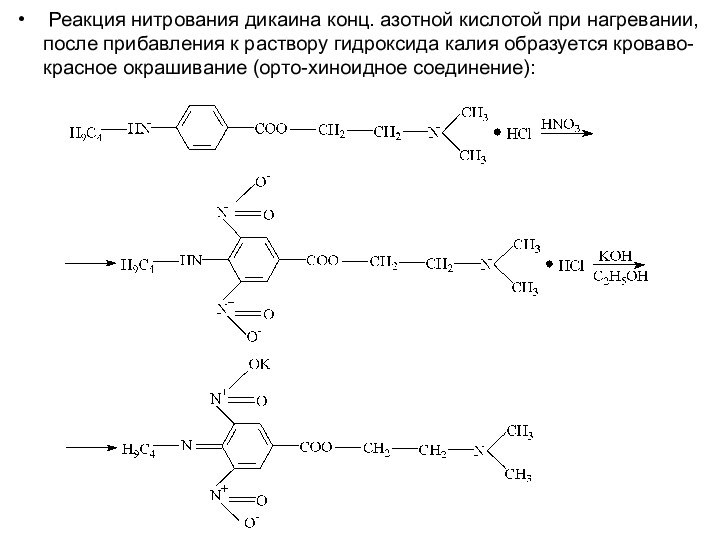
Реакция нитрования дикаина конц. азотной кислотой при
нагревании, после прибавления к раствору гидроксида калия образуется кроваво-красное
окрашивание (oртo-хиноидное соединение):
Слайд 16
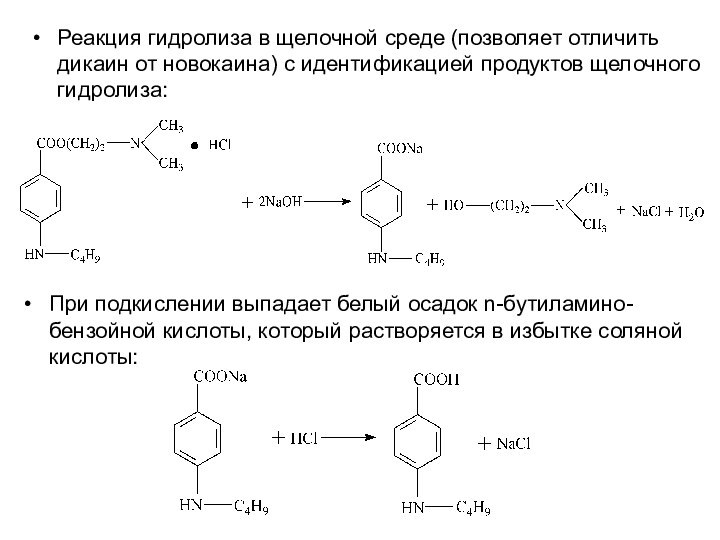
Реакция гидролиза в щелочной среде (позволяет отличить дикаин
от новокаина) с идентификацией продуктов щелочного гидролиза:
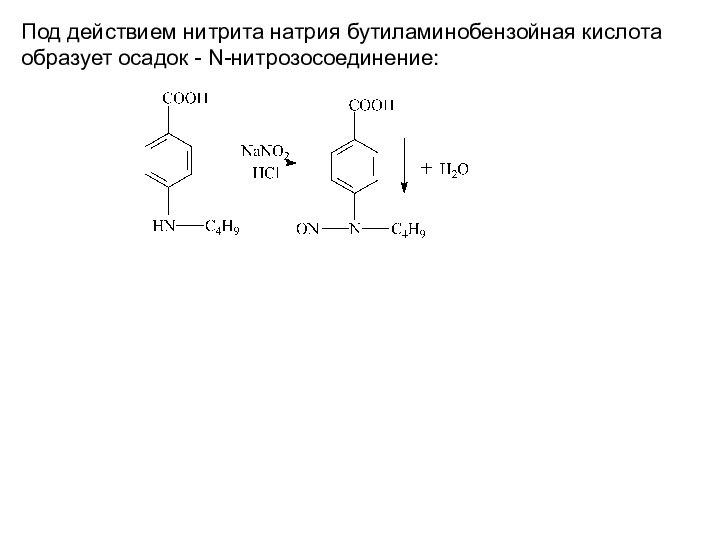
При подкислении выпадает
белый осадок n-бутиламино-бензойной кислоты, который растворяется в избытке соляной кислоты:
Слайд 17
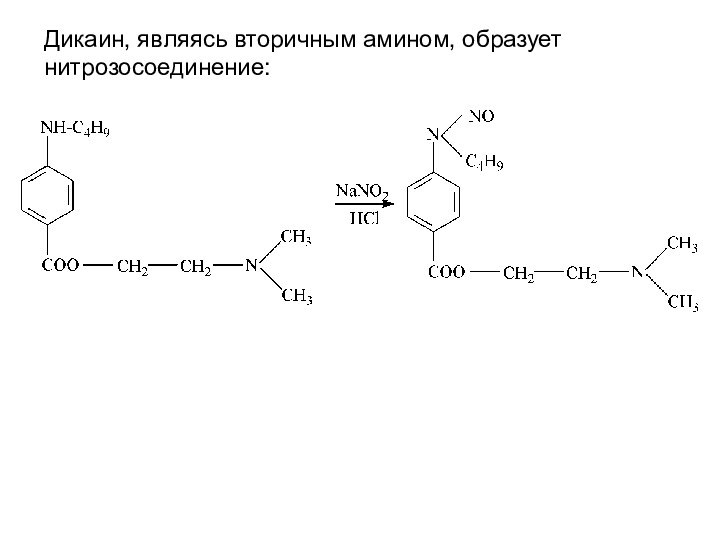
Под действием нитрита натрия бутиламинобензойная кислота образует осадок
- N-нитрозосоединение:
Слайд 18
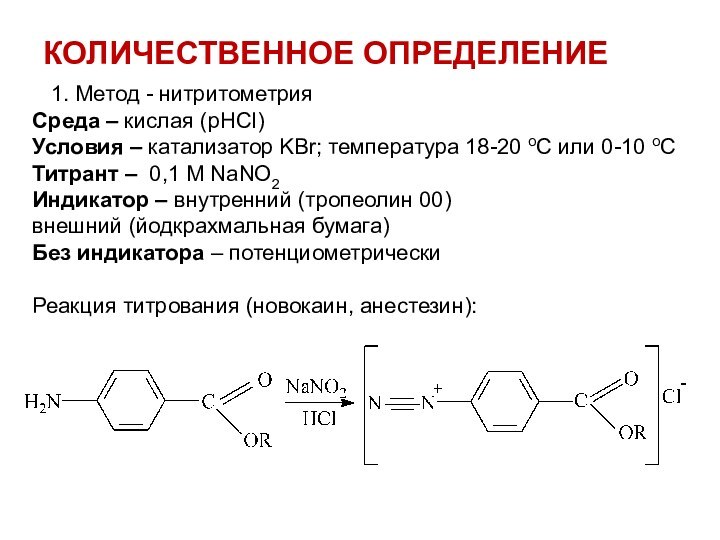
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ
1. Метод - нитритометрия
Среда –
кислая (рHCl)
Условия – катализатор KBr; температура 18-20 оС или
0-10 оС
Титрант – 0,1 М NaNO2
Индикатор – внутренний (тропеолин 00)
внешний (йодкрахмальная бумага)
Без индикатора – потенциометрически
Реакция титрования (новокаин, анестезин):
Слайд 19
Дикаин, являясь вторичным амином, образует нитрозосоединение:
Слайд 20
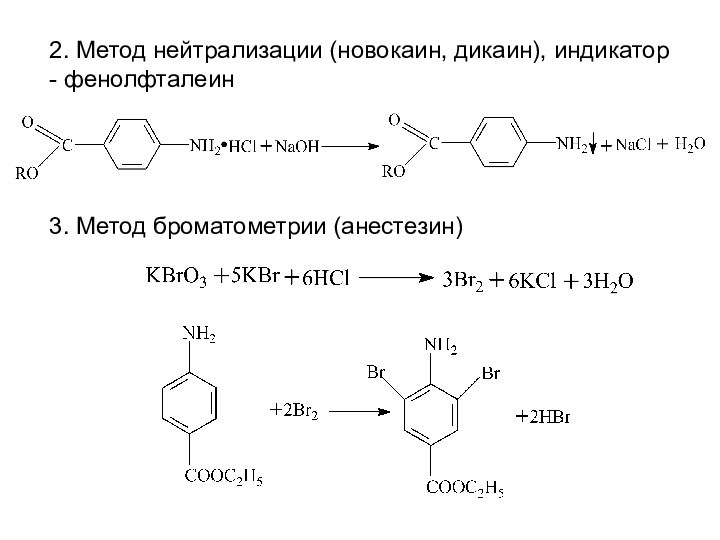
2. Метод нейтрализации (новокаин, дикаин), индикатор - фенолфталеин
3.
Метод броматометрии (анестезин)
Слайд 21
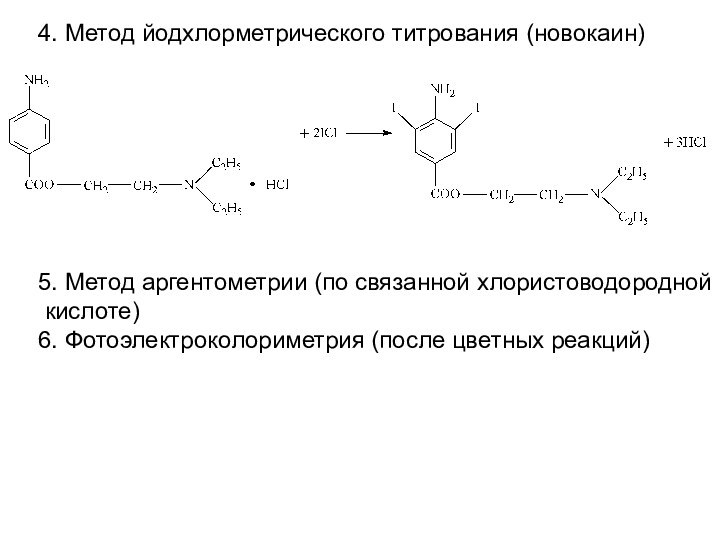
4. Метод йодхлорметрического титрования (новокаин)
5. Метод аргентометрии (по
связанной хлористоводородной
кислоте)
6. Фотоэлектроколориметрия (после цветных реакций)
Слайд 22
ХРАНЕНИЕ
Анестезин, новокаин хранят в хорошо укупоренной таре, предохраняющей
от действия света (в банках из оранжевого стекла). Дикаин
хранят по правилам хранения веществ списка А в хорошо укупоренной таре. При несоблюдении условий хранения происходит постепенный гидролиз.
Слайд 23
ПРИМЕНЕНИЕ
Местноанестезирующие средства.
Анестезин назначают внутрь по 0,25− 0,3 г
в виде таблеток, порошков.
Новокаин широко применяют для инфильтрационной и
спинно-мозговой анестезии в виде 0,25−0,5%-ных водных растворов.
Дикаин активнее новокаина, но токсичнее его в 10 раз, применяют для поверхностной анестезии в глазной и оториноларингологической практике в виде 0,5−2%-ных растворов, а также для перидуральной анестезии в виде 0,3%-ных растворов в изотоническом растворе.
Слайд 24
ПРОИЗВОДНЫЕ АМИДА ПАБК
Novocainamid
Новокаинамид
МНН Прокаинамида гидрохлорид
β-диэтиламиноэтиламида n-амино-бензойной кислоты гидрохлорид
Белый
или белый со слегка кремоватым оттенком кристаллический порошок без
запаха. Тпл. 165-1690С.
Очень легко растворим в воде, легко – в спирте, мало – в хлороформе, практически нерастворим в эфире.
Слайд 25
МЕТОДЫ ОПРЕДЕЛЕНИЯ ПОДЛИННОСТИ
ИК-спектроскопия
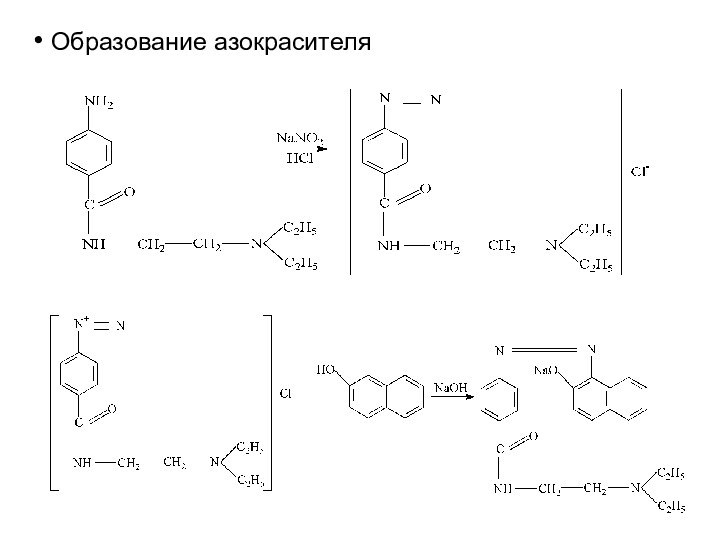
Образование азокрасителя
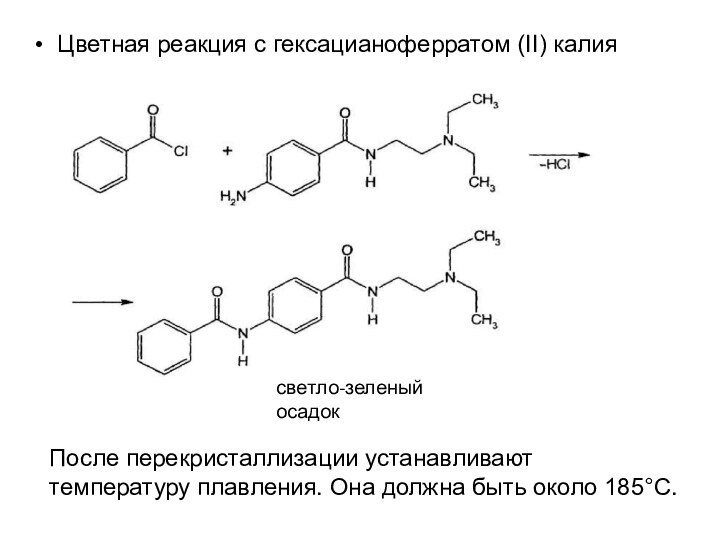
Цветная реакция с гексацианоферратом (II)
калия
Реакция обнаружения хлорид-иона
Общеалкалоидные реакции
Слайд 27
Цветная реакция с гексацианоферратом (II) калия
светло-зеленый осадок
После
перекристаллизации устанавливают температуру плавления. Она должна быть около 185°С.
Слайд 28
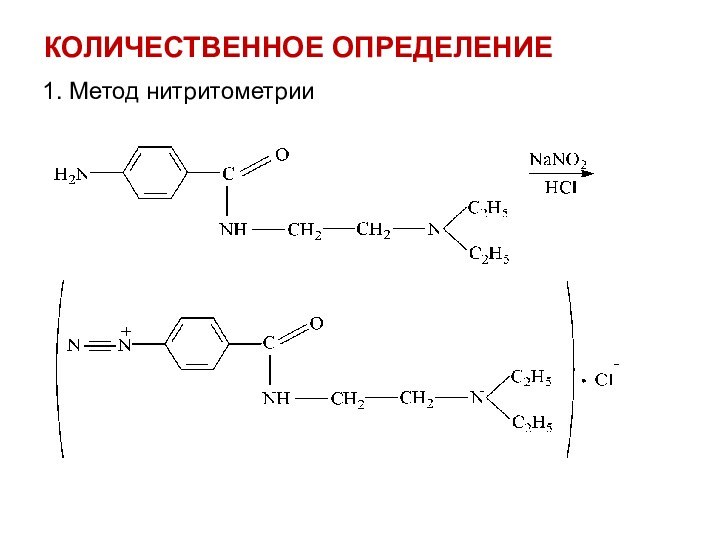
1. Метод нитритометрии
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ
Слайд 29
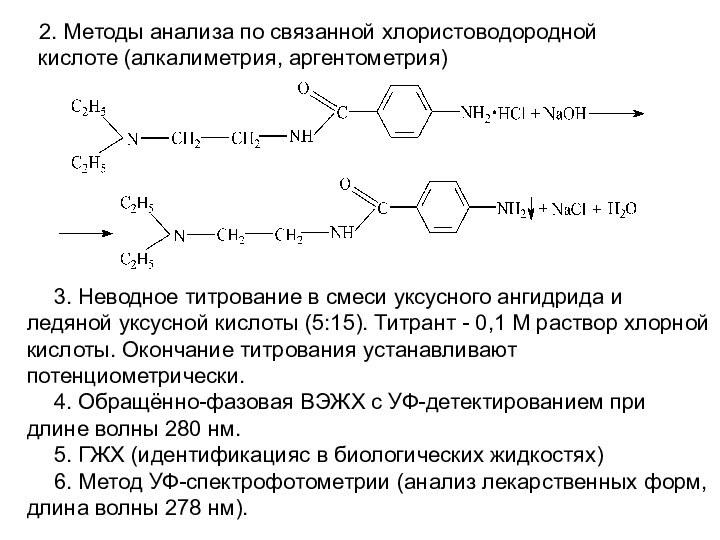
2. Методы анализа по связанной хлористоводородной кислоте (алкалиметрия,
аргентометрия)
3. Неводное титрование в смеси уксусного ангидрида и ледяной
уксусной кислоты (5:15). Титрант - 0,1 М раствор хлорной кислоты. Окончание титрования устанавливают потенциометрически.
4. Обращённо-фазовая ВЭЖХ с УФ-детектированием при длине волны 280 нм.
5. ГЖХ (идентификацияс в биологических жидкостях)
6. Метод УФ-спектрофотометрии (анализ лекарственных форм, длина волны 278 нм).
Слайд 30
ХРАНЕНИЕ И ПРИМЕНЕНИЕ
В хорошо укупоренной таре, в
сухом, защищенном от света месте, чтобы не допустить гидролиза.
Даже в отсутствие света постепенно разрушается во влажной атмосфере; при повышении температуры процесс гидролиза ускоряется.
Прокаинамида гидрохлорид относится к антиаритмическим средствам. Назначают при расстройствах сердечного ритма в виде таблеток по 0,5-1,0 или в вену по 5-10 мл 10%-ного раствора.
Слайд 31
ПРОИЗВОДНЫЕ n-АМИНОСАЛИЦИЛОВОЙ КИСЛОТЫ
Natrii para-aminosalicylas
Натрия пара-аминосалицилат
Белый или белый со
слегка желтоватым или розоватым оттенком мелкокристаллический порошок.
Легко растворим в
воде, трудно - в спирте.
натриевая соль n-аминосалициловой кислоты
Слайд 32
ПОДЛИННОСТЬ
УФ-спектроскопия
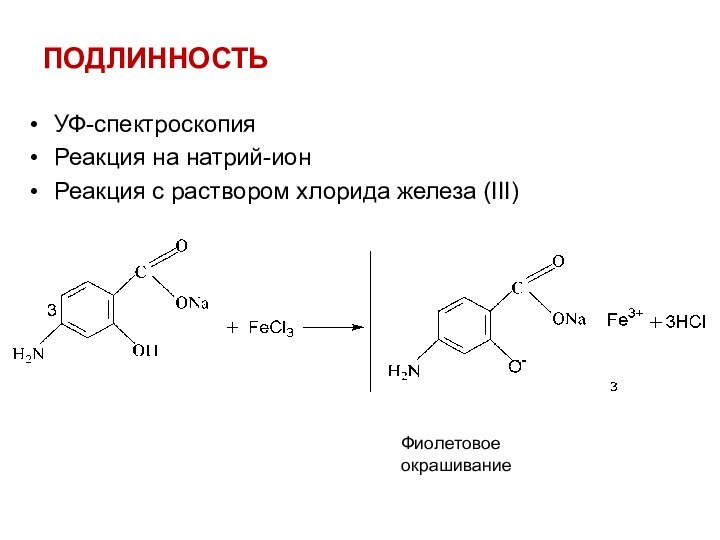
Реакция на натрий-ион
Реакция с раствором хлорида железа (III)
Фиолетовое окрашивание
Слайд 33
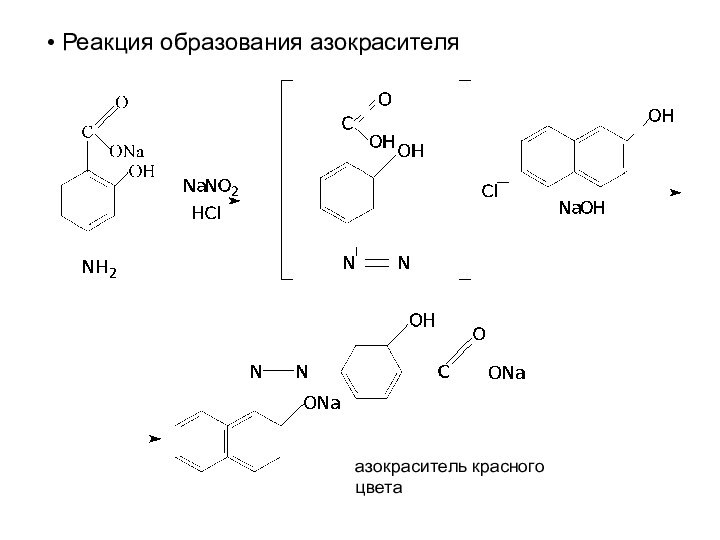
Реакция образования азокрасителя
азокраситель красного цвета
Слайд 34
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ
1. Метод нитритометрии с внешним индикатором (йодкрахмальной
бумагой) - ГФ X
Нефармакопейные методы:
2. метод нейтрализации
3. обратная аргентометрия
4.
Броматометрия, Йодхлорометрия
(аналогично определению производных n-аминобензойной кислоты)
5. Спектрофотометрия при длине волны 265 нм (растворитель вода).
Слайд 35
ХРАНЕНИЕ И ПРИМЕНЕНИЕ
Препарат хранят в хорошо укупоренной таре,
предохраняющей от действия света, в сухом, защищенном от света
месте, чтобы не допустить образования примесей продуктов разложения.
Натрия n-аминосалицилат применяют в качестве противотуберкулезных средств. Назначают препарат для лечения различных форм туберкулеза по 2,0−3,0 г.
Слайд 36
Лекарственные вещества, производные ароматического амина - анилина
Слайд 37
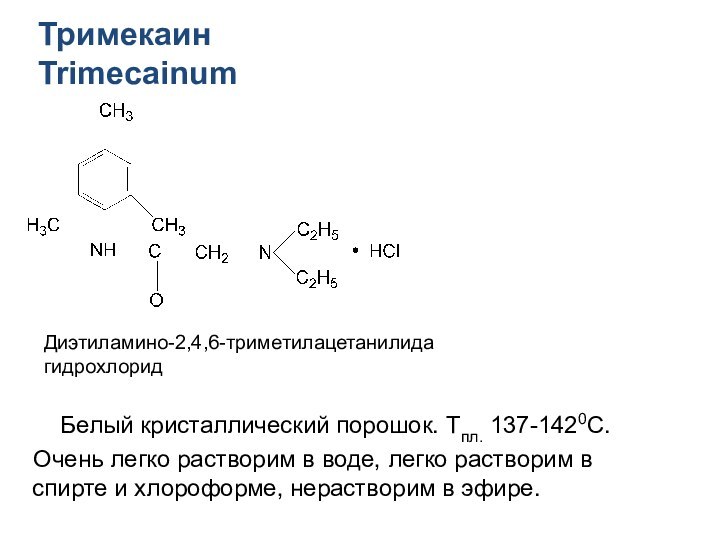
Тримекаин
Trimecainum
Белый кристаллический порошок. Тпл. 137-1420С.
Очень легко растворим в
воде, легко растворим в спирте и хлороформе, нерастворим в
эфире.
Диэтиламино-2,4,6-триметилацетанилида гидрохлорид
Слайд 38
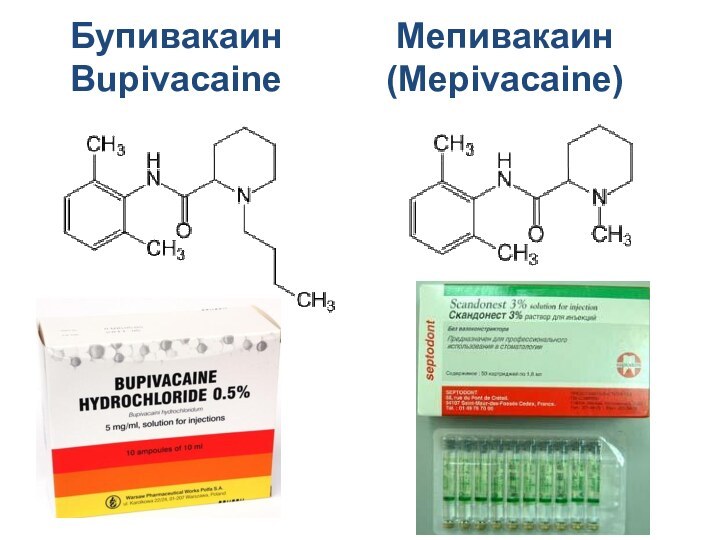
Бупивакаин
Bupivacaine
Мепивакаин (Mepivacaine)
Слайд 40
ПОДЛИННОСТЬ
ИК-спектроскопия
УФ-спектроскопия (в области 250-300 нм имеет максимумы
поглощения при 262,5 нм и при 271 нм, минимум
поглощения - при 255 нм.
Положительная реакция на хлорид-ион.
Окисление тримекаина при нагревании до 155-165ºС (масляная баня) в смеси сульфата меди (II) и конц. серной кислоты. После охлаждения смеси и добавления раствора аммиака появляется синее окрашивание, а при УФ-облучении наблюдается красно-розовая флуоресценция (отличие от других местноанестезирующих средств).
Слайд 41
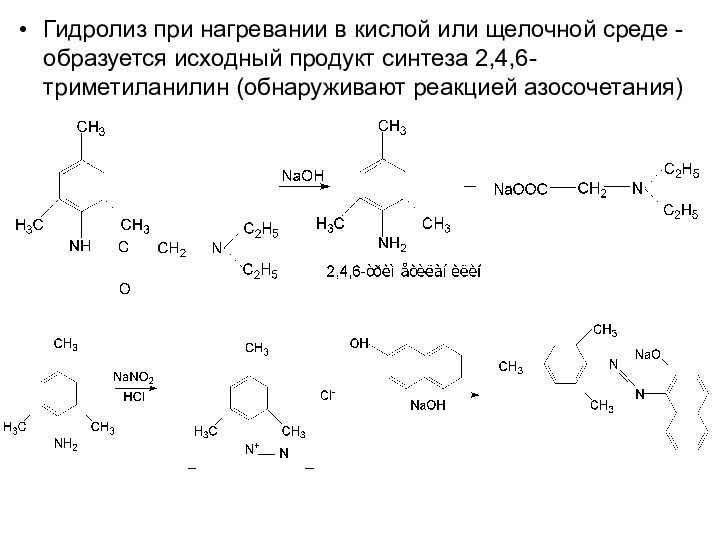
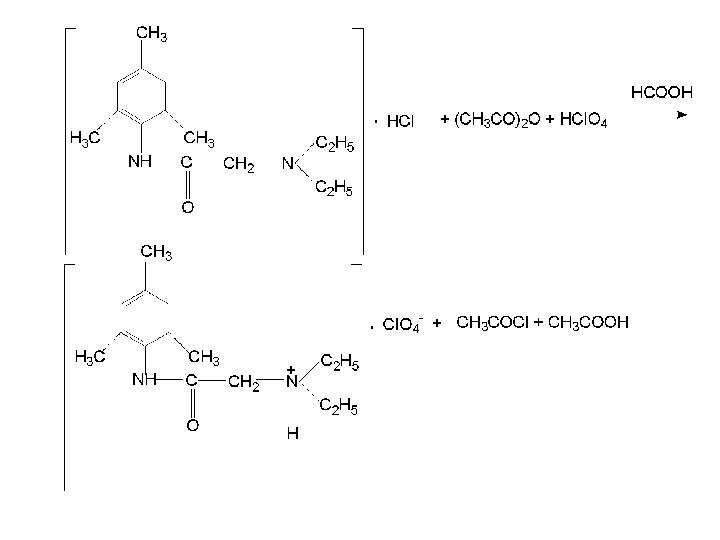
Гидролиз при нагревании в кислой или щелочной среде
- образуется исходный продукт синтеза 2,4,6-триметиланилин (обнаруживают реакцией азосочетания)
Слайд 42
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ
Метод неводного титрования
Среда – смесь муравьиной
кислоты и уксусного ангидрида (для связывания хлористоводородной кислоты)
Титрант -
0,1 н. раствор хлорной кислоты
Индикатор - кристаллический фиолетовый
2. Нейтрализация спиртовых растворов (индикатор фенолфталеин)
3. Аргентометрия (по связанной хлористоводородной кислоте).
4. Инструментальные методы – ГЖХ с пламенно-ионизационным детектором, ВЭЖХ
Слайд 44
ХРАНЕНИЕ И ПРИМЕНЕНИЕ
Лидокаин, тримекаин, бупивакаин хранят в сухим
месте, в плотно укупоренной таре, предохраняющей от действия света,
при комнатной температуре. Во влажной атмосфере и при повышении температуры разрушаются.
Тримекаин и лидокаин применяют в качестве местноанестезирующих средств для инфильтрационной (0,25-0,5%-ные растворы) и проводниковой (1-2%-ные растворы) анестезии.
Бупивакаин – местноанестезирующее средство длительного действия (0,25-0,5% растворы для инъекций)
Тримекаин входит в состав комбинированных мягких лекарственных форм – «Левосин», «Гиоксизоль».
Слайд 45
ПРЕПАРАТЫ, ПРОИЗВОДНЫЕ n-АМИНОФЕНОЛА
Парацетамол
Paracetamolum
Белый или белый с кремоватым или
розоватым оттенком кристаллический порошок без запаха. Температура плавления 168-172
ºС
Трудно растворим в воде, легко – в спирте, растворим в ацетоне и растворах едких щелочей, практически нерастворим в эфире
Слайд 46
ПРЕДПОСЫЛКИ СОЗДАНИЯ ПАРАЦЕТАМОЛА
Производные n-аминофенола в основе химической структуры
содержат молекулу анилина.
Анилин, являясь очень токсичным метгемоглобинобразующим веществом,
вместе с тем обладает способностью снижать температуру тела.
В качестве жаропонижающего средства применялся ацетилированный анилин – антифебрин (имеет меньшую токсичность, но при длительном применении также вызывает отравление).
В результате гидролиза антифебрина образуется анилин , который окисляется в организме до n-аминофенола (менее токсичен и сравнительно легко выводится из организма)
На основе изучения фармакологического действия производных n-аминофенола был синтезирован малотоксичный препарат парацетамол
Слайд 47
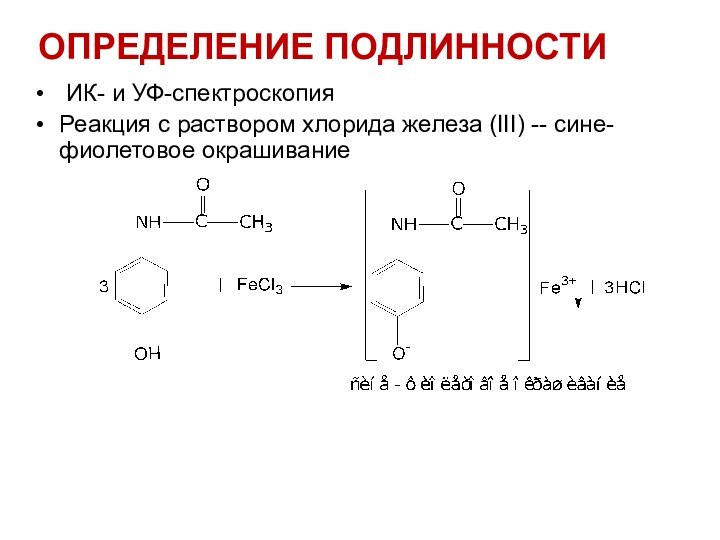
ОПРЕДЕЛЕНИЕ ПОДЛИННОСТИ
ИК- и УФ-спектроскопия
Реакция с раствором
хлорида железа (III) -- сине-фиолетовое окрашивание
Слайд 48
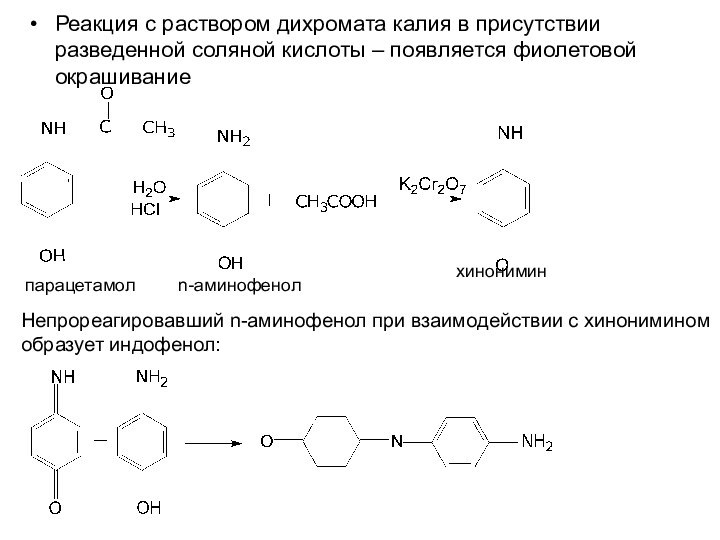
Реакция с раствором дихромата калия в присутствии разведенной
соляной кислоты – появляется фиолетовой окрашивание
парацетамол n-аминофенол
хинонимин
Непрореагировавший n-аминофенол при взаимодействии
с хинонимином образует индофенол:
Слайд 49
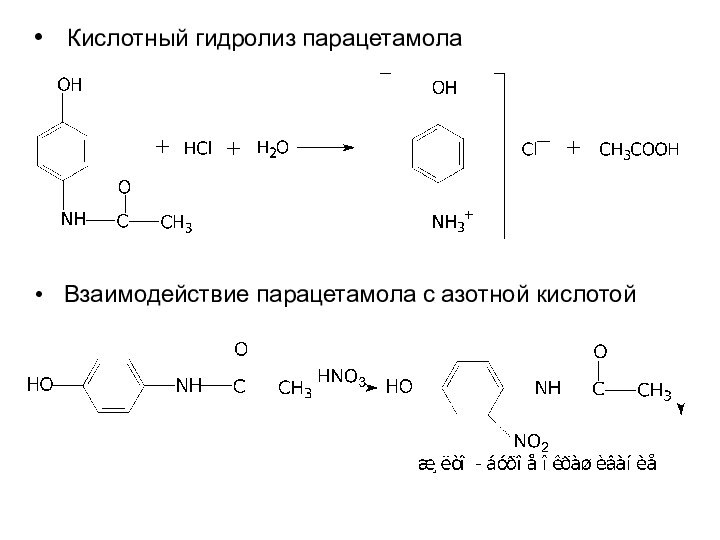
Кислотный гидролиз парацетамола
Взаимодействие парацетамола
с азотной кислотой
Слайд 50
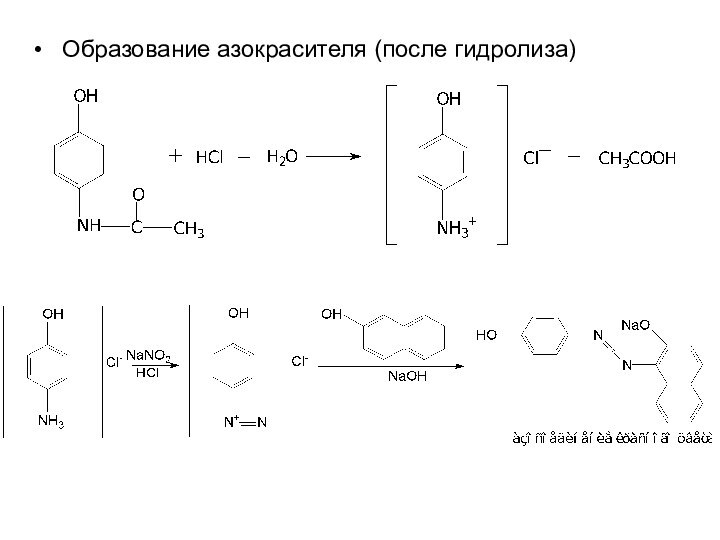
Образование азокрасителя (после гидролиза)
Слайд 51
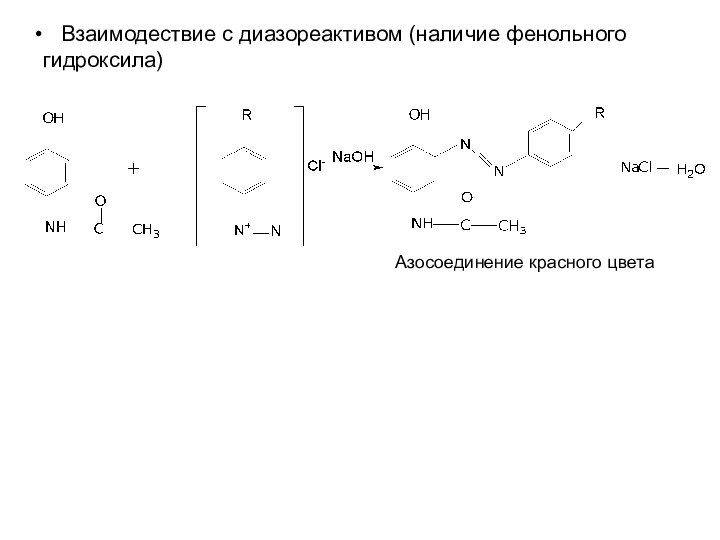
Взаимодествие с диазореактивом (наличие фенольного гидроксила)
Азосоединение
красного цвета
Слайд 52
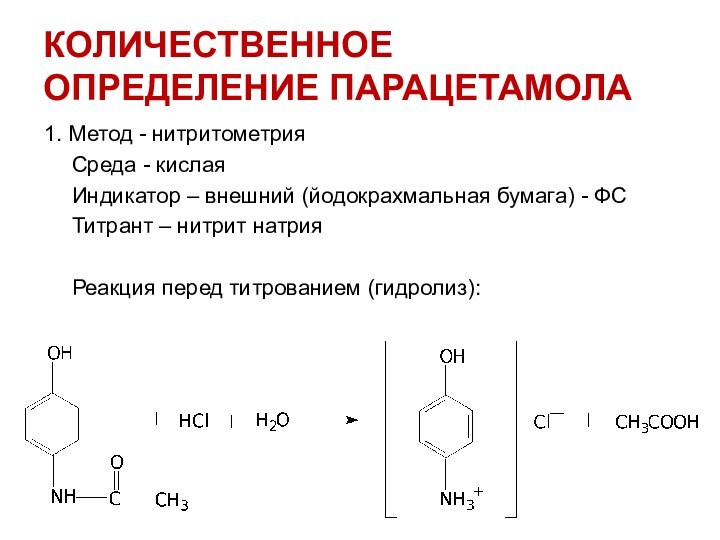
КОЛИЧЕСТВЕННОЕ ОПРЕДЕЛЕНИЕ ПАРАЦЕТАМОЛА
1. метод - нитритометрия
Среда - кислая
Индикатор
– внешний (йодокрахмальная бумага) - ФС
Титрант – нитрит натрия
Реакция
перед титрованием (гидролиз):
Слайд 53
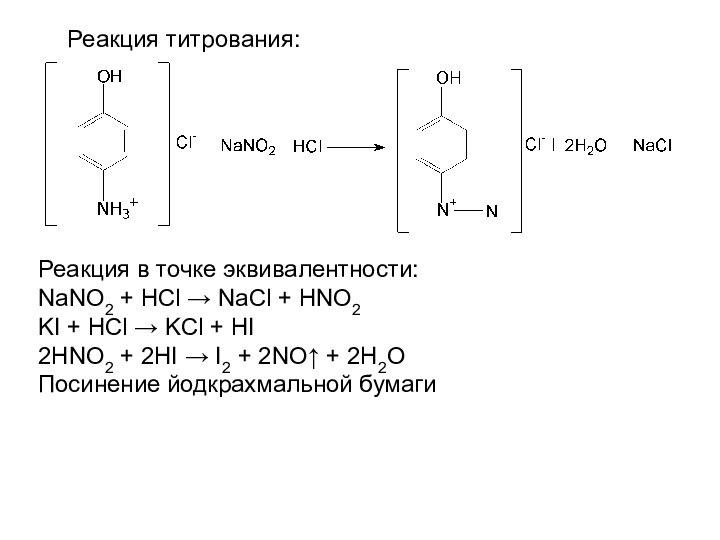
Реакция в точке эквивалентности:
NaNO2 + HCl → NaCl
+ HNO2
KI + HCl → KCl + HI
2HNO2 +
2HI → I2 + 2NO↑ + 2H2O
Посинение йодкрахмальной бумаги
Реакция титрования:
Слайд 54
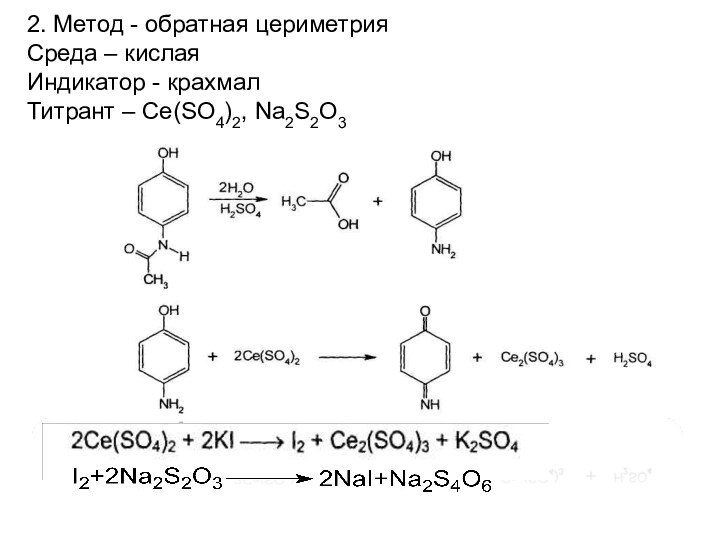
2. Метод - обратная цериметрия
Среда – кислая
Индикатор -
крахмал
Титрант – Ce(SO4)2, Na2S2O3