Слайд 2
Спортивная физиология
Физиология физической культуры и спорта - это
специальный раздел физиологии человека, изучающий изменения функций организма и
их механизмы под влиянием мышечной (спортивной) деятельности и обосновывающий практические мероприятия по повышению ее эффективности.
Спортивная физиология имеет 2 раздела: общий и частный.
Слайд 5
Спортивная физиология
Решает 2 проблемы:
Для массовых форм физической культуры:
Физиологическое
обоснование закономерностей укрепления здоровья человека с помощью физических упражнений
для повышения устойчивости организма к действию различных неблагоприятных факторов внешней среды (температура, давление, инфекции и пр.);
Сохранение и восстановление работоспособности, препятствие развитию раннего утомления в процессе трудовой деятельности;
Слайд 6
Для спортсменов:
Физиологическое обоснование мероприятий, направленных на достижение высоких
спортивных результатов без ухудшения состояния здоровья
Слайд 8
Спортивная физиология
Особенность СФ – получение материалов для изучения
только из экспериментов с человеком: сравнительное изучение функционального состояния
организма до, во время и после двигательной активности (используя нагрузочные тесты и современные методы исследования).
Слайд 9
Спортивная физиология
Основные методы исследования
Метод наблюдения;
Эксперимента (экспериментальные методы);
Слайд 10
Спортивная физиология
Использует современные методы исследования:
регистрация электрических потенциалов
головного мозга (электроэнцефалография),
сердца (электрокардиография),
скелетной мускулатуры (электромиография);
УЗИ
(ультразвуковые методы исследования);
КТ (рентгеновская компьютерная томография);
МРТ (магнитно-резонансная томография);
используется оптическая, радиотехническая и электронная аппаратура;
математическое моделирование и др. методы
Слайд 11
БИОХИМИЯ
Биохи́мия (биологи́ческая, или физиологи́ческая хи́мия) — наука о химическом составе живых клеток и организмов и о
химических процессах, лежащих в основе их жизнедеятельности.
Термин «биохимия»
был предложен и введён в научную среду в 1903 г. немецким химиком Карлом Нойбергом.
Биохимия находится на стыке нескольких наук, прежде всего — биологии и химии.
Слайд 12
БИОХИМИЯ
Биохимии чуть больше 100 лет.
Возникла как наука
о химии жизни в конце XIX века на основании
развития органической химии;
Отличается от нее тем, что исследует вещества и химические реакции только в живых организмах (прежде всего в живой клетке);
Бурное развитие биохимия получила во второй половине 20 века.
Слайд 13
БИОХИМИЯ
В зависимости от объекта исследования выделяют:
биохимию животных
и человека;
биохимию растений и микроорганизмов.
Биохимия человека делится на:
1.Общую
биохимию (статическую и динамическую).Она изучает:
- структуру и свойства химических соединений, входящих в состав живых организмов;
- химические реакции, происходящие в процессе обмена веществ;
Слайд 14
БИОХИМИЯ
2.Функциональную биохимию. Она изучает связь между обменом веществ
и функциями организма.
К этому разделу относится и биохимия
ФКиС.
Слайд 15
БИОХИМИЯ ФКиС
Знание биохимии необходимо для специалиста получающего высшее
физкультурное образование, т.к. она:
- раскрывает законы жизнедеятельности организмов на
молекулярном уровне;
- устанавливает причинно-следственные связи процессов, происходящих в организме;
Слайд 16
- изучает особенности биохимических превращений при мышечной деятельности;
-
раскрывает биохимические принципы спортивной тренировки и повышения работоспособности;
- говорит
о биохимическом контроле в спорте (допинг-контроль и др. вопросы).
Слайд 17
Методы биохимических исследований
В биохимии в основе изучения структуры
и свойств живого вещества лежит его разделение на отдельные
компоненты и их последующий анализ;
Методы биохимии преимущественно формировались в XX веке;
Наиболее распространенными являются:
- хроматография, изобретённая М. С. Цветом в 1906 г.;
- центрифугирование (Т. Сведберг, 1923 г., Нобелевская премия по химии 1926 г.);
- электрофорез (А. Тизелиус, 1937 г., Нобелевская премия по химии 1948 г.);
- спектральные методы исследования.
Слайд 18
Методы биохимических исследований
Генетические методы исследования – все шире
применяются с конца ХХ в.(взяты из молекулярной и клеточной биологии: искусственная экспрессия
и нокаут генов в модельных клетках и целых организмах); Выделилось отдельное направление биохимии – функциональная геномика.
Комьютерное моделирование. Эта методика позволяет исследовать свойства биомолекул там, где невозможно провести прямой эксперимент. Методика основана на компьютерных программах, которые позволяют визуализировать структуру биомолекул, задать их предполагаемые свойства и наблюдать реакции между молекулами.
Слайд 19
хроматография
Хроматография [гр. сhrömatos − цвет + graphö −
пишу] — метод разделения, анализа и физико-химических исследований веществ и
их смесей. Разделяемые вещества распределяются между двумя несмешивающимися фазами (в зависимости от их относительной растворимости в каждой фазе): подвижной и неподвижной. Неподвижная - твердая фаза или жидкость, связанная на инертном носителе; подвижная - газовая или жидкая фаза (элюент).
С середины XX века и до наших дней хроматография интенсивно развивалась и стала одним из наиболее широко применяемых аналитических методов.
Слайд 20
хроматография
Существует множество разновидностей этого метода.
За создание метода распределительной
хроматографии Дж. Мартину и Р. Сингу была присуждена Нобелевская премия
по химии (1952г., открытие метода –1941г.).
Слайд 21
По агрегатному состоянию фаз
Газовая хроматография
Газо-жидкостная хроматография
Газо-твёрдофазная хроматография
Жидкостная
хроматография
Жидкостно-жидкостная хроматография
Жидкостно-твёрдофазная хроматография
Жидкостно-гелевая хроматография
Сверхкритическая флюидная хроматография
По рабочему давлению
Хроматография низкого
давления (FPLC)
Хроматография высокого давления (HPLC)
Хроматография ультравысокого давления (UHPLC)
По механизму взаимодействия
Распределительная хроматография
Ионообменная хроматография
Адсорбционная хроматография
Эксклюзионная хроматография
Аффинная хроматография
Осадочная хроматография
Адсорбционно-комплексообразовательная хроматография
Слайд 22
Михаил Семёнович Цвет (1872-1919)
Слайд 23
Замечательный русский ботаник Михаил Семёнович Цвет известен своими
исследованиями хлорофилла. Изучая который он создал новый метод адсорбционного
хроматографического анализа, открывшего широчайшие возможности для тонкого химического исследования (Варшава, 1910г.).
Метод осуществляет заветную мечту химиков - разделить смесь на компоненты до её анализа.
Он даёт возможность открыть искомое вещество в смеси многих родственных химических веществ там, где обычные химические методы оказываются совершенно бессильными.
Слайд 24
В силу исторической случайности адсорбционный метод хроматографического анализа
был в забвении почти 30 лет.
Лишь начиная примерно
с 1931 г., метод М. С. Цвета стал находить всё более и более растущее применение во многих областях науки.
Сейчас этот метод признан по своему значению совершенно исключительным.
На основе его возникла обширная химия каротиноидов, развёртываются работы большой практической важности по исследованию пигментов жёлчи и порфиринов; исследуются физиологически важные пигменты - флавины и т. д. Метод Цвета применяется при контроле продуктов и товаров. В будущем он найдёт ещё и другие важные применения.
Слайд 25
хроматография
По экспертным оценкам, хроматография относится к 20 выдающимся
открытиям прошедшего столетия, которые в наибольшей степени преобразовали науку,
а через нее определили уровень развития техники и промышленности, цивилизации в целом.
Хотя по образованию и роду занятий Цвет был ботаником, результаты его открытия столь значимы для всех естественных наук, что Федерация европейских химических обществ, приводит имя Цвета, наряду с четырьмя другими русскими именами - Ломоносова, Менделеева, Бутлерова и Семенова, - в числе ста выдающихся химиков прошлого.
Слайд 26
В конце своего 100-летия хроматография представляет собой:
самый распространенный
и совершенный метод разделения смесей атомов, изотопов, молекул, всех
типов изомерных молекул, включая и оптические изомеры, макромолекул (синтетических полимеров и биополимеров), ионов, устойчивых свободных радикалов, комплексов, ассоциатов, микрочастиц;
уникальный метод качественного и количественного анализа сложных многокомпонентных смесей:
самостоятельное научное направление и важный физико-химический метод исследования и измерения;
препаративный и промышленный метод выделения веществ в чистом виде;
мощную отрасль научного приборостроения.
Слайд 27
Ни один аналитический метод не может конкурировать с
хроматографией по универсальности применения и эффективности разделения самых сложных
многокомпонентных смесей.
На современных газохроматографических капиллярных колонках в одном эксперименте могут быть разделены, количественно и качественно определены более 1000 белков или пептидов;
Только благодаря сочетанию разнообразных методов хроматографии и капиллярного электрофореза стала возможной расшифровка нуклеотидной последовательности ДНК и завершение работ по программе "Геном человека".
Слайд 28
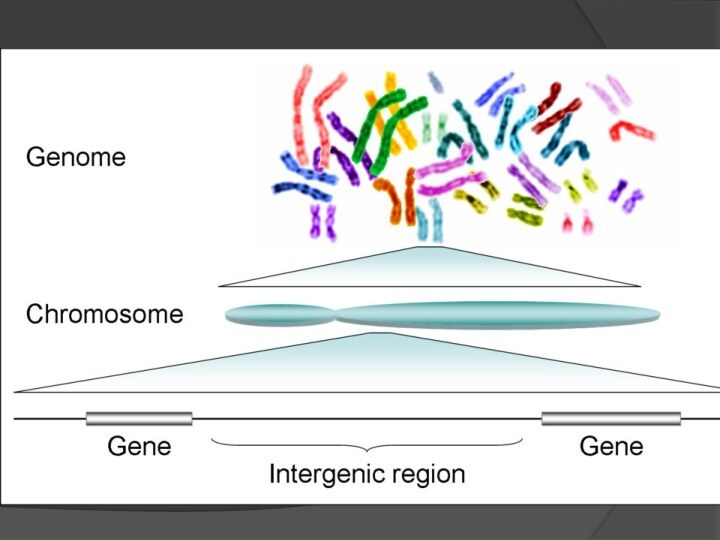
ГЕНОМ ЧЕЛОВЕКА
Геном человека — совокупность наследственного
материала, заключенного в клетке человека;
Человеческий геном
состоит из 23 пар хромосом, находящихся в ядре (а также митохондриальной ДНК):
- двадцать две пары аутосом;
- одна пару половых хромосом (ХY или XX)
(вместе они содержат примерно 3,1 млрд пар оснований).
Слайд 29
В ходе выполнения проекта «Геном человека» была определена
последовательность ДНК всех хромосом и митохондриальной ДНК (закончен в
2000 -2003гг, начат – в 1990г.).
В настоящее время эти данные активно используются по всему миру в биомедицинских исследованиях.
Выявлено, что человеческий геном содержит 20—25 тыс. активных генов, что значительно меньше, чем ожидалось в начале проекта (порядка 100 тыс.) — то есть только 1,5 % всего генетического материала кодирует белки или функциональные РНК. Остальная часть является некодирующей ДНК, которую часто называют мусорной ДНК.
Слайд 30
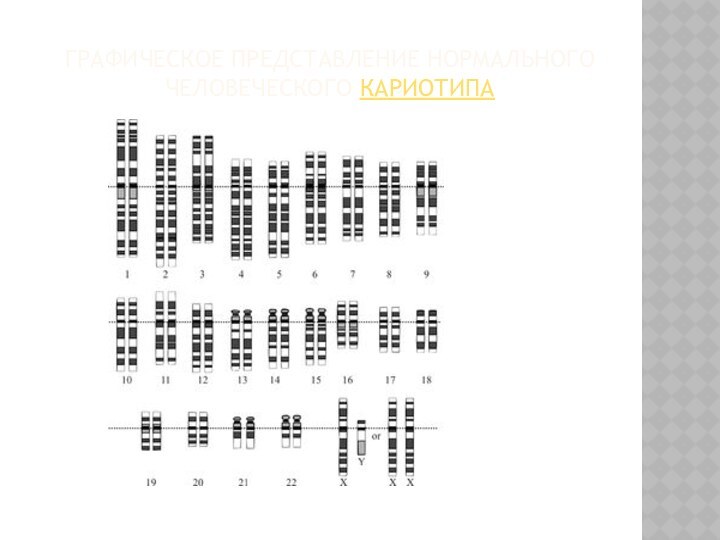
Графическое представление нормального человеческого кариотипа
Слайд 32
ФЕРМЕНТЫ
1. Понятие. Биологическая роль.
2. Особенности строения.
3. Принцип действия
и активность ферментов.
4. Методы выделения.
5. Классификация и область применения.
Слайд 33
Ферменты (от лат. fermentum – брожение, закваска) –
органические вещества белковой природы, которые синтезируются в клетках, во
много раз ускоряют протекающие в них реакции, не подвергаясь при этом химическим превращениям.
Слайд 34
1. Понятие. Биологическая роль.
Термин «фермент» предложил химик Ван
Гельмонт, изучая пищеварение, 17 век.
Луи Пастер (19 век) был
близок к открытию ферментов, изучая брожение.
Только в 1926г. был выделен первый фермент (уреаза) - американским биохимиком Д. Самнером.
Слайд 35
1. Понятие. Биологическая роль.
В настоящее время известно
более 3000 ферментов.
Они играют важнейшую роль в процессах жизнедеятельности,
регулируя обмен веществ.
Слайд 36
2. Особенности строения
Выделяют:
- однокомпонентные ферменты (простые белки);
- двухкомпонентные
(сложные белки) – в составе фермента кроме белковой части
есть группа небелковой природы – кофермент.
Слайд 37
2. Особенности строения
В качестве коферментов выступают большинство витаминов:
Е, К, В1, В2, В6, В12, С, Н, и
др.
В двухкомпонентных ферментах белковая часть и добавочная группа по отдельности не имеют каталитической активности, а только в комплексе.
Слайд 38
2. Особенности строения
Для выполнения своих функций в молекуле
фермента выделяют разные участки:
- каталитический центр;
- субстратный центр;
- аллостерический
центр.
Первые два объединяют в активный центр фермента.
Каталитической активностью белки-ферменты обладают при наличии третичной структуры.
Слайд 39
4. Принцип действия
Вещество (субстрат) присоединяется к ферменту.
Он ускоряет
разрыв одних химических связей и создание других.
Продукт реакции отсоединяется
от фермента.
Фермент не тратится и готов начать новую реакцию.
Слайд 40
4. Активность ферментов
На активность ферментов и на скорость
реакции катализа влияют:
- концентрация и доступность субстрата;
- концентрация фермента;
-
температура реакции;
- pH реакции;
- наличие ингибиторов (медь, железо, кальций) или активаторов (некоторые ионы).
Слайд 41
Отличия ферментов от неорганических катализаторов
- работают в физиологически
нормальных условиях для организма;
- катализируют только определенные биохимические реакции;
-
эти реакции идут последовательно (продукт реакции одного – субстрат для следующего);
- высокая скорость фермент. реакций (ускоряют в 100 -1000 раз);
- 100% выход реакции без побочных продуктов.
Слайд 42
3. Методы выделения ферментов
Вначале ткань (материал) измельчают до
кашицы (гомогената) и используют:
- осаждение белка органич. растворителями;
- высаливание;
-
электрофорез;
- ионообменную или аффинную хроматографию;
- центрифугирование;
- гельфильтрацию;
- избирательную денатурацию и др.
Слайд 43
4. Классификация
С 1961г. ферменты разделяют по типу катализируемой
ими реакции на 6 групп (классов):
- оксидоредуктазы;
- трансферазы;
- гидролазы;
-
лиазы;
- изомеразы;
- лигазы.
Слайд 44
Для каждого фермента также разработан шифр (шифровая классификация)
Это
4 числа, разделенные точками.
Слайд 45
Например, глюкозоксидазе присвоен шифр КФ 1.1.3.4, что означает:
КФ 1 — Оксидоредуктазы
КФ 1.1 — Алкогольоксидоредуктазы
КФ 1.1.3 —
Оксидоредуктазы, окисляющие группу CH-OH и восстанавливающие кислород
КФ 1.1.3.4 — Оксидоредуктазы, окисляющие глюкозу в
присутствии кислорода
КФ – классификационный номер.
Всего известно 3 глюкозоксидазы из разных организмов.
Слайд 46
Область применения
В таких отраслях как:
хлебопечение, пивоварение, виноделие;
производство
сыра, соков, кофе;
для обработки мяса в кулинарии;
в чайном, кожевенном
и меховом производстве;
в пр-ве моющих средств и бумаги;
в текстильной и фармацевтической промышленности (фестал, мезим-форте);
в кормах для животных.
Слайд 47
Г О Р М О Н Ы
«Мы
такие, какими нас делают гормоны».
Они определяют наши физические и
психические особенности в течение всей жизни, оказывая влияние на:
- рост и половое развитие;
- желания и поведение;
- обмен веществ;
- мышечную силу;
- остроту ума и сон.
Слайд 48
гормоны
Это специфические биологически активные вещества, вырабатываемые ЖВС, и
оказывающие значительное влияние на физиологические процессы.
ЖВС не имеют
выводных протоков и свои гормоны выделяют прямо в кровь - гуморальная регуляция;
Но все процессы в организме контролирует и НС.
Поэтому говорят о нейро-гуморальной регуляции.
Слайд 49
Ж В С
К ЖВС относятся:
- гипофиз;
- эпифиз (шишковидная
железа);
- вилочковая железа (ТИМУС);
- щитовидная и паращитовидные железы;
-
надпочечники;
- поджелудочная железа;
- половые железы.
Слайд 50
ГОРМОНЫ
Термин «гормон» предложили У. Бейлисс, Э. Старлинг в
1905г. (от греч. hormaino – побуждаю, привожу в движение).
В настоящее время описано более 150 гормонов человека, животных и растений.
Слайд 51
классификация
По химической природе выделяют 3 группы гормонов:
- пептидные
гормоны;
- производные аминокислот;
- стероидные гормоны.
Слайд 52
Пептидные гормоны
Это гормоны, синтезируемые:
- в гипофизе и гипоталамусе
(в ГМ – гормон роста, вазопрессин, окситоцин и др.
– в т.ч. эндорфины);
- в поджелудочной железе (инсулин и глюкагон);
- в ЩЖ (кальцитонин);
- в паращитовидных железах (парат-гормон).
Слайд 53
Производные аминокислот
Это гормоны, осинтезируемые:
- в надпочечниках (адреналин и
норадреналин);
- в эпифизе (мелатонин);
- в ЩЖ (тироксин и трийодтиронин).
Слайд 54
Стероидные гормоны
Синтезируются в коре надпочечников и половых железах
из холестерина: это мужские (тестостерон) и женские (эстрогены) половые
гормоны.
Слайд 55
Механизм действия гормонов
Существует 2 сложных механизма действия:
- гормон
взаимодействует с белками-рецепторами на поверхности клеточных мембран (клеток-мишеней, активируя
фермент аденилатциклазу);
- проникает внутрь клетки и связывается в ее цитоплазме с белками-рецепторами (далее взаимодействуя с ядерной ДНК).
Слайд 56
Свойства гормонов
1. Строгая специфичность действия (один гормон нельзя
заменить другим);
2. Высокая биологическая активность (действуют в очень малых
концентрациях);
3. Дистантный характер действия (образуются далеко от своей цели);
4. Эффект гормона зависит от его дозы (норма, гипо- и гиперфункция);
5. Быстро разрушаются в тканях;
Слайд 57
Свойства гормонов
6. Нет видовой специфичности (одинаково действуют у
человека и животных);
7. Имеют небольшую молекулярную массу (легко проникают
в клетки);
8. Пролонгированность действия.
Слайд 58
ВИТАМИНЫ
Слово «витамин» вошло в лексикон в начале 20
века.
Предположение о их существовании и необходимости для роста и
развития животных и человека сделал русский врач Н.И. Лунин в 1888г.
Впервые выделил (из рисовых отрубей) поляк К. Функ в 1912г. и дал название «витамин» («вита» – жизнь; «амин» - содержащий азот).
Слайд 59
ВИТАМИНЫ
Витамины – группа низкомолекулярных органических веществ различной химической
природы, обладающих высокой биологической активностью и необходимых для роста
и развития организма.
Слайд 60
ВИТАМИНЫ
- содержатся в пище в незначительных количествах;
- не
синтезируются в нашем организме, либо в небольшом кол-ве микрофлорой
кишечника;
- не выполняют пластической функции;
- не являются источником энергии;
- играют роль коферментов;
Слайд 61
ВИТАМИНЫ
- оказывают действие в малых концентрациях;
- влияют на
все обменные процессы;
- суточная потребность составляет от нескольких мкг
до нескольких мг.
Вреден как недостаток, так и избыток витаминов (авитаминоз; гиповитаминоз; гипервитаминоз).
Слайд 62
КЛАССИФИКАЦИЯ
1. Витамины обозначают буквами латинского алфавита (с нижним
цифровым индексом): А; В; С; Е и др.
2. Названия
отражают химическую природу и функцию витамина (С – антискорбутный; К – антигеморра-гический и др.).
Слайд 63
КЛАССИФИКАЦИЯ
Делятся на 2 группы:
I. Водорастворимые
II.
Жирорастворимые
Выделяют еще витаминоподобные вещества.
Слайд 64
I. Водорастворимые
В1 – антиневритный;
В2 – антидерматитный;
В3 – пантотеновая
кислота;
В6 – пиридоксин;
В9 – фолиевая кислота;
В12 – цианкобаламин;
РР –
никотиновая кислота (ниацин);
Н – биотин;
С – аскорбиновая кислота.
Слайд 65
II. Жирорастворимые
А – ретинол;
D – кальциферол;
Е – токоферол;
К
– антигеморрагический.


















![ФИЗИОЛОГО-БИОХИМИЧЕСКИЕ ОСНОВЫ ФКиС хроматографияХроматография [гр. сhrömatos − цвет + graphö − пишу] — метод разделения, анализа](/img/tmb/13/1262026/95b8f521de0b43ff4f96c03462b98d12-720x.jpg)